
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Коагуляция смесью электролитов
|
|
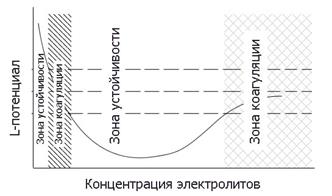
Рис. 4. Изменение z-потенциала и зоны устойчивости в случае неправильных рядов коагуляции.
Коагулирующая способность смесей электролитов, из которых каждый вызывает коагуляции золя при определённой концентрации не всегда аддитивна. В сравнительно редких случаях каждый электролит действует соответственно своей коагулирующей способности, и их действие суммируется, т.е. наблюдается аддитивность коагулирующего действия.
Чаще же наблюдается снижение коагулирующей способности активности одного электролита другим. Подобное взаимодействие называют антагонизмом ионов.Явление сенсибилизации – явление, обратное антогонизму, когда коагулирующее действие каждого из ионов-коагуляторов в присутствии другого иона-коагулятора в смеси повышается.
Опыт № 3. ОПРЕДЕЛЕНИЕ ПОРОГА КОАГУЛЯЦИИ ЗОЛЯ ОКСОГИДРОКСИДА ЖЕЛЕЗА НЕЙТРАЛЬНЫМИ СОЛЯМИ.
Работа проводится с золем оксогидроксида железа, полученным вышеописанным методом. Порог коагуляции определяется при добавлении к золю раствора K2SO4 с концентрацией 0, 05 моль экв/л.
B пять чистых пробирок наливают из бюретки по 4 мл испытуемого золя, раствор соли K2SO4 разбавляют дистиллированной водой в отношении 1: 5; 1: 10; 1: 15; 1: 20; 1: 25 и в каждую из пробирок с золем добавляет по 1 мл раствора различной концентрации.
После прибавления раствора соли K2SO4 пробирки несколько раз встряхивают.
Пробирки группируют по добавленной соли, располагая их в штативе в ряд от низкой концентрации к высокой. Отмечают пробирки, в которых наступила коагуляция.
Затем готовят вторую серию из пяти разбавлений соли так, чтобы концентрация растворов находилась между двумя значениями концентраций, где произошла коагуляция и где она не наступила. Вторично замечают пробирку с наименьшим количеством соли, где наступила явная коагуляция.
Результаты наблюдения коагуляции записывают в таблицу. Наличие коагуляции отмечают знаком +, отсутствие коагуляции знаком –, например:
Таблица 2
| Соль | Первая серия разбавлений | |||||||
| 1: 25 | 1: 20 | 1: 15 | 1: 10 | 1: 5 | ||||
| K2SO4 | - | - | + | + | + | |||
| Соль | Вторая серия разбавлений | |||||||
| 1: 14 | 1: 13 | 1: 12 | 1: 1 | |||||
| K2SO4 | - | + | + | + | ||||
Вычисление порога коагуляции производится, исходя из значения начальной концентрации раствора соли при смешении его с золем. Так, например, если начальная концентрация раствора составляет 0, 05 моль экв/л, порог коагуляции отвечает разбавлению 1: 18 и при смешании с золем раствор соли разбавляется в отношении 1: 4, то порог коагуляции равен:
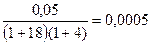 моль экв/л
моль экв/л
|
|