
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Константа химического равновесия. Выведем константу равновесия для обратимых химических реакций (в общем виде) aA + bB = mM + nN . (10)
|
|
Выведем константу равновесия для обратимых химических реакций (в общем виде)
| aA + bB = mM + nN. | (10) |
Применим закон действия масс и запишем выражения скорости прямой и обратной реакций:
· скорость прямой реакции: vпр. = k1[A]a[B]b (11)
· скорость обратной реакции: vобр. = k2[N]n[M]m (12)
· в состоянии равновесия: vпр. = vобр. , т.е. k1[A]a[B] b= k2[N]n[M]m (13)
Переносим постоянные величины (константы скорости) в левую часть равенства, а переменные (концентрации) – в правую часть равенства, т.е. записываем данное равенство в виде пропорции:
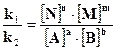 . .
| (14) |
Так как величины k1 и k2 в определенных условиях постоянны, то и отношение их тоже будет постоянной величиной для данной системы. Её обозначают К и называют константой равновесия.
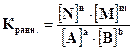 . .
| (15) |
В выражение константы входят равновесные концентрации веществ, взятые в степенях, равных коэффициентам перед веществом в уравнении реакции.
Константа равновесия отражает глубину протекания процесса. Чем больше величина константы равновесия, тем выше концентрация продуктов реакции в момент равновесия, т.е. тем полнее протекает реакция.
Константа равновесия зависит от природы реагирующих веществ, но не зависит от присутствия катализатора, так как он в равной степени ускоряет как прямую, так и обратную реакции. Влияние других факторов (концентрации веществ, давления газов и температуры) на величину константы равновесия мы разберем ниже на конкретных примерах
Рассмотрим вывод выражения константы равновесия на конкретных примерах.
Пример 2. для реакции: N2(г) +3H2(г) Û 2NH3(г)
Vпр = k1[N2][H2]3 ; Vобр. = k2 [NH3]2. Если Vпр= Vобр., то k1[N2][ H2]3 = k2[NH3]2,
константа химического равновесия будет равна 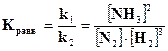 .
.
Если в реакции участвуют твердые вещества (гетерогенная система), то концентрация их не входит в выражение скорости реакции (т.к. остается постоянной в единице поверхности в единицу времени), а следовательно - константы равновесия.
Пример 3. для реакции: С(тв.) + О2 (г) Û СО2(г) константа химического равновесия будет равна 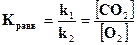 .
.
Пример 4. В обратимой химической реакции А + 2В Û С равновесие наступило при следующих равновесных концентрациях: [А] = 0, 6 моль/л; [В] = 1, 2 моль/л; [С] = 2, 16 моль/л. Определить константу равновесия и исходные концентрации вещества А и В.
Решение. Вычисляем константу равновесия: 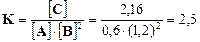 .
.
чтобы определить исходные концентрации веществ А и В, нужно учесть, что согласно уравнению реакции А + 2В Û С из одного моля вещества А и двух молей вещества В образуется один моль вещества С. отсюда следует, что на образование каждых 2, 16 молей вещества С пошло 2, 16 моля вещества А и 2, 16·2=4, 32 моля вещества В. Тогда число молей вещества А и В до начала реакции равнялось: [А]исх. =0, 6+2, 16=2, 76 моль/л, [ В]исх. =1, 2+4, 32=5, 54 моль/л.
|
|