
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Синтез Сахаров при обращении гликолиза
|
|
Реакции гликолиза могут идти в обратном направлении, в результате чего из пирувата вновь будут синтезированы углеводы. Такой обращенный гликолиз носит название глюконеогенеза:
Глюкоза 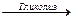 Пируват
Пируват
Глюкоза 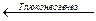 Пируват
Пируват
 Большинство реакций гликолиза близки к равновесию и легко обратимы. Только три реакции, катализируемые киназами (гексокиназой, фосфофруктокиназой и пируваткиназой), необратимы. На этих участках гликолиз идет в обратном направлении с помощью других ферментов и реакций (см. рис. 4.3). Для обращения реакции, катализируемой пируваткиназой, и получения ФЕП из пирувата необходим обходной путь, в котором участвуют ферменты цитозоля и митохондрий. Сначала пируват поступает в митохондрии, где при участии пируваткарбоксилазы карбоксилируется в энергозависимой реакции (12) с образованием оксалоацетата (ОАА). В митохондриях ОАА восстанавливается за счет НАДН с образованием малата (13) при участии НАД-зависимой малатдегидрогеназы. Этот фермент катализирует легко обратимую реакцию, которая идет в направлении синтеза малата, так как соотношение НАДН/НАД
Большинство реакций гликолиза близки к равновесию и легко обратимы. Только три реакции, катализируемые киназами (гексокиназой, фосфофруктокиназой и пируваткиназой), необратимы. На этих участках гликолиз идет в обратном направлении с помощью других ферментов и реакций (см. рис. 4.3). Для обращения реакции, катализируемой пируваткиназой, и получения ФЕП из пирувата необходим обходной путь, в котором участвуют ферменты цитозоля и митохондрий. Сначала пируват поступает в митохондрии, где при участии пируваткарбоксилазы карбоксилируется в энергозависимой реакции (12) с образованием оксалоацетата (ОАА). В митохондриях ОАА восстанавливается за счет НАДН с образованием малата (13) при участии НАД-зависимой малатдегидрогеназы. Этот фермент катализирует легко обратимую реакцию, которая идет в направлении синтеза малата, так как соотношение НАДН/НАД 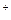 в митохондриях высокое. Далее малат выносится в цитозоль и вновь окисляется до ОАА (14). И наконец, оксалоацетат превращается в ФЕП в энергозависимой реакции, катализируемой
в митохондриях высокое. Далее малат выносится в цитозоль и вновь окисляется до ОАА (14). И наконец, оксалоацетат превращается в ФЕП в энергозависимой реакции, катализируемой
ФЕП-карбоксикиназой (15). Далее фосфоенолпируват легко превращается во фруктозо-1, 6-бисфосфат за счет обращения реакций гликолиза. Обращение реакций (16 и 17), катализируемых гексокиназой и фосфофруктокиназами, достигается при действии соответствующих фосфатаз. Из 6С-сахаров, образованных в результате глюконеогенеза, возможен синтез сахарозы при участии сахарозофосфатсинтазы. Таким образом, в метаболизме растений существует способ синтеза Сахаров из пирувата. Наиболее активно глюконеогенез протекает в прорастающих семенах тех растений, в которых запасными соединениями являются жиры (см. подразд. 4.1.9).
4.1, 5. ОБРАЗОВАНИЕ ВОССТАНОВИТЕЛЬНЫХ ЭКВИВАЛЕНТОВ, АТФ И СО2 В ЦИКЛЕ ТРИКАРБОНОВЫХ КИСЛОТ
В процессе гликолиза освобождается лишь незначительная часть той энергии, которая потенциально заключена в такой сложной молекуле, как глюкоза. В аэробных условиях пируват поступает в митохондрии, где подвергается окончательному окислению с образованием СО2.
Сначала окисление пирувата катализирует сложный пируватдегидрогеназный комплекс (ПДК) (рис. 4.4). В его состав входят три фермента (пируватдегидрогеназа, дигидролипоилтрансацетилаза, дигидролипоилдегидрогеназа) и пять коферментов (тиаминпирофосфат — витамин В1, липоевая кислота, НАД 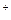 , ФАД и коэнзим А).
, ФАД и коэнзим А).
В реакции окисления пирувата участвует коэнзим А (СоА—SH) — сложная молекула, в составе которой есть активная SH-группа. Коэнзим А функционирует как универсальный переносчик ацетильных групп в разных ферментативных реакциях. Это соединение способно связывать остатки уксусной кислоты с образованием макроэргической тиоэфирной связи в молекуле
ацетил-СоА. Окислительное декарбоксилирование пирувата (7) пируватдегидрогеназным комплексом сопровождается восстановлением НАД 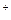 до НАДН, отщеплением СО2 и образованием ацетил-СоА. Ацетил-СоА вступает на путь дальнейших превращений в цикле трикарбоновых кислот (ЦТК), известным также как цикл Кребса, или цикл лимонной кислоты. Цикл был открыт в результате блестящих работ, выполненных в лаборатории английского биохимика Г. А. Кребса в 30-х гг. XX в. на летательных мышцах голубя. Как выяснилось впоследствии, ЦТК — универсальный путь окисления остатков уксусной кислоты, включенный как обязательный компонент в дыхательный метаболизм аэробных организмов. У животных и растений все ферменты цикла кодируются ядерными генами, обладают несомненным сходством и, за единственным исключением, локализованы в матриксе митохондрий.
до НАДН, отщеплением СО2 и образованием ацетил-СоА. Ацетил-СоА вступает на путь дальнейших превращений в цикле трикарбоновых кислот (ЦТК), известным также как цикл Кребса, или цикл лимонной кислоты. Цикл был открыт в результате блестящих работ, выполненных в лаборатории английского биохимика Г. А. Кребса в 30-х гг. XX в. на летательных мышцах голубя. Как выяснилось впоследствии, ЦТК — универсальный путь окисления остатков уксусной кислоты, включенный как обязательный компонент в дыхательный метаболизм аэробных организмов. У животных и растений все ферменты цикла кодируются ядерными генами, обладают несомненным сходством и, за единственным исключением, локализованы в матриксе митохондрий.
Первой реакцией цикла можно считать реакцию конденсации ацетил-СоА с оксалоацетатом с образованием цитрата (2), катализируемую цитратсинтазой (см. рис. 4.4).
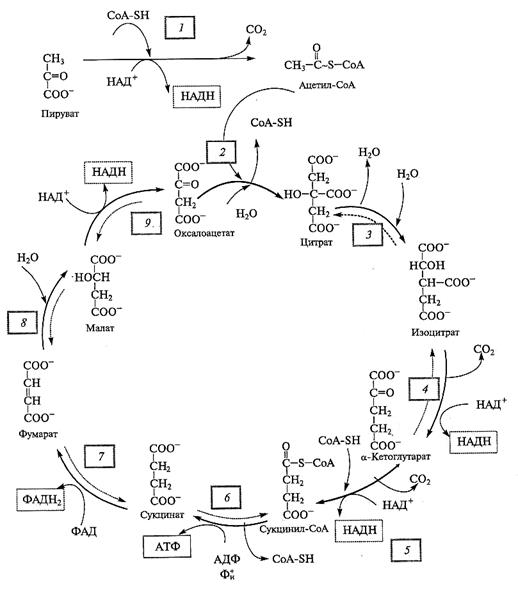
Рис. 4.4. Окисление пирувата в матриксе митохондрий через пируватдегидрогеназный
комплекс и цикл трикарбоновых кислот.
Окислительное декарбоксилирование пирувата сопровождается выделением СО2, восстановлением НАДН и синтезом ацетил-СоА. В реакции, катализируемой цитратсинтазой, ацетил-СоА конденсируется с оксалоацетатом с образованием цитрата. В ЦТК цитрат окисляется с выделением двух молекул СО2, в результате вновь синтезируется оксалоацетат. В реакциях ЦТК образуются 3 НАДН и 1 ФАДН2, а также синтезируется 1 АТФ. Образованный оксалоацетат вновь реагирует с ацетил-СоА, запуская следующий оборот цикла. Реакции 1— 9 катализируют следующие ферменты: 1 — пируватдегидрогеназный комплекс; 2 — цитратсинтаза; 3 — аконитаза; 4 — НАД-зависимая изоцитратдегидрогеназа; 5 — α -кетоглутаратдегидрогеназный комплекс; б — сукцинил-СоА-синтетаза; 7 — сукцинатдегидрогеназа; 8 — фумараза; 9 — НАД-зависимая малатдегидрогеназа
Изомеризация цитрата в изоцитрат включает две реакции, связанные сначала с отщеплением, а затем присоединением воды (3). Обе реакции катализируются одним ферментом — аконитазой. Далее следуют две реакции окислительного декарбоксилирования, каждая из которых связана с восстановлением НАД 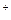 и выделением СО2. Сначала НАД-зависимая изоцитратдегидрогеназа окисляет изоцитрат (4) с образованием α -кетоглутарата, СО2 и НАДН. Эта самая медленная реакция определяет скорость оборота всего цикла. Образованный α -кетоглутарат подвергается дальнейшему окислению α -кетоглутаратдегидрогеназным комплексом, который по своей структуре и механизму действия является аналогом ПДК. В результате реакции (5) образуются НАДН, СО2 и сукцинил-СоА. Далее сукцинил-СоА-синтетаза катализирует превращение сукцинил-СоА в сукцинат (6), что сопровождается фосфорилированием АДФ за счет энергии тиоэфирной связи в молекуле сукцинил-СоА. Это единственная реакция цикла, в которой за счет субстратного фосфорилирования синтезируется АТФ (растения) или ГТФ (животные).
и выделением СО2. Сначала НАД-зависимая изоцитратдегидрогеназа окисляет изоцитрат (4) с образованием α -кетоглутарата, СО2 и НАДН. Эта самая медленная реакция определяет скорость оборота всего цикла. Образованный α -кетоглутарат подвергается дальнейшему окислению α -кетоглутаратдегидрогеназным комплексом, который по своей структуре и механизму действия является аналогом ПДК. В результате реакции (5) образуются НАДН, СО2 и сукцинил-СоА. Далее сукцинил-СоА-синтетаза катализирует превращение сукцинил-СоА в сукцинат (6), что сопровождается фосфорилированием АДФ за счет энергии тиоэфирной связи в молекуле сукцинил-СоА. Это единственная реакция цикла, в которой за счет субстратного фосфорилирования синтезируется АТФ (растения) или ГТФ (животные).
Сукцинат окисляется до фумарата (7) сукцинатдегидрогеназой. Этот фермент локализован не в матриксе, а во внутренней мембране митохондрий и представляет собой один из компонентов дыхательной цепи — комплекс II. В ходе окисления сукцината электроны передаются на молекулу ФАД, которая является простетической группой в составе комплекса. Электроны с ФАДН2 прямо уходят в дыхательную цепь. Таким образом, сукцинатдегидрогеназа — это общий компонент ЦТК и дыхательной цепи (см. подразд. 4.2.3). Далее фумараза гидратирует фумарат с образованием малата (8). И наконец, цикл замыкается реакцией окисления малата в оксалоацетат (9) при участии НАД-зависимой малатдегидрогеназы. Это третья реакция цикла, в которой генерируются НАДН. Хотя данная реакция легкообратима, in vivo ее равновесие сдвинуто в сторону образования оксалоацетата. Сдвиг происходит потому, что продукты реакции быстро используются: оксалоацетат вновь реагирует с очередной молекулой ацетил-СоА и вступает в следующий оборот цикла, а НАДН окисляется в дыхательной цепи. Хотя большинство реакций цикла обратимы, две из них, катализируемые цитратсинтазой и α -кетоглутаратдегидрогеназным комплексом, физиологически необратимы и контролируют направление цикла.
Таким образом, в матриксе митохондрий завершается процесс окисления глюкозы, начавшийся в цитозоле. В результате действия ПДК и одного оборота ЦТК молекула пирувата полностью окисляется с образованием 3 молекул СО2. Окисление пирувата сопровождается образованием 4 молекул НАДН, восстановлением ФАД и синтезом одной молекулы АТФ.
Энергетический выход при окислении глюкозы принято приравнивать к 36 молекулам АТФ. Эта цифра базируется на том, что окисление в дыхательной цепи НАДН, образованного в ЦТК, связано с синтезом трех молекул АТФ, а ФАДН2 — двух. Образованный в цитозоле НАДН также может быть окислен в цепи с образованием двух молекул АТФ (см. подразд. 4.2.6 и 4.2.9). При полном окислении глюкозы 2НАДН образуются при гликолизе в цитозоле, 8НАДН и 2ФАДН2 — в матриксе при окислении двух молекул пирувата. При окислении всех восстановленных эквивалентов в дыхательной цепи в сумме может быть получено 32 АТФ. Если учесть 4 молекулы АТФ, образованных на уровне субстратного фосфорилирования (2 АТФ в гликолизе и 2 АТФ в ЦТК), общий итог составит 36 молекул АТФ. Следует отметить, что эта цифра достаточно приблизительна и скорее всего завышена. Ряд данных указывает на то, что число молекул АТФ, синтезированных при окислении НАДН, может быть меньше трех (см. подразд. 4.2.7).
|
|