
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Інструктаж з БЖД
|
|
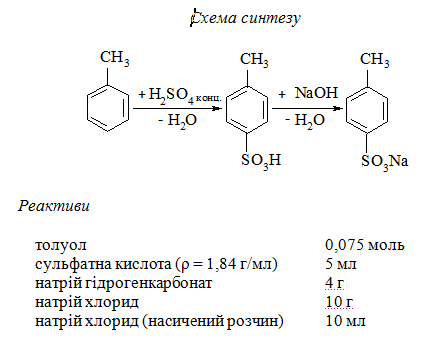
Тема: Реакції сульфування
МЕТА: Одержання натрієвої солі пара–толуолсульфокислоти п -CH3С6Н4SO3Na
РОБОЧЕ МІСЦЕ: ХІМІЧНА ЛАБОРАТОРІЯ
ТРИВАЛІСТЬ ЗАНЯТТЯ: 6 ГОДИН
МЕТА ПРОВЕДЕННЯ ЗАНЯТТЯ:
ЗАКРІПЛЕННЯ ТЕОРЕТИЧНИХ ЗНАНЬ З ТЕМИ,
ПІДТВЕРДЖЕННЯ ТЕОРЕТИЧНИХ ЗНАНЬ ПРИ ВИКОНАННІ ЛАБОРАТОРНИХ ДОСЛІДІВ; ОВОЛОДІННЯ МЕТОДОМ СИНТЕЗУ.
МАТЕРІАЛЬНО-ТЕХНІЧНЕ ОСНАЩЕННЯ РОБОЧОГО МІСЦЯ:
Толуол, концентрована сульфатна кислота, натрій карбонат, натрій хлорид.
Стакан, холодильник оборотний, колба круглодонна, воронка Бюхнера, водяний насос, кипілки, водяна баня, промивалка.
ПРАВИЛА ОХОРОНИ ПРАЦІ:
Дотримуватися обережності при поводженні з хімічними реактивами, скляним посудом, електричним нагрівальним приладом. Синтез проводити у витяжній шафі.
Реакція сульфування - це процес введення в молекулу органічної речовини сульфогрупи -SO3H.
Речовини, до складу яких входить сульфогрупа називають сульфуючими агентами (сульфатна кислота, її оксиди, естери тощо). Речовини, до молекул яких вводиться сульфогрупа - сульфуються. Продукти реакцій сульфування - це сульфокислоти, які застосовуються при виробництві фенолів, нафтолів, лікарських препаратів, фарбників, миючих та дезінфікуючих засобів.
Інструктаж з БЖД
ЗМІСТ І ПОСЛІДОВНІСТЬ ВИКОНАННЯ ЗАВДАНЬ:
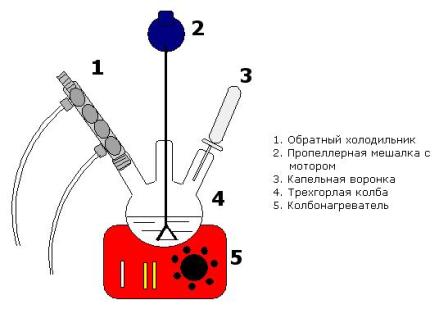
1. В круглодонну колбу приладу 1 поміщають 16 мл толуолу і обережно вносять 9, 5 мл концентрованої сульфатної кислоти. Реакційну рідину протягом 1 години слабо кип'ятять, час від часу струшуючи колбу (для перемішування шарів).
| Змн. |
| Арк. |
| № докум. |
| Підпис |
| Дата |
| Арк. |
| Т 00. 5.05130101.08. ЛР |
3. Потім теплу реакційну суміш виливають в склянку з 18 мл води (якщо суміш почне кристалізуватись, її необхідно підігріти) та колбу ополіскивають із промивалки.
4. Кислий розчин обережно нейтралізують 2 г карбоната натрія, додаючи його невеликими порціями, додають у розчин 5 г хлорида натрія і нагрівають суміш до кипіння (якщо хлорид натрію не розчиняється додають ще трохи води).
5. Розчин охолоджують водою з льодом.
6. Кристали натрієвої солі n-толуолсульфокислоти, які випали в осад, відсмоктують на воронці Бюхнера і віджимають між листами фільтровального паперу.
МЕТОДИЧНІ РЕКОМЕНДАЦІЇ ЩОДО ВИКОНАННЯ Й ОФОРМЛЕННЯ:
1. При виконанні дослідів строго дотримуватися кількості реагентів та методики виконання роботи, які вказані в інструкції, а також заходів техніки безпеки.
2. Розрахувати практичний вихід (%) пара-толуолсульфокислоти.
3. По закінченню роботи зробити загальний висновок.
Виділення продукту.
Реакційну суміш охолоджують і теплою виливають в конічну колбу, заповнену 30 мл води. Кислий розчин частково нейтралізують, при доданні невеликими порціями твердого натрій гідрогенкарбонату (обережно – спінення!). Потім додають твердий натрій хлорид та нагрівають суміш до повного розчинення солі.
Гарячий розчин фільтрують через лійку для гарячого фільтрування. З охолодженого фільтрату кристалізується натрій пара-толуолсульфонат. Кристалічний осад відділяють вакуумним фільтруванням на лійці Бюхнера, промивають 10 мл насиченого розчину натрій хлориду, висушують і зважують.
| Змн. |
| Арк. |
| № докум. |
| Підпис |
| Дата |
| Арк. |
| Т 00. 5.05130101.08. ЛР |
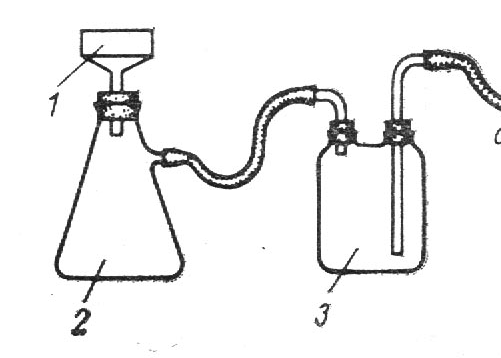
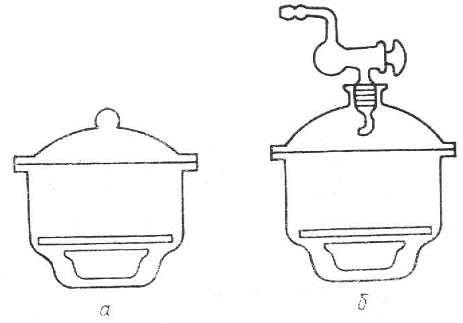
- – воронка Бюхнера;
- – колба з тубусом (колба Бунзена);
- – запобіжна склянка (склянка Вульфа).
Рисунок 3 – Прилад для відсмоктування (для фільтрування у вакуумі)
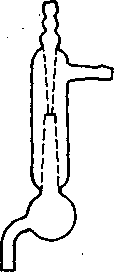
Рисунок 4 – Водоструйний скляний вакуум – насос.
Таблиця - Властивості вихідних речовин і продуктів реакції
| Речовина | Молярна маса | Температура плавлення t, °С | Температура кипіння t, °С | Густина ρ, кг/м3 | Показник заломлення n 20D | Розчинність, s | Примітка |
| Толуол | |||||||
| Кальцій карбонат | |||||||
| Сульфатна кислота | |||||||
| Натрій хлорид | |||||||
| пара – толуол-сульфокис-лота |
ЗАХИСТ РОБОТИ:
Дати визначення реакції сульфування.
Навести рівняння основних і побічних реакцій, які відбуваються при одержанні
пара-толуолсульфокислоти.
Пояснити схеми приладів для синтезу пара -толуолсульфокислоти.
Пояснити розрахунок виходу пара-толуолсульфокислоти.
ЗАВДАННЯ ДЛЯ САМОСТІЙНОЇ РОБОТИ:
Які сульфуючі агенти використовуються для проведення реакції сульфування.
Чому при сульфуванні використовуються великий надлишок сульфатної кислоти.
Чому температура є важливим чинником, який впливає на хід реакції сульфування.
Пояснити фізико-хімічні властивості пара -толуолсульфокислоти.
Пояснити області використання пара-толуолсульфокислоти.
Яких заходів техніки безпеки необхідно додержуватись при синтезах пара-толуолсульфокислоти?
РОЗРАХУНКИ ТА ВИСНОВКИ:
| Змн. |
| Арк. |
| № докум. |
| Підпис |
| Дата |
| Арк. |
| Т 00. 5.05130101.08. ЛР |
1. Храмкина М.Н. Практикум по органическому синтезу.- Л.: Химия, 1988. С 216-218, 222 – 224.
2. Храмкина М.Н. Практикум по органическому синтезу.- М.: Химия, 1974.
3. Гороновский И.Г. Краткий справочник по химии.- К.: Наукова думка, 1974.
4. Потапов В.М., Татаринчик С.Н. Органическая химия. М.: Химия, 1980.
5. Аверина А.В. Лабораторный практикум по органической химии.- М.: Высш.шк., 1980.
6. Березан О.М. Органічна хімія.- К.: Абрис, 2000.
7. Липатников В.Е. Лабораторные работы по неорганической и органической химии.- М.: Высш.шк., 1981.
Витрачено робочих годин __________________
Препарат здано_____________________________ Відмітка про здачу речовини
Підпис викладача
|
|