
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Дипломна робота. на державний випускний кваліфікаційний екзамен
|
|
на державний випускний кваліфікаційний екзамен
з підготовки робочої професії
лаборант хімічного аналізу
на тему:
«Аналіз готової продукції у виробництві нітратної кислоти»
Виконала:
учениця групи №5
Дмитришина А. Р.
Керівник:
Боярчук Є. М.
Рівне 201
Зміст
І. Вступ.....................................................................................................................3
ІІ. Основна частина:
5. Технологічний процес виробництва нітратної кислоти......................................................................................................5
6. Аналізи у виробництві...........................................................................14
7. Описання приладу КФК-3.....................................................................26
8. Заходи з охорони праці і техніки безпеки...........................................36
ІІІ. Висновки..........................................................................................................37
IV. Список літератури...........................................................................................38
V. Рецензія.............................................................................................................39
№I. Вступ
ПАТ”Рівнеазот”представляє хімічне підприємство, розташоване у північно-західній частині України на відстані 15 км від міста Рівне. Це - хімічний гігант України зі своєю історією, наполегливим та працьовитим трудовим колективом, який творить його сьогодення.
Публічне акціонерне товариство " Рівнеазот" створене 13.11.1995 року на базі орендного підприємства " Азот", яке до 1994 року мало статус державного підприємства. В 2003 році на підприємстві завершено процес приватизації. Пріоритетним напрямком в його діяльності стало впровадження у виробництво заходів, спрямованих на підвищення ефективності діючих цехів, модернізацію обладнання, поліпшення якості продукції та розширення її асортименту.
Для виготовлення і пакування своєї продукції підприємство використовує сировину і матеріали:
- природний газ;
- бензол;
- сірчану кислоту;
- доломіт;
- брусит;
- соду каустичну;
- вапно будівельне;
- ліламін;
- мішки;
- м'які контейнери типу " біг-бег";
- каталізатори;
- хімреактиви.
Наша продукція.
Мінеральні добрива:
1 Селітра аміачна
2 Вапняково-аміачна селітра
3 Аміак рідкий
4 Аміак водний технічний
5 Тукосуміш " Рівне-NРК"
Технологічні процеси на підприємстві
Виробництво аміаку
Виробництво аміачної води
Виробництво неконцентрованої азотної кислоти
Виробництво аміачної селітри..
— Виробництво екстракційної фосфорної кислоти
Виробництво циклогексанолу Виробництво адипінової кислоти
№II.Основна частина:
1)Технологічний процес виробництва.
Азотна кислота (HNO3) – безколірна чи жовтувата рідина. Дуже гігроскопічна, " димить" на повітрі, оскільки її пара з вологою повітря утворює краплі туману. Як сильний окисник бурхливо реагує з відновниками. Солома, тирса та інші органічні матеріали, облиті кислотою, загораються, виділяючи при цьому діоксид азоту.
Токсична, може викликати хімічні опіки при потраплянні на шкіру і слизові оболонки, подразнює дихальні шляхи (пара азотної кислоти), може викликати пошкодження зубів, кон'юктивіти. Пари НNO3 на 25% токсичніші, ніж NO2. При важких отруєннях - набряк легень, слабкість, блювота, ядуха, кашель з сильною мокротою, пошкодження зубів, пальців рук. При легких – бронхіт.
При попаданні на шкіру викликає її омертвіння, з'являються водянисті пухирці, які при розривах перетворюються в довго не заживаючі рани.
Використовується для виробництва добрив, органічних барвників, для травлення металів, у виробництві сірчаної кислоти за нітрозним методом та для виготовлення целюлозних лаків.
Кислота азотна використовується як окислювач в багатьох хімічних процесах. Пакування і транспортування: кислоту заливають в скляні бутелі, бочки і бідони для нехарчових продуктів, в щільно закриті посудини, виготовлені із корозійнотривкої сталі. Зберігається в упакуванні виробника в критих складських темних приміщеннях окремо від інших реактивів при температурі не вище 300С. Транспортують в залізничних цистернах з написом " Обережно", " Азотна кислота". Закупорені і марковані бутелі поміщають у вторинну транспортну
Стадії виробництва
— Підготовка і компримування повітря
— Підготовка газоподібного аміаку
— Підготовка аміачно-повітряної суміші
— Конверсія аміаку та охолодження нітрозного газу
— Абсорбція оксидів азоту
— Селективне очищення хвостових газів від залишкових оксидів азоту
— Рекуперація енергії тиску і теплоти очищених хвостових газів
— Видача та зберігання продукційної кислоти
Коротка характеристика технологічного процесу виробництва азотної кислоти
Виробництво неконцентрованої азотної кислоти складається з наступних стадій:
Підготовка і компримування повітря.
Підготовка газоподібного аміаку.
Підготовка аміачно-повітряної суміші.
Конверсія аміаку та охолодження нітрозного газу.
Абсорбція оксидів азоту.
Селективне очищення хвостових газів від залишкових оксидів азоту.
Рекуперація енергії тиску і теплоти очищених хвостових газів.
Видача та зберігання продукційної кислоти.
Підготовка і компримування повітря.
Атмосферне повітря осьовим компресором газотурбінної установки ГТТ-3М всмоктується через повітрозабірну трубу в апарат очищення повітря поз. IX), в якому проходить двоступеневе очищення від пилу і твердих домішок на касетних фільтрах:
грубе очищення - на лавсановому фільтрі елементу Ф-1, 8;
тонке очищення - на фільтрі Петрянова елементу Д-33КЛ;
Із апарату поз. IX повітря надходить в газотурбінну установку ГТТ-3М, де, осьовий компресор поз. Іа стискує повітря до тиску 0, 250 - 0, 293 МПа з підвищенням температури до 175 0С. Потім повітря охолоджується в повітроохолоджувачі поз. Ід до температури не більше 48 0С оборотною водою. Після повітроохолоджувача поз. Ід повітря під тиском 0, 247- 0, 290 МПа надходить в нагнітач поз. Іг, в якому стискується до 0, 80 МПа з підвищенням температури не вище 175 0С.
Після нагнітача основна частина повітря направляється в технологічний цикл безпосередньо на окислення аміаку.
Підготовка газоподібного аміаку.
Газоподібний аміак утворюється в процесі випаровування рідкого аміаку у випарнику поз. 11вузла підготовки аміаку (ВПА).
Рідкий аміак під тиском 1, 3-1, 5 МПа надходить в випарник поз. 11 із мережі підприємства попередньо очистившись від механічних домішок і каталізаторного пилу на магнітному фільтрі, який розміщений на вході рідкого аміаку в цех. Випаровування рідкого аміаку відбувається під тиском 1, 08-1, 20 МПа і температурі 30º С за рахунок теплоти пари, яка надходить в трубний простір випарника з температурою 230-250º С під тиском 1, 5 МПа. В міжтрубному просторі знаходиться рідкий і газоподібний аміак.
Із випарника поз.11газоподібний аміак надходить в фільтр поз.11а, в якому очищується від масла і механічних домішок.
Очищений газоподібний аміак після фільтру надходить в трубний простір підігрівача газоподібного аміаку поз.11г, в якому підігрівається до температури не менше 100-110º С за рахунок теплоти пари, яка надходить в міжтрубний простір з температурою 180-200º С під тиском 0, 6 МПа.
Після підігрівача газоподібного аміаку поз.11ггазоподібний аміак з температурою не менше 100º С направляється в змішувач поз. 2. Частина газоподібного аміаку після вузла підготовки аміаку надходить в реактор селективної очистки поз.5 Конденсат із випарника поз.11 і підігрівача поз.11г окремими загально цеховими колекторами надходить в збірник цехового конденсату поз. 28.
Підготовка аміачно-повітряної суміші (АПС).
Після нагнітача поз. Іг повітря під тиском до 0, 80 МПа з температурою не більше 175º С надходить в змішувач поз.2.
Аміак надходить в трубки знизу, повітря надходить в міжтрубний простір також знизу. Аміак і повітря змішуються на виході із трубної решітки в завихрювачі, який розміщений над трубною решіткою.
Газоподібний аміак надходить в змішувач під тиском до 0, 80 МПа з температурою не менше 80С. Співвідношення аміак-повітря в АПС підтримується регулятором співвідношення постійним в межах 9, 5-11, 0% об’ємних. Частина газоподібного аміаку, який надходить в змішувач, направляється в реактор селективної очистки поз.5.
Після змішування аміаку і повітря в змішувачі поз.2, утворена АПС очищується від пилу, механічних домішок, масла на патронних фільтрах, розміщених в верхній частині змішувача..
Конверсія аміаку та охолодження нітрозного газу.
Аміачно-повітряна суміш із змішувача поз.2 з температурою 140-230º С надходить в контактний апарат поз.3, в якому при температурі 850-910º С на каталізаторі відбувається окислення аміаку киснем, який знаходиться в АПС, з утворенням оксиду азоту, водяної пари та елементарного азоту за реакціями:
4NH3 + 5O2 = 4NO + 6H2O + 905, 8 кДж (1)
4NH3 + 4O2 = 2N2O + 6H2O + 1103 кДж (2)
4NH3 + 3O2 = 2N2 + 6H2O + 1267 кДж (3)
Основною є перша реакція. Вихід оксиду азоту від кількості аміаку, який іде на окислення, повинен складати не менше 93, 5 % вагових.
Окислення аміаку відбувається на пакеті платино-родієвих сіток,.
Утворені на каталізаторі нітрозні гази (NOX, N2, H2O) з температурою 850-9100С надходять в котел-утилізатор, де охолоджуються до температури 300-3800С. За рахунок теплоти нітрозних газів в котлі відбувається випаровування деаерованої хімочищеної води з утворенням пари тиском не більше 1, 5 МПа і температурою 230-250º С.
В об’ємі котла частково проходить реакція окислення оксиду азоту в двооксид азоту з виділенням теплоти. Нітрозні гази після котла-утилізатора надходять в підігрівач хвостових газів ІІ ступені поз.1.
В підігрівачі хвостових газів ІІ ступені за рахунок охолодження нітрозних газів від температури 300-380º С до температури 210-260º С хвостові гази підігріваються від температури 110-140º С до температури 240-300º С.
З підігрівача хвостових газів ІІ ступені поз.1 нітрозні гази надходять в підігрівач хвостових газів І ступені поз.6, де за рахунок підігріву хвостових газів охолоджуються до температури 140-190º С.
Абсорбція оксидів азоту.
Після підігрівача хвостових газів І ступені поз.6 нітрозні гази з температурою не більше 197º С надходять в міжтрубний простір холодильників-конденсаторів поз.7, 7а, де охолоджуються до температури 800С оборотною водою, яка подається в трубний простір від абсорбційної колони поз.8. В холодильниках-конденсаторах в міжтрубному просторі відбувається конденсація водяної пари і утворення азотної кислоти з масовою часткою моногідрату 40-50%.
Оборотна вода подається в холодильники-конденсатори після змійовиків абсорбційної колони поз.8. Кислота з холодильників-конденсаторів подається на одну з тарілок абсорбційної колони з відповідною концентрацією.
Нітрозні гази після холодильників-конденсаторів надходять в кубову частину абсорбційної колони під першу тарілку і проходять вверх колони через 47 сітчастих тарілок. На 46 тарілку подається насосами знесолена вода з температурою не більше 35º С.Утворена на верхній тарілці слабка азотна кислота перетікає на нижче розташовані тарілки, рухаючись назустріч нітрозному газу. Масова частка азотної
Процес абсорбції двооксиду азоту - екзотермічний. Для відведення теплоти, яка виділяється в процесі абсорбції, на тарілках розміщено змійовики, по яких проходить оборотна вода. Підведення і відведення оборотної води виконано індивідуально для кожної тарілки.
Після абсорбційної колони оборотна вода з температурою не більше 30º С направляється в холодильники-конденсатори. Далі оборотна вода з температурою не більше 35º С направляється в оборотний цикл.В процесі утворення азотної кислоти в абсорбційній колоні накопичуються хлориди, які посилюють корозію металу. З метою запобігання їх накопичення і зменшення корозійної дії на матеріал колони схемою передбачено відвід хлоридів з тарілок абсорбційної колони в цеховий колектор азотної кислоти.
Допустима масова концентрація хлоридів на тарілках абсорбційної колони становить не більше 500 мг/дм3. З метою підвищення ступеня абсорбції схемою передбачено подачу додаткового повітря для доокислення нітрозних газів в трубопровід нітрозних газів після холодильників-конденсаторів поз.7, 7а. З абсорбційної колони азотна кислота надходить в віддувну колону поз.12, де на тарілках сітчастого типу гарячим повітрям азотна кислота віддувається від оксидів азоту до масової концентрації останніх не більше 0, 1%.
Освітлена азотна кислота після віддувної колони направляється на склад в сховища кислоти або безпосередньо на виробництво адипінової кислоти. Віддуті із віддувної колони гази надходять в трубопровід нітрозних газів перед абсорбційною колоною поз.8 Не абсорбовані хвостові гази після абсорбційної колони з об'ємною часткою оксидів азоту не більше 0, 11% і об'ємною часткою кисню не більше 1, 7-4, 0% надходять в підігрівач хвостових газів І ступені поз.6, де за рахунок теплоти нітрозних газів підігріваються до температури 110-140º С.
Селективне очищення хвостових газів від залишкових оксидів азоту.
Хвостові гази після підігрівача хвостових газів І ступені поз.6 надходять в підігрівач хвостових газів ІІ ступені, де за рахунок охолодження нітрозних газів підігріваються до температури 240-300º С і направляються в реактор селективного очищення.В реакторі на каталізаторі АВК-С)) відбувається відновлення оксидів азоту за реакціями:
6NO + 4NH3 = 5N2 + 6H2O + Q;
6NO2 + 8NH3 = 7N2 + 12H2O + Q;
4NH3 +3O2 = 2N2 + 6H2O + Q;
Газоподібний аміак подається безпосередньо в трубопровід хвостових газів перед реактором поз.5.
Рекуперація енергії тиску і теплоти очищених хвостових газів.
Очищені хвостові гази після реактора селективного очищення поз.5) проходять між зовнішнім і внутрішнім корпусами універсальної камери згоряння турбіни поз. Ів і змішуються з топковими газами, які виходять з камери згоряння турбіни, і з температурою не більше 700º С надходять в газову турбіну.
Сталість температури газової суміші на вході в турбіну забезпечується відповідним режимом роботи камери згоряння турбіни агрегату ГТТ-3М.
Відпрацьовані в турбіні гази з температурою 390-410º С під тиском 0, 006 МПа надходять в котел-утилізатор хвостових газів. В котлі виробляється пара тиском не більше 1, 5 МПа) і температурою 230-250º С за рахунок теплоти хвостових газів.
Хвостові гази після котлів-утилізаторів хвостових газів проходять через економайзер котла-утилізатора нітрозних газів і викидаються в атмосферу через вихлопні труби висотою 151м і 153м.
Зберігання і видача продукційної кислоти.
Освітлена в віддувній колоні азотна кислота з масовою часткою оксиду азоту не більше 0, 1% і масовою часткою моногідрату (МНГ) азотної кислоти не менше 57, 0% по двох колекторах надходить в сховища поз.1021-8 складу Із сховищ азотна кислота насосами подається на виробництво аміачної селітри, на виробництво адипінової кислоти, в цех складних мінеральних добрив. Схемою передбачено подачу азотної кислоти на виробництво АК безпосередньо з віддувних колон.
Крім цього, схемою передбачено наливання азотної кислоти в залізничні цистерни для відправки споживачам.
Оксиди азоту (нітрозний газ) -червоно-бурий газ, в склад якого входять NO, NO2, N2O5.
Токсичний, при вдиханні подразнює верхні дихальні шляхи і слизові оболонки, в великих концентраціях викликає набряк легень. Ознаки отруєння – кашель, подразнення дихальних шляхів, головний біль, блювання, неможливість зробити глибокий вдих, подразнення слизової облонки очей, білуватий наліт на яснах. Через 2-12 годин з’являється відчуття страху, сильної слабкості, зростаючий кашель, лихоманка, піднімається температура, блювота, сильна спрага, біль у діафрагмі. Іноді сильна пітливість.
ГДК – 5 мг/м3.
Перша допомога: необхідно перенести потерпілого на свіже повітря (неприпустимо, щоб потерпілий йшов сам навіть при задовільному стані). Спокій, вдихання кисню, запобігання переохолодження, при зупинці дихання – штучне дихання (спосіб Сильвестра), без стискання грудної клітки. При подразненні дихальних шяхів – содові інгаляції, пити гаряче молоко з содою.
Засоби індивідуального захисту: фільтруючий протигаз з коробкою марки " В" або " М", рукавиці гумові, спецодяг, окуляри герметичні.
Перша допомога: при отруєнні парами - свіже повітря, содові інгаляції, пити молоко з содою. При попаданні на шкіру або слизові оболонки - негайно змити, водою, на шкіру - содові примочки.
Засоби індивідуального захисту: спецодяг з тканини КС, чоботи гумові кислотостійкі, окуляри, фільтруючий протигаз з коробкою марки " М" від парів, гумові рукавиці.
Азотна кислота (НNО3). Безбарвна чи жовтувата рідина. Токсична, може викликати хімічні опіки при потраплянні на шкіру і слизові оболонки, подразнює дихальні шляхи (пара азотної кислоти), може викликати пошкодження зубів, кон’юнктивіти. Пари НNO3 на 25% токсичніші, ніж NO2. При важких отруєннях - набряк легень, слабкість, блювання, ядуха, кашель з сильною мокротою, пошкодження зубів, пальців рук. При легких – бронхіт.
При попаданні на шкіру викликає її омертвіння, з'являються водянисті пухирці, які при розривах перетворюються в довго незагоювані рани.
ГДК: 2мг/м3
Перша допомога: при отруєнні парами - свіже повітря, содові інгаляції, пити молоко з содою. При попаданні на шкіру або слизові оболонки - негайно змити водою, на шкіру - содові примочки.
ЗІЗ: спецодяг з тканини КС, чоботи гумові кислотостійкі, окуляри, фільтруючий протигаз з коробкою марки " М" або ДОТ-600 від парів.
Луги (NаОН, КОН) – білі кристалічні речовини. Застосовуються у вигляді розчинів різних концентрацій. Водний розчин лугу - їдка рідина. Розчини лугу токсичні, діють тим сильніше, чим вища концентрація і температура. При попаданні на шкіру луг викликає тяжко загоюванні опіки, після опіків залишаються рубці. При попаданні на слизові оболонки утворюється м’який струп.
Дуже небезпечне попадання лугу в очі, уражаються глибокі частини очей, що може привести до сліпоти.
ГДК - 0, 5 мг/м3. Клас небезпеки – другий.
Перша допомога: при попаданні на шкіру промити уражену ділянку великою кількістю води під сильним струменем на протязі 10 хв., потім прикласти примочку з 2% розчину оцтової чи борної кислоти. При попаданні в очі - промити їх над фонтанчиком на протязі 10-30хв, потім примочки 5% розчином оцтової або лимонної кислоти. Звернутися в медпункт.
2)Аналізи у виробництві:
1)Нітратна кислота.Вміст заліза.
Метод вимірювання:
Вимірювання за цією методикою виконання вимірювання виконують опосередкованим методом, а саме фотоколориметричним методом, який заснований на випарюванні проби, розчиненні залишку трьохвалентного заліза хлористоводневою кислотою, яке при взаємодії з роданистим амонієм утворює забарвлену сполуку. Інтенсивність забарвлення вимірюють на фотоколориметрі.
1 Підготовка приладу до роботи
Колориметр фотоелектричний концентраційний КФК-2 включають згідно з інструкцією до приладу [5]. Час виходу приладу на робочий режим 30 хвилин. Вимірювання виконують при довжині хвилі λ =440 нм.
2 Відбір проби
Пробу азотної кислоти відбирають в місцях, які призначені для пробовідбору в чисту склянку з товстостінного скла з притертою пробкою. Перед відбором склянку обполіскують азотною кислотою, яку відбирають. На склянці роблять надпис з зазначенням назви проби, дати, часу та місця відбору.
Основний стандартний розчин з масовою концентрацією заліза 1 мг/см3 готують згідно з ГОСТ 4212-76.
Із основного стандартного розчину готують робочий стандартний розчин з масовою концентрацією заліза 0, 01 мг/см3. В мірну колбу місткістю 100 см3 вносять піпеткою місткістю 1 см3 основний стандартний розчин в об’ємі 1 см3, доводять об’єм розчину в колбі до риски розчином сірчаної кислоти з молярною концентрацією c(½ H2SO4)=0, 01 моль/дм3.
Побудова градуювального графіка
В мірні колби місткістю 50 см3 послідовно вносять з бюретки місткістю 5 см3 робочий стандартний розчин з масовою концентрацією заліза 0, 01 мг/см3 в об’ємі 0, 5; 1, 0; 1, 5; 2, 0; 2, 5; 3, 0; 3, 5; 4, 0 см3, що відповідає 0, 005; 0, 01; 0, 015; 0, 02; 0, 025; 0, 03; 0, 035; 0, 04 мг заліза.
В кожну колбу циліндром місткістю 25 см3 додають дистильовану воду в об’ємі 25 см3 і піпеткою місткістю 2 см3 вносять розчин хлористоводневої кислоти (конц.) в об’ємі 2 см3, піпеткою місткістю 10 см3 вносять розчин амонію роданистого з масовою часткою 10 % в об’ємі 10 см3. Об’єм розчину в колбах доводять до риски дистильованою водою і ретельно перемішують.
Через 2 хвилини вимірюють оптичну густину кожного розчину на електрофотоколориметрі при довжині хвилі λ =440 нм в кюветах з товщиною поглинаючого світло шару ℓ = 50 мм. Як розчин порівняння використовується розчин, який містить внесені з тією ж послідовністю всі вище зазначені реактиви, крім стандартного розчину.
За отриманими даними будують градуювальний графік, відкладаючи на осі абсцис введену масу заліза (а) в мг, а на осі ординат відповідні їм значення оптичних густин. Градуювальний графік будують в координатах: а, мг – оптична густина D по середніх значеннях з трьох паралельних вимірювань.
Градуювальний графік перевіряють один раз в 90 днів, а також у випадку заміни реактивів або приладів.
Виконання вимірювання:
При виконанні вимірювання масової частки заліза в азотній кислоті виконують наступні операції:
Наважку проби азотної кислоти масою 25, 0 г, зважену на вазі, яка вказана в розд.2, в фарфоровому тиглі випарюють на електроплитці або під інфрачервоною лампою досуха, в охолоджений тигель піпеткою місткістю 2 см3 вносять розчин хлористоводневої кислоти (конц.) в об’ємі 2 см3. Вміст тигля кількісно переносять в мірну колбу місткістю 50 см3, циліндром місткістю 25 см3 додають дистильовану воду в об’ємі 25 см3 і піпеткою місткістю 10 см3 вносять розчин амонію роданистого з масовою часткою 10 % в об’ємі 10 см3. Об’єм розчину в колбі доводять до риски дистильованою водою і ретельно перемішують.
Через 2 хвилини вимірюють оптичну густину розчину на електрофотоколориметрі так, як вказано при побудові градуювального графіка.
Обчислення результатів вимірювання
Обчислення результатів вимірювання масової частки заліза в азотній кислоті ω в мг/кг виконують за формулою:
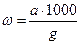 ,
,
де а – маса заліза, знайдена за градуювальним графіком, мг;
g – маса наважки, г;
1001– перерахунок г в кг.
Наприклад: 7.04.2012р.:
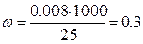 ,
,
2) Нітратна кислота. Залишок після прожарювання.
Метод вимірювання:
Вимірювання за цією методикою виконання вимірювання виконують опосередкованим методом, а саме гравіметричним методом, який заснований на зважуванні залишку, що одержано після прожарювання проби при температурі t=(820±20) º С.
Відбір проби:
Пробу азотної кислоти відбирають в місцях, які призначені для пробовідбору в чисту склянку з товстостінного скла з притертою пробкою. Перед відбором склянку обполіскують азотною кислотою, яку відбирають. На склянці роблять надпис з зазначенням назви проби, дати, часу та місця відбору.
Підготовка платинової чашки.
Нова платинова чашка або яка була у використанні, підлягає чистці. Для цього в чашці розплавляють 2-3 г піросульфату калію і кип’ятять в розбавленій хлористоводневій кислоті  (розчин з масовою часткою 18 %) 30 хв.
(розчин з масовою часткою 18 %) 30 хв.
Після цього чашку промивають дистильованою водою, висушують і прожарюють в електропечі до постійної маси.
Виконання вимірювання:
Наважку проби азотної кислоти масою (200, 00 ± 0, 02) г, зважують на вазі ВЛКТ-500 в платиновій чашці (кварцевій чаші), яка попередньо прожарена до постійної маси і зважена на вазі ВЛР-200. Обережно випарюють наважку проби на електроплитці насухо. Потім чашку ставлять у нагріту до температури t=(200±20) º С електропіч і поступово піднімають температуру печі. При досягненні температури t=(820±20) º С чашку витримують в печі 60 хв. Залишок після прожарювання охолоджують до температури навколишнього середовища і витримують в ексикаторі 40 хв. Після цього чашку (чашу) з залишком зважують на вазі ВЛР-200. Масу залишку після прожарювання визначають за різницею мас чашки (чаші) з залишком і порожньої чашки (чаші), результат зважування в грамах записують до п’ятого десяткового знаку.
Прожарювання виконують до постійної маси. Для контролю сталості маси залишку після прожарювання виконують повторне прожарювання чашки (чаші) з залишком протягом 30 хвилин з наступним його зважуванням.
Обчислення результатів вимірювання:
Обчислення результатів вимірювання масової частки залишку після прожарювання в азотній кислоті 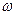 в відсотках виконують за формулою
в відсотках виконують за формулою
 ,
,
де m1 – маса порожньої чашки, г;
m2 – маса чашки з залишком після прожарювання, г;
m – маса наважки азотної кислоти, г;
100 – перерахунок у відсотки;
3)Нітратна кислота.Вміст нітратної кислоти.
Метод вимірювання:
Вимірювання за цією методикою виконання вимірювання виконують опосередкованим методом, а саме методом, який заснований на вимірюванні густини і температури проби азотної кислоти, що аналізують, з наступним визначенням масової частки за табличними даними.
Відбір проби:
Пробу азотної кислоти відбирають в місцях, які призначені для пробовідбору в чисту склянку з товстостінного скла з притертою пробкою. Перед відбором склянку обполіскують азотною кислотою, яку відбирають. На склянці роблять надпис з зазначенням назви проби, дати, часу та місця відбору.
Виконання вимірювання:
Пробу азотної кислоти, що аналізують, поміщають в чистий сухий циліндр, який поставлений на піддон, так, щоб рівень рідини не доходив до верхнього його краю на 3-4 см. Потім в циліндр обережно опускають чистий сухий ареометр з відповідним діапазоном вимірювання. Віддаль від нижнього кінця ареометра, який занурено в рідину, до дна циліндра, повинна бути не менше 3 см. Ареометр не випускають із рук до тих пір, поки він не стане плавати, не торкаючись стінок і дна циліндра. Проводять вимірювання густини згідно з поділкою шкали ареометра, яка відповідає нижньому краю меніска рідини. При вимірюванні око повинно бути на рівні нижнього краю меніска.
Одночасно проводять вимірювання температури. Вимірювання виконують при температурі від 20 оС до 27 оС.
Після проведення вимірювань виймають ареометр і термометр з циліндра, обмивають їх водою, витирають і зберігають в футлярах.
Обчислення результатів вимірювання:
Виміряне значення густини розчину азотної кислоти приводять до значення густини при температурі t = +20 оС за формулою (9.1):
 ,
,
де 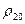 – густина розчину азотної кислоти при температурі +20 оС, г/см3;
– густина розчину азотної кислоти при температурі +20 оС, г/см3;
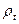 – густина розчину азотної кислоти при температурі в момент вимірювання, г/см3;
– густина розчину азотної кислоти при температурі в момент вимірювання, г/см3;
К – поправочний коефіцієнт для густини азотної кислоти (вказаний в таблиці 8.1), г ∙ см-3/оС;
t – температура азотної кислоти в момент вимірювання, оС.
Наприклад: 18.04.2012р.:
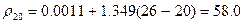 ,
,
4) Нітратна кислота. Вміст оксидів азоту.
Метод вимірювання:
Вимірювання за цією методикою виконання вимірювання виконують опосередкованим методом, а саме титриметричним методом, який заснований на взаємодії оксидів азоту з калієм марганцевокислим в кислому середовищі, при цьому відомий об’єм розчину калію марганцевокислого титрують розчином кислоти, що аналізують.
Вимоги безпеки, охорони довкілля:
При виконанні вимірювання масової частки оксидів азоту необхідно дотримуватись вимог згідно з правилами [1].
Нітратна кислота – за ступенем дії на організм людини належить до ІІІ класу небезпечних речовин, гранично допустима концентрація (ГДК) в повітрі робочої зони виробничих приміщень – 2 мг/м3 згідно з ГОСТ 12.1.005-88.
Чиста азотна кислота – безбарвна рідина з їдким запахом, змішується з водою в будь-яких співвідношеннях з виділенням тепла. Пара азотної кислоти в 2, 2 рази важча від повітря. Сильно димить на повітрі, виділяє оксид азоту (V), який утворює з повітрям сильний туман. Сильний окислювач. Солома, тирса і інші органічні матеріали, облиті кислотою, спалахують, при цьому виділяється оксид азоту (ІІ).
При безпосередньому контакті з шкірою азотна кислота викликає кислотний опік. Дим, який містить оксиди азоту (ІІ) і (V), подразнює дихальні шляхи, крім того може привести до руйнування зубів, кон’юктивітів і пошкодження рогівки очей. Кислотні опіки часто супроводжуються підвищенням температури, змінами в крові, зменшенням кількості сечі, що виділяється. Азотна кислота викликає небезпечні пошкодження очей, аж до омертвіння рогівки. При вдиханні пари слабке отруєння виражається в бронхіті, головній болі, шумі в вухах, сопливості. При середньому ступені отруєння можуть з’явитися початкові симптоми набряку легенів. Концентрована азотна кислота викликає важкі опіки; струп забарвлений в характерний жовтий колір. Розбавленні розчини азотної кислоти можуть бути причиною екземи.
Всі роботи з азотною кислотою повинні проводитись в витяжній шафі.
Засоби індивідуального захисту: фільтруючий протигаз марки В з фільтром для захисту від туману азотної кислоти або марки М з меншим часом захисту; захисні окуляри, рукавички гумові кислотнозахисні, чоботи резинові кислотостійкі, кислотнозахисний спецодяг.
Підготовка до виконання вимірювання
При підготовці до виконання вимірювання проводять наступні роботи:
Відбір проби:
Пробу азотної кислоти відбирають в місцях, які призначені для пробовідбору в чисту склянку з товстостінного скла з притертою пробкою. Перед відбором склянку обполіскують азотною кислотою, яку відбирають. На склянці роблять надпис з зазначенням назви проби, дати, часу та місця відбору.
Вимірювання густини проби:
Пробу азотної кислоти, що аналізують, поміщають в чистий сухий циліндр, який поставлений на піддон, так, щоб рівень рідини не доходив до верхнього його краю на 3-4 см. Потім в циліндр обережно опускають чистий сухий ареометр з відповідним діапазоном вимірювання густини. Віддаль від нижнього кінця ареометра, який занурено в рідину, до дна циліндра, повинна бути не менше 3 см. Ареометр не випускають із рук до тих пір, поки він не стане плавати, не торкаючись стінок і дна циліндра. Проводять вимірювання густини згідно з поділкою шкали ареометра, яка відповідає нижньому краю меніска рідини. При вимірюванні око повинно бути на рівні нижнього краю меніска.
Після проведення вимірювань виймають ареометр з циліндра, обмивають його водою, витирають і зберігають в футлярі.
Виконання вимірювання:
При виконанні вимірювання масової частки оксидів азоту виконують наступні операції:
В конічну колбу місткістю 250 см3 циліндром місткістю 50 см3 наливають дистильовану воду в об’ємі 50 см3 і піпеткою міскістю 10 см3 розчин сірчаної кислоти з масовою часткою 20 % в об’ємі 10 см3.
Потім додають по краплях розчин калію марганцевокислого з молярною концентрацією С(1/5КМnО4) = 0, 1 моль/дм3 з бюретки місткістю 25 см3 до блідо-рожевого середовища, після чого з цієї ж бюретки доливають ще розчин калію марганцевокислого в об’ємі 10 см3 і вміст колби нагрівають на електроплитці до температури t = 40 оС при постійному перемішуванні. В бюретку місткістю 25 см3 наливають азотну кислоту, що аналізують (маючи на увазі те, що проходить виділення оксидів азоту з кислоти, що аналізують, титрування необхідно проводити з бюретки з довгим відтягнутим кінцем, який доходить до поверхні титруючого розчину) і титрують розчин в колбі при безперервному перемішуванні до зникнення рожевого забарвлення.
Обчислення результатів вимірювання
Обчислення результатів вимірювання масової частки оксидів азоту в азотній кислоті 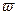 в відсотках виконують за формулою:
в відсотках виконують за формулою:
 ,
,
де 10 – об’єм розчину калію марганцевокислого з молярною концентрацією С(1/5КМnО4) = 0, 1 моль/дм3, см3;
К – поправочний коефіцієнт для приведення дійсної молярної концентрації розчину калію марганцевокислого до номінальної;
0, 004601 – маса оксидів азоту, яка відповідає 1 см3 розчину калію марганцевокислого з молярною концентрацією С(1/5КМnО4) = 0, 1 моль/дм3, г/см3;
V – об’єм азотної кислоти, що аналізують, який витрачено для титрування, см3;
 – густина азотної кислоти, г/см3;
– густина азотної кислоти, г/см3;
100 – перерахунок у відсотки.
Наприклад: 27.04.2012р.:
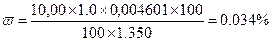 ,
,
5) Нітратна кислота. Вміст хлоридів.
Метод вимірювання:
Вимірювання за цією методикою виконання вимірювання виконують опосередкованим методом, а саме меркуриметричним методом, який заснований на взаємодії хлоридів з нітратом ртуті (ІІ) з утворенням малодисоційованих молекул хлориду ртуті (ІІ):
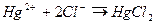
Надлишок катіонів ртуті Hg2+ взаємодіє з індикатором нітропрусидом натрію з утворенням білого нерозчинного осаду нітропрусиду ртуті:
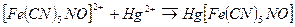
Для усунення взаємодії оксидів азоту з нітратом ртуті (ІІ) виконують попереднє їх окислення пероксидом водню:
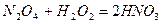
Підготовка до виконання вимірювання.
При підготовці до виконання вимірювання виконують наступні роботи:
Відбір проби:
Пробу для аналізу відбирають з пробовідбірної точки в місцях, призначених для пробовідбору, в термостійку склянку з притертою пробкою. Перед відбором проби пробовідбірний посуд попередньо миють, а потім обполіскують пробою азотної кислоти, яку відбирають. На пробовідбірному посуді роблять надпис із зазначенням назви проби, місця, дати та часу відбору проби.
Об’єм проби від 300 см3 до 500 см3.
Виконання вимірювання:
В конічну колбу місткістю 250 см3 піпеткою відповідної місткості вносять аліквотну частину проби в об’ємі 10 см3 або 25 см3 (в залежності від масової концентрації хлоридів в азотній кислоті). Циліндром місткістю 50 см3 додають дистильовану воду в об’ємі від 30 см3 до 40 см3 (в разі необхідності із крапельниці по краплях додають розчин пероксиду водню до знебарвлення середовища) потім із крапельниці додають чотири краплі розчину нітропрусиду натрію, ретельно перемішують вміст колби і титрують його з бюретки місткістю 1 см3 розчи-ном азотнокислої ртуті з молярною концентрацією 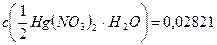 моль/дм3 до появи слабкої муті, яка не зникає при перемішуванні.
моль/дм3 до появи слабкої муті, яка не зникає при перемішуванні.
Обчислення результатів вимірювання масової концентрації хлоридів в азотній кислоті ρ в мг/дм3 виконують за формулою (9.1):
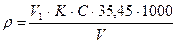 ,
,
де V1 – об’єм розчину нітрату ртуті (ІІ), який витрачено для титрування, см3;
К – поправочний коефіцієнт для приведення дійсної молярної концентрації розчину нітрату ртуті (ІІ) до номінальної;
С – номінальна молярна концентрація розчину нітрату ртуті 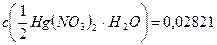 моль/дм3
моль/дм3
V – об’єм проби, взятий для аналізу, см3;
1002– перерахунок г в мг.
Наприклад: 14.04.2012р.: 
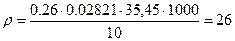
3)Описання приладу КФК-3
|
|