
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Хід роботи. Зберіть прилад для одержання амоніаку, як показано на малюнку 1.
|
|
Зберіть прилад для одержання амоніаку, як показано на малюнку 1.
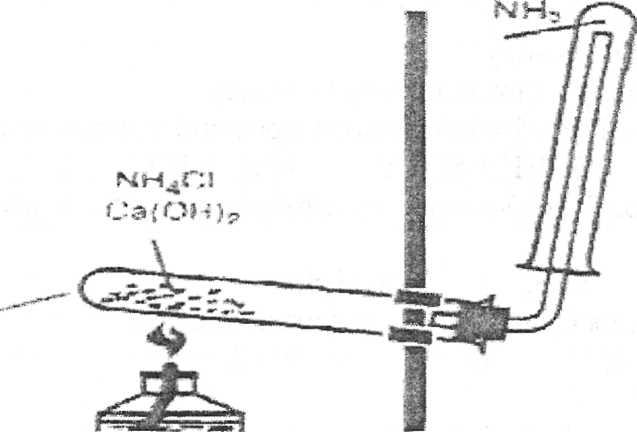
Малюнок 1
Дослід I. Добування амоніаку.
Приготуйте суміш з рівних об'ємів амоній хлориду і порошку кальцій гідроксиду. Розмішайте суміш у фарфоровій ступці.
Приготовану суміш всипте в пробірку 1 на 1/3 її місткості, закрийте її газовідвідною трубкою та закріпіть, як показано на мал. 1. Обережно прогрійте спочатку всю пробірку, а потім лише те місце, де знаходиться суміш. Для виявлення наявності амоніаку в пробірці 2 піднесіть до її отвору вологий фенолфталеїновий папір. Нагрівання припиніть, коли пробірка 2 заповниться амоніаком.
Спостереження _________________________________________________________
Рівняння хімічних реакцій запишіть у молекулярній, повній і скороченій йонній формах: ______________________________________________________________________
Дослід II. Збирання амоніаку та розчинення його у воді.
Пробірку 2, в якій знаходиться амоніак, не перевертаючи, закрийте пробкою та занурте її в кристалізатор з водою.
Дослід III. Дія розчину амоніаку на індикатори.
Вміст пробірки 2 розділіть на чотири рівні частини. Визначте реакцію середовища розчину у першій пробірці за допомогою лакмусу, у другій - фенолфталеїну, у третій - метилового оранжевого, а в четвертій - універсальним індикатором.
| Фенолфталеїн | Метиловий-оранжевий | Лакмус | Універсальний індикатор |
Дослід IV. Взаємодія амоніаку з кислотами.
Піднесіть до отвору пробірки з амоніаком по черзі скляні палички, змочені розчинами концентрованих хлоридної, сульфатної і нітратної кислот.
| Хлоридна кислота | Сульфатна кислота | Нітратна кислота |
Рівняння хімічних реакцій амоніаку з кислотами запишіть у молекулярній,
повній і скороченій йонній формах: ______________________________________________
Висновок:
Таким чином, у лабораторних умовах амоніак можна одержати __________________
Амоніак збирають у_____________________ пробірку, перевернуту догори дном, оскільки _____
Під час розчинення добутого газу у воді утворюється речовина __________________
Під час дії розчину амоніаку на індикатори спостерігається _____________________
що свідчить про _______________________________________________________________
Під час взаємодії амоніаку з кислотами спостерігається _________________________
що пояснюється _______________________________________________________________
Тести
1. У лабораторних умовах амоніак одержують:
а) розкладанням амоній хлориду;
б) при взаємодії азоту з воднем;
в) при взаємодії амоній хлориду з кальцій гідроксидом.
2. Амоніак збирають способом:
а) витісненням повітря;
б) витісненням води;
в) витісненням азоту.
3. При розчиненні амоніаку у воді утворюється середовище:
а) нейтральне; б) кисле; в) лужне.
4. Які гази можна збирати у пробірку, перевернуту вверх дном:
а) CO2; б) Н2; в) O2.
5. Виходячи зі ступеня окислення Нітрогену з амоніаку, поясніть, які
властивості виявляє амоніак у реакціях зі зміною ступеня окислення Нітрогену:
а) тільки окисні; б) тільки відновні; в) окисні й відновні.
6. При взаємодії з кислотами амоніак вступає в реакції:
а) обміну; б) заміщення; в) сполучення; г) розкладу.
7. Структурною формулою амоніаку є:
а).NH3; б) Н-N-Н; в) Н: N: Н
׀ ∙ ׀ ∙
Н Н
8. Який тип хімічного зв'язку в молекулі амоніаку:
а) йонний; б) ковалентний полярний; в) ковалентний неполярний.
9. Вкажіть сіль амоній сульфату:
а)(NН4)2SO4; б) (NH4)2S; в)(NH4)2SO3.
10. Напишіть рівняння реакцій за даним схемами:
а) NH3 + O2 =
б) NH3 + Н2SO4 =
Яка з них є окисно-відновна? Відповідь мотивуйте.
|
|