
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Классификация хроматографических методов
|
|
В основе хроматографического разделения лежат различные механизмы, как правило, дополняющие друг друга.
По доминирующему механизму могут быть выделены следующие виды хроматографии:
1) адсорбционная (в основе лежит явление адсорбции);
2) распределительная (основана на различии коэффициентов распределения вещества между двумя несмешивающимися жидкостями);
3) ионообменная (основана на различии констант ионного обмена разделяемых ионов между раствором и ионитом);
4) ситовая (основана на различии размеров молекул; используется в основном для разделения белков и других высокомолекулярных соединений на фракции);
5) хемосорбционная; в зависимости от типа химической реакции выделяют: а) осадочную; б) редокс-хроматографию; в) лигандообменную (аффинную); г) биоспецифическую.
По цели проведения различают следующие виды хроматографии:
- аналитическая хроматография используется для качественного и количественного анализа смеси веществ;
- препаративная хроматография предназначена для выделения из смеси чистых компонентов или для очистки вещества от примесей.
По характеру подвижной и неподвижной фаз основные разновидности хроматографии приведены в таблице 2.
Таблица 2
Разновидности хроматографии
| Подвижная фаза (элюент) | Неподвижная фаза | Название хроматографического метода | Аппаратурное оформление |
| Газ | Жидкость | Газо-жидкостная | Колоночная |
| Твердый адсорбент | Газо-адсорбционная | Колоночная | |
| Жидкость | Жидкость | Жидкостно-жидкостная (распределительная) | Бумажная Тонкослойная Колоночная |
| Твердый адсорбент | Жидкостно-адсорбционная | Тонкослойная Колоночная | |
| Ионообменная смола | Ионообменная | Колоночная | |
| Гели, молекулярные сита | Гель-фильтрация, ситовая | Колоночная |
По технике эксперимента хроматография может быть колоночной (разновидность – капиллярная хроматография) и плоскостной (тонкослойной и бумажной).
В газовой хроматографии подвижной фазой является газ, а неподвижной фазой – твердый адсорбент или нелетучая жидкость, нанесенная на твердый носитель. Неподвижная фаза находится в колонке. В случае капиллярной колонки роль неподвижной фазы выполняют ее стенки. Газовую хроматографию применяют для разделения летучих термически устойчивых веществ с молекулярной массой до 500. Она имеет огромное значение как для качественного, так и количественного анализа и благодаря высокой чувствительности позволяет обнаруживать микрограммовые количества соединений (до 10-6 г).
Для проведения газовой хроматографии используют хроматограф (рис. 18). Анализируемая смесь вводится в испаритель, и оттуда с помощью газа-носителя попадает в колонку с неподвижной фазой, помещенную в термостат. Различные компоненты смеси перемещаются газом-носителем вдоль колонки с разными скоростями из-за разного сродства их к неподвижной фазе. Поэтому разделяемые вещества выходят из колонки в разное время и по отдельности регистрируются детектором, который передает сигнал самописцу. В результате получается хроматограмма, представляющая собой несколько пиков, число которых зависит от числа присутствующих в смеси веществ, а площадь каждого пика пропорциональна содержанию соответствующего вещества.
Анализируемая
смесь
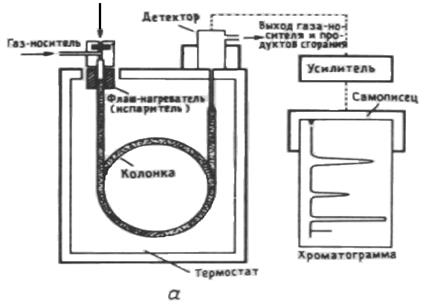
Рис. 18. Газо-жидкостная хроматография
На рис. 19. показана хроматограмма трехкомпонентной смеси.
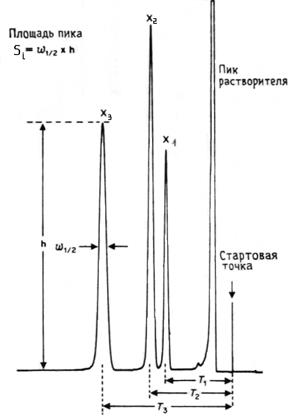
время удерживания
Рис. 19. Хроматограмма трехкомпонентной смеси, полученная на газовом хроматографе.
Идентификация веществ (Х1; Х2; Х3) проводится по времени удерживания (соответственно Т1; Т2 и Т3), которое сравнивают со временем удерживания эталона при его хроматографировании на данной колонке при аналогичных условиях. Определение количественного состава смеси выполняют, анализируя площадь полученных пиков для всех веществ, а относительное содержание каждого компонента равно отношению площади пика этого компонента Si к сумме площадей пиков всех компонентов смеси: ci=Si/SSi.
В жидкостной хроматографии (табл. 2) подвижной фазой служит жидкость, а неподвижной фазой является твердый адсорбент или тонкий слой жидкости, нанесенной на твердый носитель или содержащийся в нем.
В тонкослойной хроматографии (ТСХ) в качестве твердой фазы используют силикагель (n SiO2 * m H2O), оксид алюминия (Al2O3), целлюлозу или другие полимеры, нанесенные тонким слоем на пластинки из стекла, иногда пластмассы или толстой алюминиевой фольги.
Чтобы нанести на хроматографическую пластинку исследуемый продукт, его растворяют и полученный раствор набирают в капиллярную трубку. Осторожным прикосновением капиллярной трубки к сорбенту раствор наносят на хроматографическую пластинку. На одну пластинку можно нанести несколько проб при условии, что расстояние между ними будет не менее 2 см. Содержание веществ в пробе должно быть в пределах от 0, 5 до 50 мкг. Место нанесения проб в зависимости от размера пластинки должно быть на расстоянии 1 см от нижнего края на больших (5х20 см) пластинках и около 5 мм – на маленьких.
После нанесения на слой сорбента исследуемого вещества или смеси веществ пластинку помещают в камеру с элюентом, причем стартовая линия не должна соприкасаться с элюентом, после чего камеру герметично закрывают (рис.20).
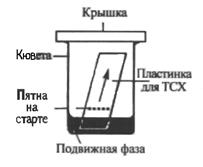
Рис. 20. Тонкослойная хроматография
Выбор элюента определяется природой хроматографируемого вещества и характером сорбента. По увеличению элюирующей способности растворители могут быть расположены в следующий ряд: н-гексан; гептан; циклогексан; четыреххлористый углерод; бензол; хлороформ; диэтиловый эфир; этилацетат; пиридин; ацетон; этанол; метанол; вода.
Если вещество обладает слабым сродством к сорбентам, то в этом случае используют наиболее активный сорбент и наиболее слабый элюент. При хроматографировании хорошо адсорбирующихся веществ применяются мало активные сорбенты и сильные элюенты. Классы органических соединений по увеличению их способности к адсорбции могут быть расположены в следующий ряд: алканы; алкены; алкадиены; ароматические углеводороды; простые эфиры; сложные эфиры; кетоны; амины; амиды; спирты одноатомные; спирты двухатомные; кислоты.
Вместе с подвижной фазой по неподвижной фазе перемещаются нанесенные вещества, причем с разной скоростью, зависящей от их сорбционных свойств. Когда фронт подвижной фазы поднимется к верхнему краю пластинки, ее вынимают из камеры, отмечают положение фронта растворителя и высушивают. Если анализируемые вещества не окрашены, то хроматограмму проявляют. С этой целью хроматограммы опрыскивают растворами реагентов, образующих с исследуемыми веществами окрашенные продукты. Для этой цели может быть использована концентрированная серная кислота, под влиянием которой на хроматограмме в местах нахождения органических веществ образуются темные пятна.
Если исследуемое вещество поглощает в УФ-области, то для приготовления хроматографических пластинок используют адсорбент, содержащий флуоресцирующее вещество. Хроматограммы, полученные на таких пластинках, рассматривают в УФ-свете.
Для идентификации веществ используются соответствующие соединения – свидетели, а также значение фактора относительного удерживания (Rf), представляющего собой отношение расстояния, пройденного веществом от линии старта к расстоянию, пройденному подвижной фазой от линии старта до линии фронта (рис.21):
Rf(x)=h(x)/h(F)
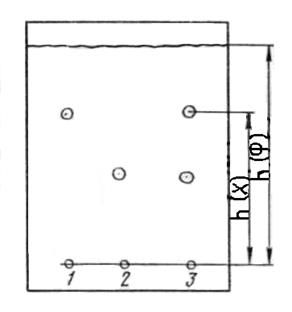
фронт подвижной фазы
h(x) – расстояние от линии старта до центра пятна вещества
линия старта
Рис. 21. Схема распределения смеси веществ на пластинке с тонким слоем сорбента: 1, 2, - индивидуальные вещества; 3 – смеси вещества 1 и 2
Поскольку значение Rf значительной степени зависит от качества сорбента, чистоты растворителя, температуры, насыщенности камеры и других факторов, для большей достоверности результата анализа применяют «свидетели» - стандартные растворы аналогичных веществ смеси, которые наносят на линию старта пластинки параллельно с пробой анализируемой смеси веществ. При одинаковом значении Rf исследуемых веществ смеси и «свидетелей» идентификация считается положительной.
Применяя «свидетели» (известной концентрации), можно визуально сравнивать интенсивность окраски пятен веществ исследуемой смеси с интенсивностью окраски пятен «свидетелей» и таким образом ориентировочно судить о количественном содержании ингредиентов анализируемой смеси.
Наряду с тонкослойной хроматографией широко используется бумажная хроматография, которая по технике исполнения близка к ТСХ. В бумажной хроматографии неподвижной фазой является вода, входящая в состав бумаги или органическая жидкость, которой бумага пропитана. Для бумажной хроматографии используют специальные сорта фильтровальной бумаги.
Колоночная хроматография широко используется для количественного разделения смесей. Хроматографическая колонка представляет собой стеклянную трубку, снабженную на выходе краном (рис.22а). В верхнюю часть колонки с сорбентом вносят анализируемую смесь и через слой сорбента медленно пропускают подвижную фазу. Этот процесс называют элюированием. Из-за разных сорбционных свойств каждый компонент смеси имеет свое время удерживания, т.е. время прохождения через колонку. Последовательные порции элюата собирают в отдельные емкости, испаряют подвижную фазу, и получается чистый компонент (рис.22б, в).
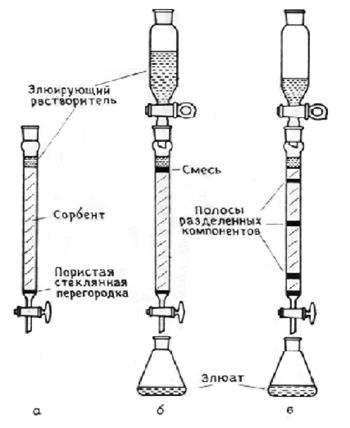
Рис. 22. Колоночная хроматография
|
|