
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Обработка экспериментальных данных
|
|
4.1. По уравнению Клапейрона-Менделеева секундный массовый расход рассчитывается по уравнению состояния идеального газа
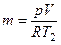 .
.
4.2. Средняя массовая теплоемкость при р = const и v = const определяется по формуле:
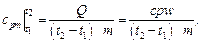 Дж /(кг · К);
Дж /(кг · К);
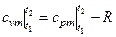 .
.
4.3. Средняя объемная теплоемкость для этого же интервала температур:
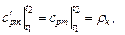 кДж /(м3 · К),
кДж /(м3 · К),
где плотность при нормальных физических условиях (t н = 0 °C, р н = 0, 1013 МПа)
 .
.
Для воздуха 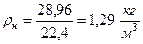 .
.
Контрольные вопросы
1. Дайте определение понятию “теплоёмкость тела в данном процессе”.
2. Что называется средней и истинной теплоёмкостью газов? Объяснить с помощью ct - диаграммы.
3. Представить вывод соотношений для определения теплоёмкости cр, cv,  ,
, 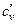 , cрт, cvт,
, cрт, cvт, 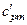 ,
, 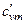 , μ cp, μ cv. Указать связь между ними.
, μ cp, μ cv. Указать связь между ними.
4. Чем отличаются теплоёмкости идеальных и реальных газов? В каких случаях можно принимать теплоёмкость газов величиной постоянной и не зависящей от внешних условий (давления и температуры).
5. Записать выражение для линейной и нелинейной зависимости теплоёмкости от температуры. Объяснить смысл коэффициентов а, b, с.
6. Изложите методику экспериментального определения теплоёмкости методом проточного калориметра.
7. Как определить среднюю теплоёмкость в интервале от t 1 до t 2 пользуясь таблицами теплоёмкостей от 0 °C до t °C?
8. В чём разница практического определения теплоёмкости газа по формулам истинной и средней теплоёмкости в пределах изменения температуры от t 1 до t 2?
9. Рассчитать теплоёмкости cр, cv,  ,
, 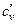 , μ cp, μ cv, k, R для азота.
, μ cp, μ cv, k, R для азота.
10. Написать уравнение для расчёта количества теплоты, выраженное через среднюю теплоёмкость. Представить и объяснить диаграмму сt.
11. Какие преимущества и недостатки молекулярно-кинетической теории.
12. Почему теплоёмкость газа уменьшается при увеличении молекулярной массы? Как это объяснить физически?
13. Объясните физическую причину зависимости теплоемкости реальных газов от давления и температуры?
14. Почему теплоёмкость при р = const больше, чем в процессе v = const. Какими уравнениями связаны между собой эти теплоёмкости?
15. Как определить объемную и массовую теплоёмкости газов по его мольной теплоёмкости?
16. Покажите на примере зависимость теплоёмкости газа от особенностей термодинамического процесса?
17. Используя I закон термодинамики представьте вывод уравнения Майера для массовой и мольной теплоёмкости.
18. Почему мольная теплоёмкость газа μ cp, μ cv изменяется с увеличением атомности газа? Какова их величина?
19. Почему разность мольных теплоемкостей μ cp, μ cv для всех газов и смесей величина постоянная, а разность массовых теплоемкостей cp - cv зависит от рода газа?
20. В каких пределах может измениться величина теплоёмкости газа и какой фактор наиболее существенно на неё влияет?
21. Рассчитать теплоёмкости cр, cv,  ,
, 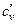 , μ cp, μ cv для CH 4.
, μ cp, μ cv для CH 4.
22. Определите теплоёмкости ср и сv для воздуха при t = 200 °С и t = 1200 °C.
23. Как определяется ср см, cv см, Rсм “k”| для газовой смеси.
24. В чем преимущества квантовой теории теплоёмкости? Как в соответствии с этой теорией определить μ cp, μ cv, μ R.
СОДЕРЖАНИЕ
| Теоретическое введение | ||
| 1.1 | Истинная и средняя теплоемкость | |
| 1.2 | Связь между массовой с, объемной с´ и мольной μ с теплоемкостями | |
| 1.3 | Элементы молекулярно-кинетической (МКТ) и квантовой теории теплоемкости | |
| 1.3.1 | Молекулярно-кинетическая теория | |
| 1.4 | Показатель адиабаты и его зависимость от температуры | |
| 1.5 | Теплоемкость газовых смесей | |
| 1.6 | Элементы квантовой теории теплоемкости | |
| Лабораторная установка | ||
| Порядок проведения работы | ||
| Обработка экспериментальных данных | ||
| Контрольные вопросы |
|
|