
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Протромбиновый тест (ПТ) по Квику
|
|
Методика выполнения ПТ-теста была предложена Квиком (Quick AJ. и соавт.) в 1935 г. и состоит в определении времени свертывания цитратнои плазмы после добавления тромбопластина и Са2+.
В тесте протромбиновое время по Квику для перевода времени свертывания в % факторов протромбинового комплекса строится калибровочный график с использованием разведений стандартной плазмы. График имеет форму логарифмической зависимости. Для вычислений вручную можно использовать линелизацию графика (рис. 99) в координатах «1/% протромбина» (т. е. 100% —0, 01; 75% - 0, 0133; 50% - 0, 02; 25% - 0, 04; дальнейшее разведение нежелательно, так как возможно отклонение калибровки из-за значительного снижения концентрации фибриногена). Недостатком этого метода калибровки ПВ является то, что разведе-

ние плазмы моделирует только снижение концентрации факторов, которое может наблюдаться, например, при нарушении синтеза белков в печени или развитии коагулопатии потребления. При дефиците витамина К или приеме его антагонистов (непрямых антикоагулянтов) концентрация факторов может быть близкой к норме, но их функциональные свойства существенно изменены. Поэтому ПВ по Квику рекомендуется использовать при постановке коагулограммы для выявления механизмов нарушения свертывания крови.
Наклон калибровочной кривой может зависеть от того, какой буфер или физиологический раствор были использованы для разведений. Разведенная плазма нестабильна, поэтому растворы разведенной контрольной плазмы хранить не рекомендуется, необходимо использовать столько исходной плазмы, сколько требуется для серии разведений и не больше.
При очевидной простоте выполнения самого теста оценка его результатов представляет собой серьезную проблему, которая окончательно не решена до настоящего времени. Две основные причины обуславливают сложность проблемы. Во-первых, в тесте активируется ряд последовательных и взаимовлияющих реакций, и суммарная скорость зависит от многих параметров (рис. 100). Во-вторых, время свертывания нормальной и, что исключительно важно, патологической плазмы значительно варьирует в зависимости от источника и метода получения тромбопластина.
Рис. 99. Линелизация калибровочного графика протромбиновое время по Квику в координатах «1/% протромбина» - время
Рис. 100. Последовательные и взаимовлияющие реакции, определяющие суммарную активность протромбинового теста (ПТ)
Обеспечение диагностики нарушений гемостаза в КДЛ
Протромбиновое время, выраженное через международное нормализованное отношение (MHO)
Современные коагулометры программируются на вычисление MHO. Стандартизованный протромбиновый тест был разработан Международным комитетом по стандартизации в гематологии и Международным комитетом по тромбозу и гемостазу и принят ВОЗ в 1983 г. В его основе лежит наличие линейной зависимости между логарифмами протромбинового времени, определенными с разными тромбопластинами. На практике это означает, что значения ПО, определенные с использованием разных тромбопластинов, могут быть приведены путем возведения в степень, представляющую собой МИЧ используемого тромбопластина, к величине, которая была бы получена при определении факторов протромбинового комплекса с первичным стандартом тромбопластина. Эту величину было предложено называть MHO - международным нормализованным отношением (INR - английская аббревиатура). По рекомендации ВОЗ определение МИЧ (ISI - английская аббревиатура) является обязанностью производителей тромбопластина, которые должны определять относительную чувствительность каждой серии выпускаемых ими тромбопластинов, сравнивая ее с эталоном тромбопластина, чувствительность которого принята за единицу.
MHO рассчитывают по формуле:

Контроль за лечением непрямыми антикоагулянтами
При приеме непрямых антикоагулянтов меняются как внешний, так и внутренний пути активации протромбиназы, однако эффект непрямых антикоагулянтов в большей степени сказывается на внешнем каскаде, и соответственно больше меняется ПВ, чем АЧТВ.
При терапии непрямыми антикоагулянтами использование MHO позволяет оценивать степень гипокоагуляции независимо от используемого тромбопластина, сравнивать результаты, полученные разными лабораториями. Для конт-
роля за терапией непрямыми антикоагулянтами рекомендуется использовать тромбопластины со значениями МИЧ ниже 2 (лучше 1, 0-1, 2).
Ограничения использования MHO
Имеются достаточно значительные ограничения в использовании MHO в лабораторной практике:
• MHO не может использоваться на начальном
этапе лечения непрямыми антикоагулянтами,
так как существующие различия между раз
ными тромбопластинами вносят слишком
большие флуктуации на этом этапе, которые
не могут быть компенсированы производи
телями реагентов.
• MHO не используется для контроля и мони
торинга состояния внешнего каскада актива
ции протромбиназы в общей популяции па
циентов, не принимающих непрямых антико
агулянтов. В этом случае нужно использовать
ПТ, различия в определении которого сохра
няются между разными лабораториями.
Комментарии по поводу разных способов
выражения ПТ-теста представлены в табл. 21.
Интерпретация результатов
ПВ удлинено (ПИ снижен, ПО и MHO повышены) - врожденный дефицит факторов II, V, VII, X, хронические заболевания печени с нарушением функции, дефицит витамина К (холес-таз, мальабсорбция, дисбактериоз), лечение антикоагулянтами непрямого действия, гипофиб-риногенемия (менее 0, 5 г/л), дисфибриногенемия и нарушение полимеризации фибрина, ДВС-син-дром, присутствие ингибиторов свертывания (гепарин, ПДФ).
ПВ укорочено (ПИ увеличен, ПО и MHO снижены) - состояние гиперкоагуляции, массивное поступление тканевого тромбопластина в кровоток (травма, некроз), повышенная свертываемость во время беременности и после родов.
Выявление дефицита факторов
с использованием принципа заменных проб
в тесте ПВ
Клоттинговый метод определения активности ф.VII основан на использовании заменных
Обеспечение диагностики нарушений гемостаза в КДЛ
Таблица 21
Способы выражения протромбинового теста

|
проб с плазмой, лишенной ф.УП. Метод аналогичен определению активности других факторов
в тесте АЧТВ, однако при анализе активности ф.VII используется тест ПВ.
Тромбиновое время
Тромбиновое время (ТВ) - скрининговый тест на полимеризацию фибриногена/фибрина и на ан-тикоагулянтную активность в плазме. ТВ регистрируется по свертыванию плазмы при добавлении к ней низкой или средней концентрации тромбина (бычьего или человеческого). ТВ определяется в основном количеством и качеством фибриногена и присутствием антикоагулянтов в плазме. Если в плазме присутствует гепарин, то комплекс гепарин-антитромбин быстро нейтрализует добавленный тромбин и ТВ будет удлиняться. Среди скрининговых тестов ТВ - наиболее чувствительный тест на присутствие гепарина. В то же время известно, что чувствительность к гепарину у ТВ зависит от рН, ионной силы тест-системы, свойств тромбина (происхождение и степень очистки), т. е. в значительной степени определяется составом набора реагентов.
Увеличение ТВ происходит также в присутствии относительно высокой концентрации про-
дуктов деградации фибрина (ПДФ), наблюдаемой при назначении тромболитической терапии, при ДВС-синдроме, заболеваниях печени и при дисфибриногенемиях. Результат определяется не только общим количеством ПДФ, но и их составом. Непрямые антикоагулянты не влияют на результаты теста.
Иногда удлинение ТВ наблюдается в присутствии аутоантител к тромбину или парапротеинов при миеломной болезни, которые препятствуют полимеризации мономеров фибрина. Ингибиторами полимеризации фибрин-мономеров могут быть IgG или IgM, которые удлиняют как ТВ, так и реп-тилазное время. Аутотела к тромбину подавляют только ТВ и не влияют на рептилазное время.
К увеличению ТВ приводят: • снижение концентрации фибриногена менее
0, 5 г/л (врожденная или приобретенная гипо/
афибриногенемия);
Обеспечение диагностики нарушений гемостаза в КДЛ
• качественные изменения молекулы фибрино
гена (дисфибриногенемия);
• присутствие физиологических (гепарин) и
патологических (ПДФ, моноклональные бел
ки) ингибиторов тромбина и фибринообра-
зования;
• наличие парапротеинемии, уремии, в некото
рых случаях волчаночных антикоагулянтов.
Пределы нормальных значений ТВ зависят от
условий постановки метода и должны определяться в каждой лаборатории самостоятельно. Тест не стандартизован, в разных лабораториях могут ис-
пользоваться разные концентрации тромбина. Тест может выполняться в модификациях, в частности после нейтрализации гепарина протамин-сульфатом. Тест практически не пригоден для мониторинга за лечением гепарином или гирудином, так как результаты зависят от состояния системы фибриноген-фибрин, кроме того, ТВ характеризуется очень малым временным интервалом. Результаты во многом зависят от того, на каком ко-агулометре проводилось исследование - механическом или оптическом, но в любом исполнении характеризуются низкой воспроизводимостью.
Рептилазное время (батроксобиновое время)
Батроксобин (или рептилаза) - тромбинопо-добная протеаза из яда щитомордника обыкновенного, которая способна вызывать переход фибриногена в фибрин. Рептилаза отщепляет от фибриногена только фибринопептид А, что отличает ее от действия тромбина, который, кроме фибрино-пептида А, отщепляет от фибриногена еще и фибринопептид В (рис. 101) и активирует факторы V, VIII, XIII. Рептилаза не подавляется антитромбином, поэтому этот тест может использоваться для оценки полимеризации мономеров фибрина в присутствии гепарина. Рептилазное время часто определяют одновременно с ТВ (табл. 22).
Таблица 22
Тромбиновое и рептилазное время при различных состояниях
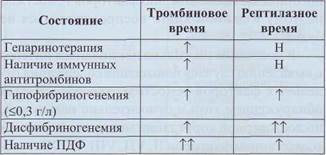
Нормальные значения рептилазного времени устанавливаются в каждой лаборатории, так как показатель зависит от реагентной и приборной
базы. Рептилазное время удлиняется при афибри-ногенемии и при некоторых формах дисфибри-ногенемии, часто не параллельно ТВ и в присутствии относительно высоких концентраций ПДФ (при гиперфибринолизе).
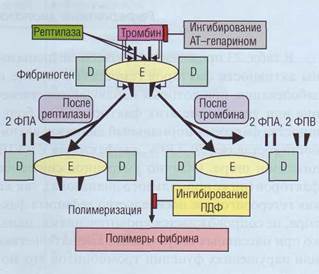
Рис. 101. Принцип и влияние факторов при постановке тестов тромбиновое время (ТВ) и рептилазное время.
Тромбин оказывает комплексный эффект, рептилаза отщепляет от фибриногена только фибринопептид А (ФПА), На ТВ активно влияет АТ-гепарин, на рептилазное время гепарин не влияет, ПДФ за счет ингибирования полимеризации фибрин-мономеров удлиняют как ТВ, так и рептилазное время
Обеспечение диагностики нарушений гемостаза в КДЛ
Отдельные факторы гемостаза
 В случае обнаружения патологических изменений АЧТВ и/или ПВ необходимо проводить дополнительные исследования с целью выяснения причины этих отклонений. Несмотря на то что за последнее время для определения отдельных факторов гемостаза были разработаны методы с использованием хромогенных субстратов (амидолитические методы), многие лаборатории продолжают пользоваться коагуляционными технологиями с использованием контрольных плазм, обедненных по определенному фактору. Дефицитные плазмы получают: 1) путем имму-носорбции отдельных факторов с добавлением других факторов, 2) от доноров, больных гемофилией с недостаточностью одного из факторов свертывания. Важнейшими качественными критериями наборов с дефицитной плазмой являются очень низкий или неопределяемый уровень од-
В случае обнаружения патологических изменений АЧТВ и/или ПВ необходимо проводить дополнительные исследования с целью выяснения причины этих отклонений. Несмотря на то что за последнее время для определения отдельных факторов гемостаза были разработаны методы с использованием хромогенных субстратов (амидолитические методы), многие лаборатории продолжают пользоваться коагуляционными технологиями с использованием контрольных плазм, обедненных по определенному фактору. Дефицитные плазмы получают: 1) путем имму-носорбции отдельных факторов с добавлением других факторов, 2) от доноров, больных гемофилией с недостаточностью одного из факторов свертывания. Важнейшими качественными критериями наборов с дефицитной плазмой являются очень низкий или неопределяемый уровень од-
ного фактора, высокий уровень других факторов, наличие в наборе калибраторов с дробным содержанием фактора, чтобы можно было построить калибровочную кривую как в зоне с нормальным, так и патологическим содержанием фактора. Для получения калибровочной кривой возможно разведение калибраторов. Ведущие мировые производители выпускают калибраторы, тестированные относительно стандартов ВОЗ (там, где они имеются). Следует подчеркнуть, что далеко не любая комбинация дефицитной плазмы и тест-наборов на ПВ или АЧТВ дают схожие результаты, поэтому следует пользоваться рекомендациями фирм-производителей дефицитных плазм и тест-наборов. Качество дефицитной плазмы и чувствительность реагентов имеют существенное значение в определении дефицита факторов в клинике.
Референтные диапазоны содержания факторов
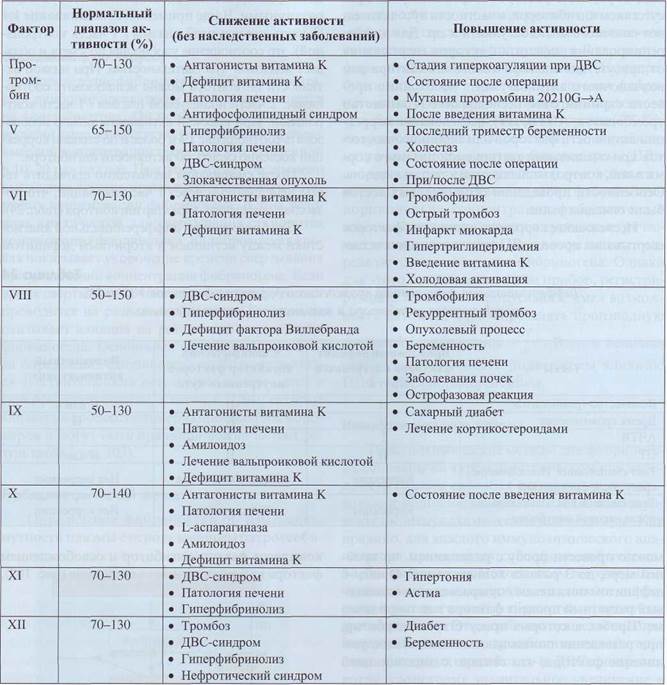
В табл. 23 приведены референтные диапазоны активности факторов гемостаза в плазме и заболевания, при которых наблюдаются снижение или увеличение этих факторов. Для большинства факторов нормальный диапазон активности составляет 70-130%, для факторов V и VIII диапазон шире. Обычно умеренное снижение факторов (ниже нормального диапазона), так же как гетерозиготное носительство дефицита фактора, не сопровождается кровотечениями, однако при массивных оперативных вмешательствах или нарушениях функции тромбоцитов это может быть решающим моментом развития геморрагического синдрома. Количественная характеристика факторов является значимой для диагностики гемофилии и лечения с использованием гемоконцентратов. Содержание факторов свертывания крови важно знать перед операцией у больных с заболеваниями печени, злокачественными опухолями, сепсисом, нефротическим синдромом, у пациентов, принимающих антикоагулянты непрямого действия, так как оператив-
ное вмешательство, особенно обширное, в этих случаях может привести к дополнительному потреблению проблемных факторов и развитию кровотечения. Технологией с использованием дефицитных плазм определяются все факторы, за исключением фибриногена и фактора XIII. Эта технология представлена в многочисленных пособиях по исследованию факторов гемостаза, поэтому в данной книге воспроизводиться не будет.
В последние несколько лет появился интерес к выявлению случаев повышения содержания отдельных факторов гемостаза, что объясняется обнаружением хотя и относительно невысокой, но достоверной корреляции между повышенным содержанием факторов II, VII, VIII, IX, XI и увеличенным риском тромбозов. Повышение активности факторов может быть зарегистрировано коагуляционными методами с применением технологии значительного разведения плазмы или методами с использованием хромогенных субстратов.
Обеспечение диагностики нарушений гемостаза в КДЛ
Таблица 23
Диапазоны активности факторов гемостаза в плазме и клинико-диагностическое значение
изменения активности факторов
|
Обеспечение диагностики нарушений гемостаза в КДЛ
Принцип дифференцирования истинного дефицита факторов и действия ингибиторов
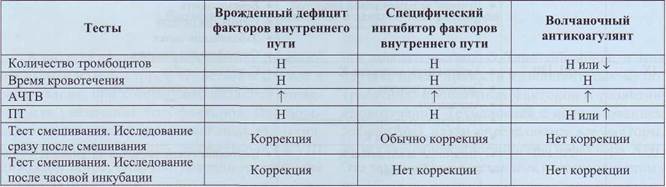
 Удлинение АЧТВ и/или ПВ может быть вызвано дефицитом факторов свертывания или присутствием ингибиторов, в частности аутоантител, волчаночного антикоагулянта и др. Для дифференцирования дефицита факторов свертывания от присутствия специфического ингибитора или волчаночного антикоагулянта необходимо провести скрининговое исследование (количество тромбоцитов, АЧТВ, ПТ), исследование коррекции активности факторов или скрининговых тестов при смешивании тестируемой плазмы с нормальной, контрольной плазмой и тест разведения. Особенности проведения скрининговых тестов были описаны выше.
Удлинение АЧТВ и/или ПВ может быть вызвано дефицитом факторов свертывания или присутствием ингибиторов, в частности аутоантител, волчаночного антикоагулянта и др. Для дифференцирования дефицита факторов свертывания от присутствия специфического ингибитора или волчаночного антикоагулянта необходимо провести скрининговое исследование (количество тромбоцитов, АЧТВ, ПТ), исследование коррекции активности факторов или скрининговых тестов при смешивании тестируемой плазмы с нормальной, контрольной плазмой и тест разведения. Особенности проведения скрининговых тестов были описаны выше.
Исследование коррекции активности факторов свертывания проводится путем смешивания иссле-
дуемой плазмы с контрольной нормальной плазмой. Соотношения компонентов могут быть различными. Чаще применяется смешивание 1: 1 (1 часть исследуемой плазмы / 1 часть контрольной), это соотношение удобно для подсчета и обладает неплохой чувствительностью. При низкой активности ингибитора можно использовать соотношение: 2 части исследуемой плазмы / 1 часть контрольной. При высокой активности можно использовать соотношение 1: 4 и более и по степени коррекции косвенно судить об активности ингибитора.
После смешивания необходимо проводить тесты немедленно и через 1 час инкубации, что позволяет определить характер ингибитора (табл. 24).
Для более точной дифференциальной диагностики между истинным и вторичным дефицитом
Дифференциальная диагностика врожденного дефицита факторов VIII и IX, специфического ингибитора и волчаночного антикоагулянта
Таблица 24
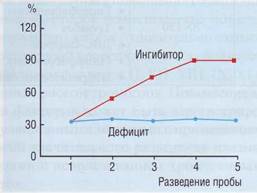
можно провести пробу с разведением, по крайней мере, до 3 разных концентраций. Пробы с дефицитом показывают при разведении одинаковый расчетный процент фактора в цельной плазме. Пробы, в которых присутствует ингибитор, при разведении показывают относительное увеличение фактора, что связано с диссоциацией
Рис. 102. Метод разведения пробы позволяет различить истинный дефицит фактора и его ингибирование.
При истинном дефиците разведение не меняет относительной активности фактора, а при подавлении активности фактора ингибитором разведение сопровождается относительным повышением активности фактора
комплекса фактор-ингибитор и освобождением фактора из блокированного состояния (рис. 102).
Обеспечение диагностики нарушений гемостаза в КДЛ
|
|