
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Прекращение реанимационных мероприятий
|
|
СЛР необходимо проводить так долго, как сохраняется на ЭКГ фибрилляция желудочков, поскольку при этом сохраняется минимальный метаболизм в миокарде, что обеспечивает потенциальную возможность восстановления самостоятельного кровообращения.
В случае остановки кровообращения по механизму асистолии при отсутствии потенциально обратимой причины (согласно алгоритму «четыре Г — четыре Т») СЛР проводят в течение 30 минут, а при ее неэффективности прекращают.
СЛР более 30 минут проводят в случаях гипотермии, утопления в ледяной воде и передозировке лекарственных препаратов.
Для базовой реанимации взрослых с остановкой сердца вне медицинского учреждения было сформулировано «правило прекращения реанимации», которое допускает прекращение основных мероприятий по поддержанию жизнедеятельности до прибытия машины скорой помощи при наличии всех перечисленных ниже критериев:
• Работник службы скорой медицинской помощи или лицо, оказывающее первую медицинскую помощь, не присутствовали при остановке сердца.
• Спонтанное кровообращение не восстановлено после трех полных
циклов СЛР и применения АНД.
Время прекращения реанимационных мероприятий фиксируется как время смерти пациента.
Стадия III — длительное поддержание жизни. Заключается в послереанимационной интенсивной терапии, которая проводится в РАО и включает этапы:
G (gauging) — оценка состояния;
Н (human mentation) восстановление сознания;
I — коррекция недостаточности функций органов.
Для постреанимационной болезни характерна своя особая этиология —сочетание глобальной ишемии(аноксии) с реперфузией(гиперемия), что вызывает каскад новых патологических изменений в органах и системах и прежде всего в ц.н.с. и сердце. Возможны: переломы грудины, ребер, повреждения легких, печени, кровотечения, аспирационный синдром. Все это наслаивается на причинное заболевание и усугубляет тяжесть состояния больного. Причины смерти в постреанимационном периоде: 1/3 — кардиальные (наиболее высок риск в первые 24 часа постреанимационного периода), 1/3 — дисфункция различных экстрацеребральных органов и 1/3 — неврологические (являются причиной смерти в отдаленном периоде ПРБ), характерен очень высокий уровень летальности, достигающий 80 % в течение 6 месяцев постреанимационного периода. Ни одна клетка организма так не зависит от уровня кислорода и глюкозы, как нейрон. Максимальный период времени клинической смерти (то есть аноксии) в условиях нормотермии, при котором возможно переживание нейронов, составляет не более 5 минут, поскольку в течение этого промежутка времени происходит полное потребление запасов глюкозы и АТФ головным мозгом, с последующим прекращением функционирования Na+-K+-АТФаз мембран клеток. Дисфункция этих систем приводит к нарушению ионного гомеостаза и последующему запуску трех основных механизмов аноксического повреждения клеток головного мозга: свободнорадикального, кальцийзависимого и фосфолипазного. Эти механизмы по мере своей реализации в конечном итоге приводят к гибели клеток мозга путем некроза или апоптоза.
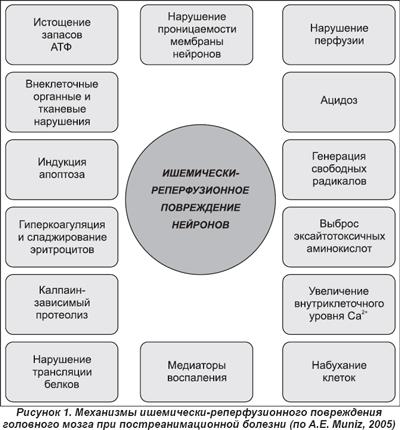
Активация анаэробного гликолиза вызывает повышение уровня неорганического фосфата, лактата и ионов Н+. Далее отмечается нарушение механизмов активного транспорта, деполяризация клеточных мембран и неуправляемый ток ионов Са2+ в цитозоль. Повышение активности ионов Са2+внутри клетки создает перегрузку митохондрий с разобщением окислительного фосфорилирования и усилением катаболических процессов. Цитотоксичность свойственна и возбуждающим аминоацидергическим нейротрансмиттерам (глутамату, аспартату), что получило название «эксайтотоксической смерти нейронов». Вовлекаются в патологический процесс зоны, менее пострадавшие от недостатка перфузии («принцип домино»). К этому присоединяют механизмы перекисного окисления, цитокиновых реакций, клеточной макрофагальной инфильтрации, нарушается реологический баланс, страдает регуляция сосудистого тонуса. В постреанимационном периоде гипергликемия приводит к более длительному неполному восстановлению рН ткани мозга и выраженному невосстановлению АТФ и креатинфосфата.
Выделяют три типа восстановления неврологического статуса в постаноксическом периоде:
1. Восстановление происходит после непродолжительного (3 часа) периода отсутствия сознания и характеризуется быстрой нормализацией адекватной психической деятельности в течении 24 часов после клинической смерти.
2. Задержанное восстановление функций ЦНС. Нарушение сознания (сомноленция, сопор, кома различной степени) может продолжаться в течение 3 суток и зависит от развития отека головного мозга.
3.Выраженные неврологические проявления в отдаленном периоде (1-2–3 мес.) декортикационная ригидность, децеребрация, апалический синдром.
Прогностическая оценка сознания в постреанимационном периоде. Для диагностики тяжести постаноксической гипоксии исследуют: реакция зрачка на свет, Постгипоксическая энцефалопатия описывается общемозговыми и очаговыми неврологическими симптомами.
В зависимости от уровня повреждения может наблюдаться различная степень угнетения сознания вплоть до атонической комы (кома III). Прогностически важным является состояние зрачков. Сохранение двустороннего расширения зрачков с изменением правильности их формы после прекращения действия «больших» доз адреномиметиков и холинолитиков свидетельствует о тяжелой степени энцефалопатии с неблагоприятным прогнозом для жизни. Даже в случае отсутствия подобной картины сохраняется вероятность необратимого повреждения корковых структур головного мозга с формированием к исходу острого периода неврологических признаков персистирующего, а затем и хронического вегетативного состояния, роговичный рефлекс, реакция на боль, рефлекс с трахео-бронхиального дерева, сроки восстановления спонтанного дыхания. Учесть седативную терапию и протокол гипотермии. Коматозное состояние в течение 48 и более часов выступает предиктором плохого неврологического исхода. Если через 72 часа после остановки кровообращения неврологический дефицит составляет меньше 5 баллов по шкале ком Глазго в отсутствие двигательной реакции в ответ на болевое раздражение или зрачкового рефлекса, это является предиктором развития персистирующего вегетативного состояния у всех больных.
Исследуются биохимические маркеры, позволяющие определить степень повреждения головного мозга, по аналогии с кардиоспецифическими ферментами при остром инфаркте миокарда. В основном исследуют уровень двух ферментов: нейронспецифической энолазы (NSE) и астроглиального протеина S-100. Так, концентрация в плазме NSE более чем 22 мкг/л (80% чувствительность и 100% специфичность), определяемая в течение первой недели после перенесенной остановки кровообращения, ассоциируется с развитием персистирующей комы.Уровень протеина S-100 более 0, 7 мкг/л в первые 24 часа постреанимационного периода ассоциируется с плохим неврологическим исходом.
Постреанимационные изменения в головном мозге укладываются в картину тотальной завершенной постгипоксической энцефалопатии. Для оценки состояния ЦНС используют клиническую оценку неврологического статуса по общепринятым шкалам (шкала ком Глазго), учитывая вероятность медикаментозного угнетения сознания препаратами, используемыми при проведении сердечно-легочной реанимации. Наличие у пациента уровня сознания менее 8 баллов (умеренная кома) свидетельствует о тяжелом повреждении мозга. Среди выживших только 15–20 % имеют быстрое восстановление адекватного уровня сознания, остальные 80 % пациентов проходят через постреанимационную болезнь.
Транскраниальная допплерография - Выраженность реперфузионного синдрома, а также косвенно судить о степени внутричерепной гипертензии. Наличие реверберирующего кровотока в крупных интра- и экстракраниальных сосудах на фоне АД, поддерживаемого на физиологическом уровне, является абсолютным признаком прекращения церебральной перфузии.
Прогрессирование постгипоксичекого отека головного мозга делает небесполезным мониторинг внутричерепного давления. Внутричерепная гипертензия представляет собой основной внутричерепной механизм прогрессирования повреждения мозга. В результате неконтролируемого увеличения внутричерепного объема крови, цитотоксического отека мозгового вещества складываются предпосылки для прогрессирования дислокационных механизмов, приводящих к вторичному повреждению подкорковых и стволовых отделов головного мозга. В целом повышение внутричерепного давления (ВЧД) или снижение системного среднего артериального давления (САД) способно уменьшать церебральное перфузионное давление и таким образом вызывать серьезное повреждение нейронов, т.е. наблюдаться клиника гипертензионно-дислокационного синдрома с артериальной гипертензией и брадикардией. Прогрессирование поражения стволовых отделов приводит к неконтролируемой артериальной гипотензии, характеризующейся резким снижением общего периферического сопротивления. Отличительным моментом такой гипотензии является отсутствие, вернее парадоксальная реакция на инотропную поддержку. Из-за утраты ауторегуляции мозгового кровотока искусственное повышение АД приводит лишь к церебральной гиперемии.
Признаком сохраняющейся (или нарастающей) гипоксии церебральной ткани является снижение сатурации, оттекающей от мозга по яремным венам крови. Падение этого показателя ниже 0, 5 прогностически считается неблагоприятным.
Для объективизации морфологических изменений ЦНС в различные периоды постреанимационной болезни используют компьютерную, магнитно-резонансную, позитронно-эмиссионную томографии (КТ, МРТ, ПЭТ), При компьютерной томографии определяется сглаженность извилин, компрессия ликворных цистерн, сдавление желудочковой системы, электро-энцефалографическое (ЭЭГ) исследование, ангиографию.
Постреанимационная болезнь затрагивает не только ЦНС, но и другие органы и системы. Отсутствие адекватного кровообращения, тканевая гипоксия, функциональные и морфологические изменения в различных сосудистых бассейнах могут приводить к развитию органной недостаточности(несостоятельности) и прежде всего миокардиальной дисфункции. Имеет различные клинические проявления. Согласно результатам исследований, у пациентов в 49 % случаев постреанимационная дисфункция миокарда манифестирует тахикардией, повышением КДД левого желудочка, а в первые 6 часов гипотензией (САД < 75 мм рт.ст.) и низким сердечным выбросом (СИ < 2, 2 л/мин/м2) Нарушение КОС-мет.ацидоз замещается мет.алкалозом, водно-электролитные нарушения, которые носят самый разнообразный характер..С индром системного воспалительного ответа. Почечная недостаточность.Пневмония.Пролежни.
|
|