
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Практическое занятие № 6
|
|
«Методика определения протеина (белка)».
Тема: «Азотистые вещества зерна».
Приборы и материалы: бачок-парообразователь, воронка, краны, зажим, воронка для щелочи, каплеуловитель, холодильник, приемная колба, колба Къелдаля.
Цель работы: изучить методику определения протеина в зерне и зернопродуктах.
Студент должен знать:
· значение азотистых веществ зерна;
· полноценность белков;
· содержание белковых веществ в зерне;
· классификацию белков;
· методику определения протеина.
Студент должен уметь:
· подготовить навеску;
· подготовить прибор к анализу;
· проводить расчеты.
Ход урока:
1. Закрепление теоретического материала.
2. Изучение методики.
3. Защита работы.
4. Проведение индивидуальных расчетов.
Вопросы к защите:
1. Классификация белков.
2. Этапы проведения анализа.
3. Подготовка аппарата.
4. Какие химические реакции происходят во время анализа?
5. Формула для расчета содержания протеина.
ПОРЯДОК РАБОТЫ:
1. ПОДГОТОВКА НАВЕСКИ. Навеску готовят так же, как и при определении зольности. Отбирают две навески, каждую высыпают в длинную, чистую, сухую пробирку. Пробирку с содержимым взвешивают на аналитических весах. Навеску пересыпают в колбу Кьельдаля, затем взвешивают пустую пробирку и по разнице массы пробирки с продуктом и без него находят величину навески.
2. МИНЕРАЛИЗАЦИЯ АЗОТА. В колбу наливают 10-15 мл концентрированной серной кислоты. Для ускорения реакции добавляют 0, 5-1, 0 г катализатора (10 частей сульфата меди, 100 частей сульфата калия, две весовые части селена). Содержимое колбы перемешивают, осторожно покачивая колбу, чтобы вся навеска была смочена кислотой. Затем колбу ставят на нагревательный прибор, находящийся в вытяжном шкафу. Вначале подогревание ведут медленно. Когда продукт обуглится и прекратится образование пены, нагревание усиливают, добиваясь равномерного непрерывного кипения жидкости. Черные несгоревшие частицы на стенках колбы смывают. Если они не смываются, то в колбу добавляют 5-10 мл серной кислоты и нагревание продолжают. Жидкость в колбе постепенно приобретает коричневый цвет, затем становится прозрачной зеленовато-голубого цвета. Если жидкость не имеет желтого оттенка, её кипятят в течение 20 минут, и сжигание считают законченным. Весь азот, входящий в различные вещества исследуемого продукта, после минерализации находится в составе сернокислого аммония (NH4)2SO4. Колбу после минерализации охлаждают.
3. ОТГОНКА. После охлаждения колбы к ее содержимому постепенно приливают 30 мл дистиллированной воды. Берут перегонный аппарат. Сначала присоединяют пустую колбу Кьельдаля и пустую приемную коническую колбу. В бачок-парообразователь через воронку наливают воду и включают нагревательный прибор. Доводят воду в бачке до кипения. Затем включают холодильник. Прибор пропаривают 5-10 минут. Это проводят для очистки прибора от остатков предыдущих опытов.
Затем вместо пустой колбы Кьельдаля ставят колбу с минерализованным азотом. В коническую колбу наливают из бюретки 25-30 мл 0, 1 н. раствора серной кислоты. Добавляют 4-5 капель индикатора (0, 20 г метилового красного и 0, 10 г метиленового голубого), и колбу ставят под холодильник вместо пустой конической колбы. Содержание конической колбы при добавлении индикатора становится красно-коричневым. Кончик холодильника обязательно погружают в раствор серной кислоты. В коническую воронку наливают 35-40 33%-ого раствора щелочи. Выливают щелочь в колбу Кьельдаля. Жидкость в колбе становится прозрачной, светло-голубого или синего цвета. В колбе, содержащей (NH4)2SO4, происходит реакция, в результате которой выделяется аммиак:
(NH4)2SO4+2NaOH→ Na2SO4+2NH3+2H2O
Выделившийся аммиак-это парообразное вещество. Он вместе с водяными парами из колбы Кьельдаля перемещается в холодильник. Попадая в холодильник, аммиак растворяется в воде, появляющейся при конденсации водяных паров, образуя раствор, который поступает в коническую колбу и вступает в реакцию с 0, 1 н. раствором серной кислоты. Через 15-17 минут считая сначала отгонки, объем жидкости в конической колбе должен увеличиться в 2 раза. Окончание отгонки проверяют по красной лакмусовой бумажке. Наносят на неё капли жидкости, стекающей из холодильника. Если бумажка не синеет, отгонка продолжаться не будет, если синеет, то отгонку продолжают.
4. ТИТРОВАНИЕ. Содержимое приемной колбы титруют 0, 1 н. раствором щелочи (едкого натрия) до появления зеленого окрашивания. В реакцию с щелочью вступает свободная 0, 1 н серная кислота, не вступившая в реакцию с раствором аммиака.
5. РАСЧЕТ. Содержание белка вычисляют по формуле:
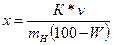
где К - постоянная величина (коэффициент) для перерасчета азота на сырой белок для пшеницы, ржи и овса=79, 8, для ячменя и семян бобовых культур=87, 5;
v - точное количество 0, 1 н. раствора серной кислоты, мл; вступившего в реакцию с аммиаком;
mH - масса навески размолотого зерна, г;
W - влажность зерна, %;
mH=mтары с нав.-mпустой тары;
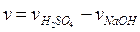
где, 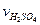 -25 или 30 мл.;
-25 или 30 мл.;
vNaOH- NaOH, израсходованный при титровании.
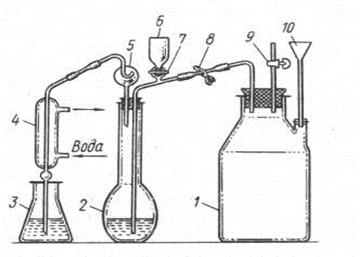
Рис.6. Перегонный аппарат.
1 — парообразователь;
2 — отгонная колба Кьельдаля;
3 — приемная колба;
4 — холодильник;
5 — каплеуловитель;
6 — воронка для гидроксида;
7 — краник;
8 — зажим;
9 — кран;
10 — воронка
|
|