
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Ход и данные опыта
|
|
Влияние концентрации реагирующих веществ на химическое равновесие исследовали при постоянной температуре на примере реакции взаимодействия хлорного железа (FeCl3) с роданидом калия (KCNS):
FeCl3 + 3KCNS Û Fe(CNS)3 + 3KCl.
Красное окрашивание роданида железа Fe(CNS)3 позволяет следить за сдвигом химического равновесия при изменении концентрации реагирующих веществ.
Изменение интенсивности окраски полученных растворов по сравнению с цветом раствора в контрольной пробирке указывает на направление смещения химического равновесия при изменении состава равновесной системы посредством добавления определенного реагента: FeCl3, KCNS или KCl. Результаты наблюдений представлены в табл. 3.
| Таблица 3 | |||
| Номер пробирки | Добавленное вещество | Изменение интенсивности окраски (ослаблениe, усиление) | Направление смещения равновесия (→, ←, Û) |
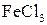
| |||
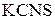
| |||

| |||
| Контрольная |
|
|