
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Катализ
|
|
Катализ – изменение скорости химической реакции в присутствии катализаторов. Катализ называют положительным, если скорость реакции увеличивается, и отрицательным, если скорость уменьшается. При гомогенном катализе реагенты и катализатор находятся в одной фазе, при гетерогенном катализе – в разных фазах.
Катализатор – вещество, участвующее в реакции и изменяющее ее скорость, но остающееся неизменным после того, как химическая реакция заканчивается. Катализатор, замедляющий реакцию, называют ингибитором. Биологические катализаторы белковой природы называют ферментами.
Механизм действия катализаторов состоит в том, что они образуют промежуточные соединения с исходными веществами и тем самым изменяют путь реакции, причем новый путь характеризуется другой высотой энергетического барьера, т.е. энергия активации изменяется по сравнению с некатализируемой реакцией (рис. 1). В случае положительного катализа она уменьшается, а отрицательного – увеличивается. Если изменение энергии активации составляет ∆ E = E некат – E кат, а предэкспоненциальный множитель в уравнении Аррениуса (3) при добавлении катализатора изменяется незначительно, то отношение констант скорости катализируемой и некатализируемой реакций будет примерно равно: 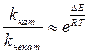 .
.
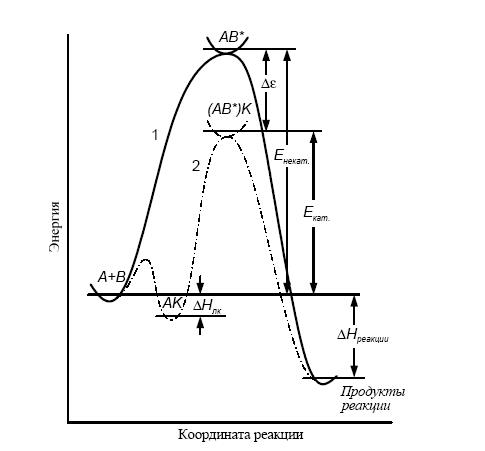
Рис. 1.Энергетические профили гомогенной реакции: сплошная кривая соответствует реакции без катализатора, пунктирная – каталитической реакции. Тепловой эффект каталитической реакции – такой же, как и в отсутствие катализатора
Например, при ∆ E ~ 40 кДж⋅ моль–1 и T = 300 К, скорость реакции увеличится в 9⋅ 106 раз.
Так как изменение термодинамических функций в химических реакциях определяется только состоянием реагентов и продуктов и не зависит от промежуточных стадий (закон Гесса), то катализатор не может повлиять ни на тепловой эффект реакции, ни на энергию Гиббса, ни на константу равновесия (в случае обратимой реакции). В последнем случае катализатор изменяет лишь время достижения равновесного состояния, но не его термодинамические характеристики.
|
|