
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Применение уравнения Аррениуса
|
|
Энергию активации можно рассчитать по экспериментальным данным графическим или аналитическим способами, используя уравнение Аррениуса
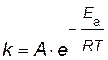 ,
,
представив его в логарифмическом виде
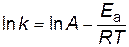 . .
| (2.16) |
Графический способ
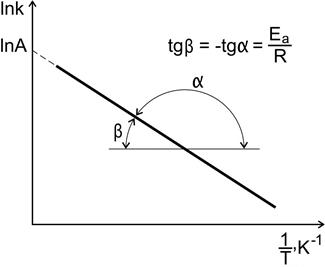
Рис. 8. Зависимость константы скорости реакции от температуры
По экспериментальным значениям константы скорости реакции при различных температурах строят график зависимости ln k = f (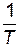 ) (рис. 8).
) (рис. 8).
По тангенсу угла наклона прямой к оси абсцисс вычисляют энергию активации
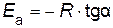 .
.
Аналитический способ
Если предположить, что для выбранной реакции величины А и Е а постоянны в небольших пределах температур от Т 1 до Т 2, то уравнение Аррениуса (2.16) можно применить для двух различных температур (Т 2> Т 1; k (Т 2) = k 2; k (Т 1) = k 1)
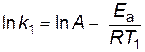 ;
;
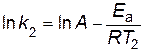 .
.
В результате вычитания первого уравнения из второго получим
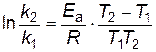 , ,
| (2.17) |
следовательно,
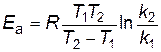 . .
| (2.18) |
Под символом логарифма находится отношение констант скоростей реакции при двух температурах, поэтому константы можно заменить любыми пропорциональными им величинами при тех же температурах. Например, вместо констант скоростей можно подставить скорости реакции, если исходные концентрации реагирующих веществ при измерении скоростей в обоих опытах были одинаковы и скорость изменилась только под влиянием изменения температуры. Тогда получим следующие выражения:
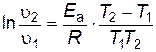 ; ;
| (2.19) |
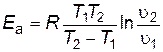 . .
| (2.20) |
|
|