
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Константа гидролиза. Поскольку гидролиз является равновесным процессом:
|
|
Поскольку гидролиз является равновесным процессом:
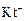 + HOH → ← KtOH +
+ HOH → ← KtOH + 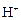 ,
,
соотношение продуктов и реагентов можно выразить с помощью константы гидролизаK г, являющейся константой равновесия – отношением концентраций продуктов и реагентов:
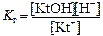
Концентрация воды остается постоянной и входит в константу.
Чем больше значение K г , тем полнее протекает гидролиз.
Константа гидролиза связана с константой диссоциации образующегося слабого электролита следующим соотношением:
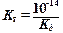
Чем слабее кислота или основание (чем меньше ихKд), тем сильнее гидролизуется образованная ими соль.
Интенсивность протекания гидролиза характеризует также степень гидролиза h – отношение числа молекул электролита, подвергшихся гидролизу N г, к общему числу молекул электролита в растворе Nобщ:
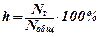
h зависит от природы соли, температуры и, в отличие от K г , от концентрации соли.
Количественно зависимость h от константы гидролиза K г и концентрации соли C выражает закон разбавления Оствальда:
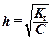
|
|