
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Применение метода коагуляции для очистки буровых растворов
|
|
Теоретические сведения
В практике очистки сточных вод, содержащих высокомолекулярные органические соединения, эмульгированные, мелкодисперсные и коллоидные частицы широко используется методы коагуляции и флокуляции.
Коагуляцией примесей воды называется процесс укрупнения коллоидных и взвешенных частиц дисперсной системы, происходящий в результате их взаимодействия и объединения в агрегаты. Завершается этот процесс осаждением образующихся агрегатов.
Эффективность процессов коагуляционной очистки сточных вод определяется устойчивостью дисперсной системы, которая зависит от ряда факторов: степени дисперсности, характера поверхности мицелл, величины электрокинетического потенциала, наличия в сточной воде других примесей, (например, электролитов, высокомолекулярных соединений), концентрации примесей и др.
Диспергированные, коллоидные и взвешенные частицы примесей природных и сточных вод, в большинстве случаев, имеют одинаковые заряды, что обусловливает возникновение межмолекулярных сил отталкивания и их агрегативную устойчивость. Большинство коллоидных частиц природных и сточных вод заряжено отрицательно. К таким коллоидам относятся кремниевая кислота, мельчайшие глинистые и почвенные частицы, гуминовые соединения и их производные, катионогенные поверхностно-активные вещества и др.
Поскольку в технологии очистки воды предусматривается частичное или полное удаление примесей, агрегативную устойчивость частичек стремятся разрушить.
В качестве коагулянтов обычно используют сульфат алюминия (АL2(SO4)3), оксихлорид алюминия, сульфат железа (II) или (III), хлорид железа (III), а также карбонат кальция, гидроксид магния, фосфат кальцияи др.
При растворении коагулянты гидролизуются. Например, гидролиз сульфата алюминия протекает по следующим стадиям:
A13++H2O=A1(OH)2++H+
Аl(ОH)2++Н2O= Аl(ОH)2++H+
Al(OH)2++H2O=Al(OH)з+H+
Alз++3H20=Al(OH)з+3H+
При гидролизе солей алюминия или железа в зависимости от рН среды могут образовываться также следующие соединения:
· катионного типа – Аl2(ОH)24+, Аl2(ОH)5+, Аl6(ОH)153+, Аl8(ОH)204+, Fе(ОН)+2, Fе2(ОН)4+2, , Fе(ОН)2+ (при низких рН);
· анионного типа – Аl(ОH)4-, Fе(Н2О)2 (ОН)4- (при высоких рН).
В воде при введении коагулянтов накапливаются ионы водорода, поэтому необходимо регулировать величину рН при очистке. Необходимым условием для более полного протекания гидролиза является удаление из сферы реакции образующихся А1(ОН)3, а также связывание ионов H+ в малодиссоциированные молекулы. Повышение рН раствора обеспечивает полный гидролиз введенного в воду коагулянта.
Для быстрого и полного гидролиза коагулянтов необходим некоторый щелочной резерв воды, т.е. наличие в ней определенного количества ионов НСО3- и ОН -, которые связывают ионы водорода, выделяющиеся при гидролизе: H++HCO3- =H2O+CO2
В тех случаях, когда концентрация ионов ОН-, НСО3 -, содержащихся в воде, недостаточна для полного гидролиза коагулянта, щелочность воды повышают введением гашеной извести (гидроксида кальция Са(ОН)2), гидроксида натрия или раствора соды (Na2CO3).
Количество добавляемого щелочного реагента можно определить по эмпирической формуле:


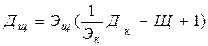 (1)
(1)
где Дщ – количество добавляемого щелочного реагента, мг/дм3;
Эщ – молярная масса эквивалента добавляемого щелочного реагента, ммоль-экв/дм3;
Дк – максимальная доза коагулянта, мг/дм3;
Эк – молярная масса эквивалента коагулянта, ммоль-экв/дм3;
Щ – минимальная щелочность воды, ммоль-экв/дм3.
Экспериментально установлено, что наибольший эффект очистки высокоцветных сточных вод при использовании в качестве коагулянта сульфата алюминия достигается в интервале значений рН среды от 6, 5 до 8, при использовании хлорида железа (III) – в интервале значений рН от 7, 0 до 8, 5, при использовании сульфата железа (II) – от 9, 0 до 9, 5.
Величина  резервной щелочности, которая остается после обработки воды коагулянтом, должна составлять не менее 1 мг-экв/л.
резервной щелочности, которая остается после обработки воды коагулянтом, должна составлять не менее 1 мг-экв/л.
Значения оптимальных значений рН при очистке сточных вод коагуляцией составляют:
| Al(OH)з - | 4, 5–7 | СаСО3 - | 9–11, 5 |
| Fе(ОН)2 - | 8, 5–10, 5 | Са3(РО4)2 - | 10–11 |
| Fе(ОН)3 - | 4–6 и 8–10 | СаSO4 - | 4–10 |
При введении в воду неорганических коагулянтов происходит снижение агрегативной устойчивости частиц, сорбция ионов на поверхности частиц и образование в результате химической реакции малорастворимого соединения.
Основными факторами, влияющими на процесс коагуляции примесей воды в объеме, являются:
- температура;
- щелочность воды;
- величина рН очищаемой воды и ее анионный состав;
- правильный выбор дозы коагулянта, быстрота его смешения и равномерность распределения в воде;
- содержание в воде естественных взвесей;
- условия протекания процесса хлопьеобразования.
По степени влияния на процесс коагуляции анионы могут быть расположены в ряд: Cl- < HCO3- < SO42-. В присутствии этих ионов увеличивается скорость коагуляции.
Правильный выбор дозы коагулянта имеет первостепенное значение для коагулирования примесей воды. Под дозой коагулянта подразумевается определенное массовое количество реагента, которое добавляется к единице объема обрабатываемой воды. Доза коагулянта измеряется в мг/л, г/м3.
График коагуляционной кривой приведен на рис.1. Кривую можно разбить на три зоны. В первой зоне при малых дозах коагулянта эффект осветления и обесцвечивания воды отстаиванием или фильтрованием незначителен. Во второй зоне увеличение дозы резко сказывается на эффекте осветления и обесцвечивания. Границу между первой и второй зонами называют порогом коагуляции – наименьшая концентрация реагента (электролита), при которой начинается коагуляция. В третьей зоне увеличение дозы коагулянта не дает заметного улучшения эффекта осветления и обесцвечивания воды. Граница между второй и третьей зонами носит название оптимальной дозы.
Оптимальной считается доза коагулянта, при обработке которой сточной воды образуются крупные хлопья, и достигается максимальное ее осветление через 15–20 мин.
Доза коагулянта для обесцвечивания высокоцветных вод ориентировочно может быть определена по формуле:
D= 4 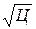 , (2)
, (2)
где D – доза сульфата алюминия, мг/л,
Ц – цветность воды по хромато-кобальтовой шкале, Цо.
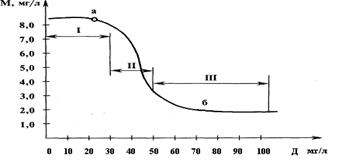
Рис.1. Коагуляционная кривая
а — порог коагуляции; б — оптимальная доза.
При коагуляционной очистке сточных вод одновременно протекают процессы соосаждения, сорбции и ионного обмена. В результате из воды могут удаляться органические вещества, поверхностно-активные вещества (ПАВ), ионы тяжелых металлов.
Конечным продуктом процесса коагулирования примесей воды являются хлопья, которые выделяются при осаждении, флокуляции или фильтровании. По своей структуре хлопья представляют собой цепочки гидроксида алюминия, на поверхности которых адсорбированы коллоидные и мелкодисперсные примеси. В свою очередь, эти цепочки могут прилипать к поверхности грубодисперсных примесей. При этом грубодисперсные примеси являются как бы центрами коагуляции, способствуя не только интенсификации процесса, но и формированию более крупных и плотных хлопьев, которые быстро выпадают в осадок или легко отфильтровываются.
Для ускорения процесса коагулирования, хлопьеобразования и повышения его эффективности используют флокулянты – высоко-молекулярные вещества – полиэлектролиты. Механизм действия флокулянтов заключается в их адсорбции на нескольких частицах с образованием полимерных мостиков, связывающих частицы между собой. Введение флокулянтов приводит к ускорению процесса хлопьеобразования и их осаждению, повышает плотность осадков.
В качестве флокулянтов для очистки природных и сточных вод от окрашенных и коллоидных частиц используют анионные полиэлектролиты, содержащие группы –СООН, -SO3Н, -ОН (активная кремниевая кислота, полиакрилат натрия, лигносульфонаты, полиакриламид, праестолы - высокомолекулярные соединения на основе полиакриламида и др.), катионные –полимеры, содержащие группы – NН2 , -NН (полиэтиленимин, сополимеры винилпиридина), амфотерные, содержащие катионные и анионные группы (гидролизованный полиакриламид).
На скорость и эффективность флокуляции существенное влияние оказывают концентрация коллоидных частиц, состав сточной воды, перемешивание. Например, процесс флокуляции полиакриламидом активизируется в присутствии гидроксидов кальция и магния. Высокое содержание солей сульфата калия, карбоната натрия, гидрофосфата натрия резко ухудшают процесс флокуляции.
На процесс флокуляции оказывает влияние молярная масса флокулянта. С увеличением размера макромолекул возрастает количество сегментов, способных к адсорбции на частицах. Это приводит к образованию более крупных агрегатов. Однако значительный рост молярной массы приводит к стерическим затруднениям и снижает эффективность процесса.
|
|