
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Опыт 5. Взаимное усиление гидролиза при взаимодействии растворов двух солей.
|
|
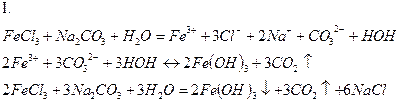
Выпадение осадка бурого цвета, выделение газа.
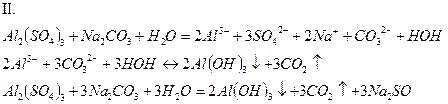
Выпадение белого осадка, выделение газа.
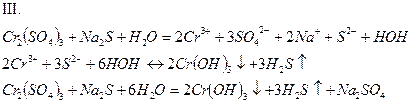
Выпадение осадка, выделение газа с неприятным запахом.
Вывод: В реакцию гидролиза вступают соли, образованные слабыми кислотой и основанием, слабым основанием и сильной кислотой и слабой кислотой и сильным основанием, а соли, образованные сильными кислотой и основанием гидролизу не подвергаются, т. к. ионы таких солей не могут образовывать с водой слабых электролитов. В рассмотренных случаях гидролизу подвергается не все количество соли, а только часть его, т. е. в растворе устанавливается равновесие между солью и образующими ее кислотой и основанием. Для большинства солей гидролиз – процесс обратимый. Процесс гидролиза может быть ступенчатым (например, гидролиз Al2(SO4)3, FeCl3).
Основываясь на результатах опытов, приходим к выводу, что чем слабее кислота, тем в большей степени подвержены гидролизу ее соли; чем слабее основание, тем в большей степени подвержены гидролизу образованные ею соли
Для того чтобы усилить гидролиз соли, надо разбавить раствор соли или нагреть его. Это часто позволяет довести гидролиз до конца.
|
|