
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Тропосферный аэрозоль.
|
|
Тропосферный аэрозоль имеет разное происхождение и химический состав. Химический состав аэрозолей определяется:
- происхождением
- превращениями под действием внешней среды – солнечного излучения, водяного пара и т.п.
Поступление аэрозолей от различных источников характеризуют следующие цифры:
 - океанический аэрозоль 1500
- океанический аэрозоль 1500
- терригенный (продукт разрушения
|
воздух пыль) 750
- вулканические извержения 50
- горение биомассы 140
- антропогенные выбросы 340
Океанический аэрозоль образуется в результате выброса в атмосферу капель морской воды (при разрыве пленки воды, покрывающей пузырек воздуха на гребне волны). Основным компонентом аэрозоля является NaCl – главная соль морской воды. Он обогащен такими элементами как Cu, Zn, V, Fe, Al и др. Эти элементы присутствуют в виде солей или могут быть включены как примеси в кристаллическую решетку NaCl.
Терригенный аэрозоль – возникает при выветривании и горных пород и поднятии пыли. Его основной источник – засушливые зоны, где пылевые бури поднимают в воздух большую массу твердых частиц.
Терригенный аэрозоль содержит в составе минералы на основе:
1) Al-Si, например, K[AlSi3O8] – полевой шпат, SiO2 – кварц;
2) фосфаты, например, апатит – Ca5(PO4)3[F, Cl, OH];
3) магнетит Fe3O4 ;
4) CaCO3
В составе терригенного аэрозоля присутсмвуют также тяжелые металлы – V, Cr, Mn, Ni и др.
Вулканический аэрозоль - по химичскому составу блтзок к наиболее распространенным магматическим породам, например базальтам. Средний состав базальтов:
| SiO2 | Al2O3 | FeO-Fe2O3 | MgO | CaO | TiO2 | MnO |
| 48.7-58.5 | 17.5-18.6 | 7.4-10.5 | 3.0-5.0 | 6.9-9.9 | 0.7-0.83 | 0.13-0.15 |
В составе пепла значительные количества примесей тяжелых металлов (десятые – сотые доли процента) – V, Cu, Co, Ni и др.
Присутствие атомов переменной валентности в составе вулканического пепла (например Fe) обуславливает каталитическую активность вулканических частиц.
Антропогенный аэрозоль
Источники антропогенного аэрозоля – промышленные предприятия, транспорт, различные виды деятельности, связанные с сжиганием биомассы (использование растительной массы в качестве топлива, сжигание отходов сельскохозяйственного производства, лесные и степные пожары инициируемые человеком).
Антропогенные источники аэрозолей сосредоточены на небольшой территории Земли, поэтому они обуславливают высокую аэрозольную загрязненность атмосферы в локальных и региональных масштабах, прежде всего атмосферы промышленных центров.
Химический состав городского аэрозоля формируется под действием всех источников города. В составе аэрозоля присутствуют частицы: 1) сажи, 2) несгоревшего топлива, 3) минеральные частицы – компоненты минеральной части органических топлив, 4) частицы истертых автопокрышек, 5) цементная пыль, 6)пыль металлургических производств и т.д. Отличительная черта городского аэрозоля – высокие содержания в нем органического углерода (более 50% общей массы всех аэрозольных частиц).
Аэрозольные частицы городских районах могут поступать в атмосферу не только от источников, но и иметь вторичное происхождение – образовываться в результате определенных фотохимических процессов из газообразных предшественников. Образование вторичных аэрозолей происходит в результате окисления молекул органических веществ и образования малолетучих соединений в концентрациях, превышающих давление насыщенного пара при температуре окружающей среды. Наиболее вероятные предшественники органических аэрозольных частиц в городах – ароматические углеводороды С6-С12, в сельских районах, в сельских районах монотерпеновые углеводороды (С10Н16), выделяемые в большом количестве различными растениями.
Стратосферный аэрозоль
Основной источник стратосферного аэрозоля – поступление аэрозольных частиц и их предшественников из тропосферы. Наиболее интенсивно это происходит при вулканических извержениях. Поэтому состав твердых частиц стратосферного аэрозоля в основном сходен с составом вулканического аэрозоля. При вулканическом извержении в атмосферу выбрасывается большое количество SO2, что приводи к образованию в стратосфере H2SO4 в жидкокапельной форме в результате постепенного окисления вулканического SO2, которое идет последовательно по схеме:
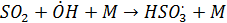
|
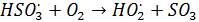
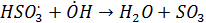
В стратосфере происходит также образование нитрозилсерной кислоты в реакциях с участием NO2
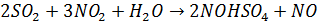
В стратосфере на высоте 18-20 км всегда присутствует слой серной кислоты аэрозоля с достаточно постоянными характеристиками [счетной концентрацией 1-3 см-3, диаметр частиц > 0, 15 мкм] - так называемый слой Юнге. Он помимо H2SO4 включает также частицы (NH4)SO4.
Существование слоя Юнге связывают не только с поступлением в стратосферу вулканического SO2, а в большей степени с химическими превращениями карбонилсульфида COS, образующегося при сжигании ископаемого топлива, выделяющегося в атмосферу в результате микробиологической активности в почвах. Время жизни COS в тропосфере около 1 года. Поэтому он переносится в стратосферу, где подвергается фотодиссоциации:
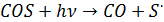 и затем
и затем
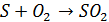
Слой Юнге оказывает существенное влияние на проницаемость атмосферы для солнечного излучения.
Химические процессы с участием атмосферного аэрозоля
Частицы аэрозоля участвую в процессах: 1) связанных с воздействием солнечной радиации; 2) в гетерогенных процессах, протекающих на их поверхности и 3) в жидкой фазе, покрывающей поверхность твердых частиц, или в жидкой фазе частиц жидкокапельных аэрозолей.
Твердые аэрозольные частицы являются центрами конденсации воды, поэтому их поверхность часто покрыта пленкой воды. Растворение кислотообразующих окислов (SO2, NO2) в пленке воды приводят к постепенному накоплению кислот и изменению химического состава твердых частиц – металлы могут при этом вымываться из минеральной матрицы и переходить в подвижные (ионные) формы. В частности наблюдается изменение химического состояния многих тяжелых металлов при их переносе в атмосферу в составе аэрозолей на большие расстояния. Например, Cu, Ni, Pb поступают в атмосферу в основном в составе нерастворимых соединений (доля нерастворимых форм от 60 до 100%), но в конечном итоге при переносе могут полностью перейти в растворимые формы. Растворенные компоненты могут выступать в качестве катализаторов гомогенных жидкофазных окислительных процессов. Например, в жидкой фазе аэрозолей ионы Fe присутствуют в основном в виде различных аквакомплексов типа 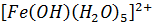 . Такие комплексы активно поглощают свет в широком спектральном диапазоне с образованием свободных радикалов.
. Такие комплексы активно поглощают свет в широком спектральном диапазоне с образованием свободных радикалов.
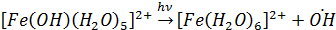
В ночное время в жидкой фазе радикалы образуются в реакции ионов Fe с H2O2:
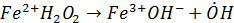
Присутствие восстановителей, например, формальдегида, придает процессу генерации свободных радикалов каталитический характер: Fe3+ восстанавливается до Fe2+
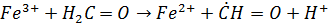
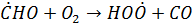
OH и OOH радикалы с высокой скоростью окисляют (в газовой и жидкой фазе) NO и SO2 в NO2 и SO3, а также инициируют окисление органических соединений.
Кроме жидкофазных реакций на поверхности частиц твердых аэрозолей происходит гетерогенное окисление газов и паров. Важную роль в таких процессах играют фотостимулированные реакции молекул с возбуждаемой излучением поверхностью твердых частиц, поскольку эти реакции формируют тропосферный сток даже химически инертных соединений.
Дело в том, что значительная часть минеральных компонентов атмосферного аэрозоля относятся к полупроводниковым, обладающим свойством фотопроводимости. Причем для многих материалов аэрозолей характерно возникновение проводимости воздействии излучения ближнего ультрафиолетового и видимого диапазона (TiO2, ZnO, ZnS, Fe2O3). Одновременно это обуславливает возникновение фотосорбции (повышение сорбционной способности твердых частиц при облучении светом). На возбужденной светом поверхности частиц генерируются (+) и (-) заряженные активные центры, которые обуславливают протекание на поверхности реакций с сорбированными веществами, приводящих к важным результатам. Например, в обводненных аэрозолях взаимодействие молекул воды с (+) заряженными центрами приводит к образованию катион-радикала (H-OH)˙ + , который быстро диссоциирует на протон H+ и гидроксильный радикал OH (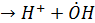 ). На поверхности фотовозбужденных частиц могут сорбироваться и химически трансформироваться даже абсолютно инертные в условиях тропосферы примеси – на фотовозбужденной поверхности может происходить разложение N2O и даже N2:
). На поверхности фотовозбужденных частиц могут сорбироваться и химически трансформироваться даже абсолютно инертные в условиях тропосферы примеси – на фотовозбужденной поверхности может происходить разложение N2O и даже N2:
N2Ohν TiO2, ZnON2+O2
N2+3H2Ohν TiO22NH3+O2
Установлена возможность фотостимулированного разложения ФХУ, CCl4, на поверхности частиц песка, вулканического пепла в результате реакции с поверхностью связанных кислородом [фотодиссоциация молекул O2 приводит к образованию высокоактивного супероксида O2− - отрицательно заряженного молекулярного иона O2, связанного с поверхностью]. Механизм фотостимулирования разложения ХФУ состоит в следующем (на примере CFCl3):
MeO(O2− )+ CFCl3=MeO(O2) + (CFCl3− )адс
(CFCl3− )адс→ (Cl− )адс + (CFCl2)адс
|
|
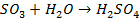 конденсация паров H2SO4 приводит к образованию аэрозольных частиц
конденсация паров H2SO4 приводит к образованию аэрозольных частиц