
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Состав, строение и свойства атмосферы
|
|
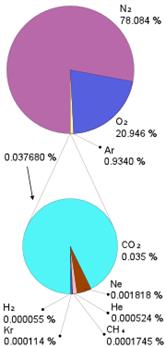
Состав
Атмосфера (газовая оболочка Земли) содержит ~ 5, 15*1015 тонн воздуха.
Основные компоненты атмосферного воздуха – N2, O2 (в сумме > 99%)/ Кроме них в заметном количестве присутствуют Ar (0.93%) и CO2 (~0.035 % объема). Другие естественные примеси (He, H2, Ne, Kr, CH4) содержатся в воздухе в концентрации 0, 001 – 0, 0001% (об.). Перечисленные вещества присутствуют в атмосфере в постоянных концентрациях. Для множества других примесей в атмосфере характерна изменчивость концентрации во времени и в разных частях.
Важнейшим компонентом атмосферы являются пары вод ы, определяющие тепловой режим атмосферы.
Концентрация водяного пара переменна и по высоте, и широте. Основная масса паров воды сосредоточена в нижних слоях атмосферы (тропосфере) вблизи поверхности земли, их концентрация легко уменьшается с высотой.
В нижних слоях наблюдается так же большой широтный разброс концентрации паров воды - от тысячи долей % в арктических районах, до % в тропиках.
Единицы измерения концентраций примесей
Для измерения содержания примесей в атмосфере помимо % (объемных) часто используют другие единицы измерения содержания газообразных компонентов в смеси.
В частности широкое распространение получили единицы концентрации миллионные (миллиардные) доли - млн-1 (млрд-1) – часть на миллион (миллиард) – в англоязычном выражении ppm (ppb) – количество объемов примеси в 1 млн (млрд) объемов смеси – т.е.1 м3 /106м3 (или 10-6 м3/м3).
Очевидно взаимосвязь ppm с % объемн:
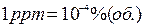
Так же для выражения массовой концентрации примесей используется единицы м2/м3 (и реже мкг/м3) - в них выражают ПДК загрязняющих веществ в воздухе, дают оценку уровня загрязнения атмосферы.
В практике достаточно часто возникает необходимость пересчета значений концентраций, выраженных в ppm, в массовые (мг/м3) и наоборот. Пересчет производится по формуле:
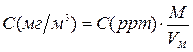 , где
, где
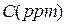 ,
, 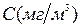 - концентрация, выраженная соответственно в м.д. и мг/м3
- концентрация, выраженная соответственно в м.д. и мг/м3
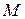 - молекулярная масса вещества,
- молекулярная масса вещества,
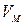 - мольный объем
- мольный объем
Формула легко выводится, если в заданной массовой концентрации содержания вещества в мг перевести в единицы объема (м3)



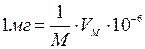 -
-

1 мг/м3 =n*ppm
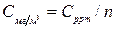
1ppm=1 мг/м3 = 
При н.у. (Т=273 К, р=1 ат=101, 3 кПа)

В принципе при большой погрешности для типичных условий в атмосфере пересчет концентраций можно производить, подставляю в формулу V0, т.е.
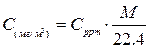
Для получения точного результата расчета необходимо учитывать реальные температуру и давление. Знание мольного объема при фактических условиях определяется из уравнения состояния:
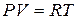 , откуда
, откуда 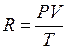
Подставляя реальные значения P, V, T и те же значения при н.у. получаем
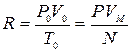 , откуда
, откуда 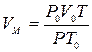
 И тогда
И тогда 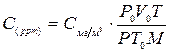
Или 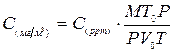
Пример
Порог обнаружения запаха NH3 составляет 32 мг/м3, максимально разовая ПДК в атмосферном воздухе 0, 2 мг/м3. Обнаружится ли органолептически (т.е. по запаху) аммиак в воздухе при концентрации 20 ppm. Представляет ли опасность для человека вдыхание воздуха с такой концентрацией аммиака (tвозд = 200С, давление 730 мм.рт.ст.)
Для ответа на вопросы необходимо сравниваемые концентрации привести к одинаковым единицам измерения – очевидно проще это сделать для одной концентрации, выраженной в ppm, переведя ее в мг/м3
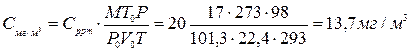
Помимо рассмотренных способов выражения концентрации примесей в воздухе иногда используют так называемую «счетную» концентрацию – количество молекул (частиц) вещества в 1 см3 или 1 м3 воздуха (размерность см-3 или м-3, т.е. молекул/см3 (м3). Чаще такой способ выражения концентрации принимают для аэрозольных частиц (количество частиц в 1 см3 и м3)
Теперь о строении и свойствах атмосферы
Атмосфера во всем объеме неоднородная по свойствам среда. Эта неоднородность проявляется прежде всего по высоте на уровнем земной поверхности. По высоте в атмосфере можно выделить несколько слоев (сфер), различающихся характером изменения температуры. Вертикальный температурный профиль выглядит так
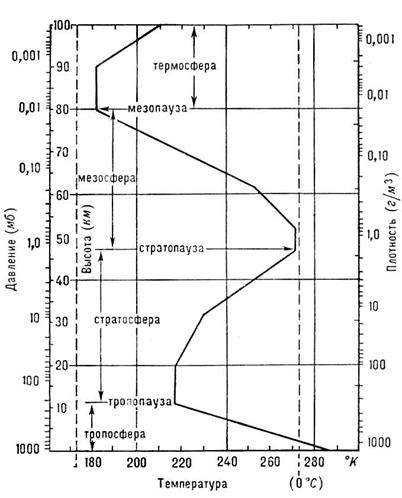
Нижний слой, непосредственно прилегающий к Земле – тропосфера, затем стратосфера, мезосфера, термосфера (простирается до высоты ~ 1000 км, на которой происходит рассеяние вещества в открытый космос).
Сферы разделены узкими переходными зонами – паузами (по названию предыдущего слоя), в пределах которых меняется направления температурной кривой.
Характеристика слоев:
Тропосфера – характеризуется средним вертикальным градиентом температур -6, 5 град/км (т.е. понижение температуры). Верхняя граница ее лежит на высоте от 8 км в полярных широтах до 16-18 км на экваторе. К тропопаузе температура понижается до ~230К.
В стратосфере – до высоты ~25 км температуру остается почти постоянной, затем возрастает до 270 К (почти до 00С) на нижней границе стратопаузы. Температурный градиент в стратосфере +1, 4 град/км.
Мезосфера, расположенная выше, характеризуется новым понижением температуры (~до -1000С на высоте 80 км)
В термосфере воздух сильно разряжен – здесь можно дать оценку лишь критической температуры – соответствующей кинетической энергии движения молекул – температура равномерно возрастает/
Помимо такого деления атмосферы на слои в ней выделяют так же слои с другими характерными признаками и другими названиями; слов, включающий тропосферу и нижнюю часть стратосферы, где преимущественно протекают химические реакции – хемосфера; слой выше 80 км, где значительное содержание заряженных частиц – ионосфера.
Давление в атмосфере в отличие от температуры, которая изменяется неоднозначно, монотонно и равномерно (и достаточно быстро) уменьшается с высотой – на верхней границе стратосферы (~ 50 км) оно уменьшается до 1 мм. рт. ст.
Распределение давления по высоте можно описать так называемой «барометрической формулой», которой может быть выведена из уравнения состояния идеального газа:
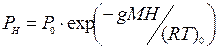 (1)
(1)
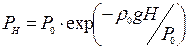 - эквивалентная запись формулы
- эквивалентная запись формулы
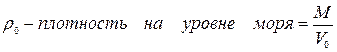
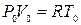
где H – высота;
P0 – давление при Н=0 (на уровне моря) (101, 3 кПа);
g – ускорение силы тяжести (9, 806 м/с2);
M – средняя молекулярная масса воздуха (28, 9)
R – универсальная газовая постоянная (8, 31 Дж/моль*К)
Уравнение вида (1) описывает изменение и некоторых других параметров атмосферы – например, изменение с высотой количества молекул газа в единице объема (т.е. изменение «счетной» концентрации)
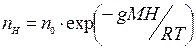 , где
, где
n0 – количество молекул в единице объема на высоте Н0
При н.у. (273 К, 101, 3 кПа) в 1 см3 газа содержит 2, 96*1019 молекул – число Лошмидта
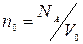 , где
, где
NA – число Авогадро – число молекул 1 моля любого газа (6, 02 * 1023)
V0 – мольный объем при н.у. (22, 4*103 см3)
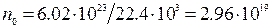
При фактическом значении Р и Т
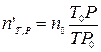
|
|