
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Общая характеристика порошков
|
|
Обычно порошки рассматривают с точки зрения природы вещества дисперсной фазы и размеров частиц.
ПРИРОДА ВЕЩЕСТВА ДИСПЕРСНОЙ ФАЗЫ
Рассмотрим только те характеристики вещества, на которых основаны свойства порошков, влияющие на технологию их использования и переработки.
Когезия определяет связь между молекулами (атомами, ионами) внутри тела в пределах одной фазы, т. е. прочность конденсированных тел и их способность противодействовать внешнему воздействию. Следовательно, энергетические затраты при диспергировании тем больше, чем больше когезия. Кроме того, величина когезия определяет такую важную характеристику порошка, как его насыпная масса. Насыпная масса – масса порошка, который занимает единичный объем при свободном его заполнении, «свободной упаковке частиц». Чем больше когезионные силы, тем сильнее связь между частицами, тем хаотичнее они распределены по объему формы и тем больше объем свободной упаковки и соответственно меньше насыпная масса. Если когезия мала, то малы силы сцепления, порошок лучше уплотняется под действием силы тяжести и объем свободной упаковки частиц оказывается небольшим.
Адгезия – это явление соединения приведенных в контакт поверхностей конденсированных фаз. Например, частички порошка взаимодействуют со стенками емкости, в которой они находятся. Адгезия обусловливает прилипание и удержание частиц на поверхности. Чем больше адгезия, тем сложнее бороться с прилипанием порошка к стенкам технологического оборудования.
Аутогезия – частный случай адгезии – сцепление одинаковых по составу и строению частиц. Адгезионное и аутогезионное взаимодействие направлены перпендикулярно площади контакта. В результате адгезии частицы порошка прижимаются к поверхности, а под действием аутогезии – друг к другу.
Аутогезия определяется, главным образом, природой и силой межчастичного взаимодействия. Основной вклад в межчастичное взаимодействие вносят
• межмолекулярное притяжение;
• электростатическое отталкивание.
Электростатическое отталкивание связано с появлением заряда поверхности при перемещении частиц друг относительно друга и их соударениях. Роль электростатических взаимодействий особенно велика для полимерных частиц.
Установлено, что для сферических частиц число точек контактов не превышает 12. Чем больше точек соприкосновения частиц, тем больше поверхность контакта и меньше удельная поверхность. Под поверхностью контакта для порошков понимают поверхность двух соприкасающихся частиц, расположенную в зоне действия молекулярных сил (~ 0, 1 нм). Для сферической частицы радиусом r поверхностью контакта считается поверхность ее сегмента с высотой h = 0, 1 нм, а доля этой поверхности составляет
у = 
где nk – число контактов, d = 2 r.
Из приведенной формулы следует, что поверхность контакта увеличивается с уменьшением размера частиц.
РАЗМЕРЫ ЧАСТИЦ ПОРОШКА
(ДИСПЕРСНОСТЬ)
От размера частиц зависит удельная площадь межфазной поверхности S уд. Напомним, что для сферической частицы диаметра d:
S уд =  см
см  1,
1,
а для частиц сложной формы
S уд = 
где 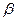 – коэффициент, зависящий от формы частиц (
– коэффициент, зависящий от формы частиц (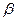 > 6). Увеличение удельной межфазной поверхности приводит к следующему:
> 6). Увеличение удельной межфазной поверхности приводит к следующему:
• интенсификации процессов, протекающих на поверхности порошка;
• усилению яркости окраски пигментов;
• повышению качества композиционных материалов;
• улучшению вкусовых качеств пищевых продуктов. Однако с уменьшением
размеров частиц порошка усиливаются и его негативные свойства:
• слеживаемость;
• прилипаемость к поверхностям оборудования и тары;
• уменьшение текучести (сыпучести).
Это затрудняет технологические процессы: смешение, дозировку, транспортировку и др.
Начиная с некоторого критического размера частиц (d 0, кр) сила связи между частицами F св становится равной силе тяжести:

где п – число контактов, т – масса частицы; g – ускорение свободного падения.
Дальнейшее уменьшение размеров частиц приводит к самопроизвольному образованию пространственных структур.
Для высокодисперсных порошков критический размер:
d 0, кр  [
[  ]
] 
где  – эффективная плотность частицы в дисперсионной среде (
– эффективная плотность частицы в дисперсионной среде ( =
= 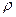 част –
част – 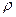 газ
газ 
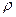 част). При расчете реальных значений d 0, кр получается величина - 100 мкм. Для увлажненных порошков, в которых существенную роль играют капиллярные силы, значение d 0, кр на порядок больше. Итак, значение d 0, кр служит критерием агрегируемости порошка.
част). При расчете реальных значений d 0, кр получается величина - 100 мкм. Для увлажненных порошков, в которых существенную роль играют капиллярные силы, значение d 0, кр на порядок больше. Итак, значение d 0, кр служит критерием агрегируемости порошка.
Высокодисперсные порошки с диаметром частиц d гораздо меньше d 0, кр являются связнодисперсными, в них возникает пространственная структура. Если d> > d 0, кр , то такие порошки являются свободнодисперсными.
|
|