
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Глава 2. Получение
|
|
Стр.
Глава 1. Нахождение в природе________________________________ 3
1.1 Распространённость_____________________________________ 3
Природные соединения алюминия________________________ 3
Изотопы алюминия______________________________________ 3
Глава 2. Получение__________________________________________ 4
Глава 3. Физические свойства_________________________________ 5
Глава 4. Электронное строение атома алюминия________________ 6
Глава 5. Химические свойства________________________________ 7
Глава 6. Применение_________________________________________ 9
Кусок алюминия________________________________________ 9
В качестве восстановителя______________________________ 10
Сплавы на основе алюминия____________________________ 10
Алюминий как добавка в другие сплавы__________________ 12
Ювелирные изделия____________________________________ 12
Столовые приборы_____________________________________ 13
Стекловарение_________________________________________ 13
Пищевая промышленность______________________________ 13
Военная промышленность_______________________________ 13
Алюминий и его соединения в ракетной технике_________ 13
Алюмоэнергетика______________________________________ 14
Список используемой литературы_____________________________ 15
Глава 1. Нахождение в природе
1.1 Распространённость
По распространённости в земной коре Земли занимает 1-е место среди металлов и 3-е место среди элементов, уступая только кислороду и кремнию. Массовая концентрация алюминия в земной коре, по данным различных исследователей, оценивается от 7, 45 до 8, 14 %.
Природные соединения алюминия
В природе алюминий, в связи с высокой химической активностью, встречается почти исключительно в виде соединений. Некоторые из природных минералов алюминия:
Бокситы — Al2O3 · H2O (с примесями SiO2, Fe2O3, CaCO3)
Нефелины — KNa3[AlSiO4]4
Алуниты — (Na, K)2SO4·Al2(SO4)3·4Al(OH)3
Глинозёмы (смеси каолинов с песком SiO2, известняком CaCO3, магнезитом MgCO3)
Корунд (сапфир, рубин, наждак) — Al2O3
Полевые шпаты — (K, Na)2O·Al2O3·6SiO2, Ca[Al2Si2O8]
Каолинит — Al2O3·2SiO2 · 2H2O
Берилл (изумруд, аквамарин) — 3ВеО · Al2О3 · 6SiO2
Хризоберилл (александрит) — BeAl2O4.
Тем не менее, в некоторых специфических восстановительных условиях (жерла вулканов) найдены ничтожные количества самородного металлического алюминия.
В природных водах алюминий содержится в виде малотоксичных химических соединений, например, фторида алюминия. Вид катиона или аниона зависит, в первую очередь, от кислотности водной среды. Концентрации алюминия в водоёмах России колеблются от 0, 001 до 10 мг/л. В морской воде его концентрация 0, 01 мг/л.
Изотопы алюминия
Природный алюминий состоит практически полностью из единственного стабильного изотопа 27Al с ничтожными следами 26Al, наиболее долгоживущего радиоактивного изотопа с периодом полураспада 720 тыс. лет, образующегося в атмосфере при расщеплении ядер аргона 40Ar протонами космических лучей с высокими энергиями.
Глава 2. Получение
Алюминий образует прочную химическую связь с кислородом. По сравнению с другими металлами, восстановление алюминия из руды более сложно в связи с его высокой реакционной способностью и с высокой температурой плавления большинства его руд (таких, как бокситы). Прямое восстановление углеродом применяться не может, потому что восстановительная способность алюминия выше, чем у углерода. Возможно непрямое восстановление с получением промежуточного продукта Al4C3, который подвергается разложению при 1900—2000 °С с образованием алюминия. Этот способ находится в разработке, но представляется более выгодным, чем процесс Холла—Эру, так как требует меньших энергозатрат и приводит к образованию меньшего количества CO2.
Современный метод получения, процесс Холла—Эру[en] был разработан независимо американцем Чарльзом Холлом и французом Полем Эру в 1886 году. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием расходуемых коксовых или графитовых анодных электродов. Такой метод получения требует очень больших затрат электроэнергии, и поэтому получил промышленное применение только в XX веке.
Для производства 1000 кг чернового алюминия требуется 1920 кг глинозёма, 65 кг криолита, 35 кг фторида алюминия, 600 кг анодных графитовых электродов и около 17 МВт·ч электроэнергии (~61 ГДж).
Лабораторный способ получения алюминия предложил Фридрих Вёлер в 1827 году восстановлением металлическим калием безводного хлорида алюминия (реакция протекает при нагревании без доступа воздуха):
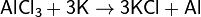
|
|