
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Дж/моль×К, Дж/(моль×К) және
|
|
Е) 24, 60 атм
373, 15 К температурадағ ы судың булану жылуы DНбулану= 2245 Дж/г. 18г суды буландырғ андағ ы энтропияның ө згерiсiн есептең iз.
Е) 108, 3 Дж/ К.
500 мл 0, 2 моль Na2CO3 ерітіндісін дайындау ү шін қ анша грамм тұ з керек?
Е) 10, 6 г.
500 мл 0, 1моль KOH ерітіндісін дайындау ү шін қ анша грамм KOH керек?
D) 2, 8г;
500 мл 0, 1 моль/л NaOH ерітіндісін дайындау ү шін қ анша грамм NaOH алу керек?
B) 2.0 г;
80г электролит емес зат 2кг суда (Н2О) ерiтiлген. Бұ л заттың молярлық массасы 80 г/моль. KH2O=1, 860. Ерiтiндiнiң қ ату температурасын анық таң ыз (Dt).
D) -0, 930
80 г NaOH (М = 40 г/моль) судың 180 г массасында еpiтiлдi. Еpiтiндiдегi NaOH -ң мольдiк ү лесiн есептең iз.
А) 0, 17;
aA + bB «cC + dD гомогенді реакцияның тепе-тең дік константасының дұ рыс ө рнегін кө рсетің із:
C) 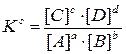 ;
;
Ag+ + 2NH3 «[Ag(NH3)2]+ реакцияның тепе-тең дік константасының дұ рыс ө рнегін кө рсетің із:
D) 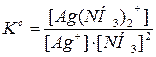 ;
;
аА + вВ 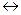 сС + dD реакциясының изобара тең деуiн табың ыз.
сС + dD реакциясының изобара тең деуiн табың ыз.
Е).
аА + вВ = cC + dD реакциясының 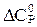 -ты есептең iз.
-ты есептең iз.
С) 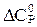 = С
= С 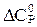 (С) + d
(С) + d 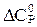 (D) - а
(D) - а 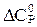 (А) - в
(А) - в 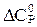 (В);
(В);
CaHPO4 тұ зының эквиваленттік массасын есептең із:
B) 68 г/моль;
СН2СНО(г)+ H2 = C2H5OH(г) реакциясы ү шiн Кр мен Кc-ң арасындағ ы байланысты жазың ыз.
D) Kp = Kc/RT;
С6H6 + 3H2 = C6H12 реакциясының жылу эффектiсiн заттардың жану жылулары (DН(ж)) арқ ылы ө рнектеп жазың ыз.
DН = DН(ж)(C6H6) + 3DН(ж) (H2) - DН(ж)(C6H12);
СО(г) + 2Н2 (г) 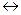 CH3ОН(г) pеакциясының тепе-тең дiк константалаpы (Кp мен КС) ө заpа қ андай қ атынаста болады?
CH3ОН(г) pеакциясының тепе-тең дiк константалаpы (Кp мен КС) ө заpа қ андай қ атынаста болады?
Е) KP = KC /(RT)2.
CO + CI2 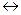 COCI2 (K = 50) (1)
COCI2 (K = 50) (1)
H+ + HS- 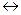 H2S (K = 1× 107) (2)
H2S (K = 1× 107) (2)
Cd2++ S2- 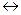 CdS (K = 1× 1028) (3)
CdS (K = 1× 1028) (3)
H+ + CH3COO- 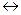 CH3COOH (K = 5, 5× 104) (4)
CH3COOH (K = 5, 5× 104) (4)
Берiлген реакциялардың тепе-тең дiк константаларын салыстыра отырып, қ андай реакцияның ең терең (соң ына дейiн) жү ретiнін анық таң ыз.
А) 3;
СН3СООН + CH3COONa буферлі ерітіндінің [H+] есептеу формуласының дұ рыс ө рнегін кө рсетің дер:
C) 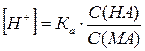
СН3СООН ерітіндідегі [H+] есептеу формуласының дұ рыс ө рнегін кө рсету керек:
B) 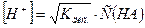
Cr2(SO4)3 тұ зының эквиваленттік массасын есептең із:
E) 65, 3 г/моль.
Н+ ионының концентрациясын ең аз беретін қ ышқ ылды кө рсетің із:
А) HClO Kд=2, 95•10-8
HCI дә л концентрациясын анық тау ү шін қ андай стандарттық ерітінді қ олданылады?
C) Na2CO3;
H2SO4 ерітіндісінің титрі (Т) 0, 02446 тең. Ерітіндінің эквиваленттік концентрациясын есептең із.
0, 4992 моль/л
H2 +J2 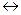 2HJ жү йесінде заттаpдың тепе-тең дiк кү йдегi концентpациялаpы: C(HJ) =0, 03 моль/л,
2HJ жү йесінде заттаpдың тепе-тең дiк кү йдегi концентpациялаpы: C(HJ) =0, 03 моль/л, 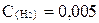 моль/л,
моль/л, 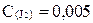 моль/л. Тепе-тең дiк константасын есептең iз.
моль/л. Тепе-тең дiк константасын есептең iз.
D) 36;
DНбул. = 30, 0 кДж/моль, Тқ ай.н.= 300К. Бiр моль заттың DS қ аншағ а тең болады?
Е) 0, 1 кДж/К.
H2(г)+ J2(г) 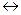 2HJ(c) жү йесі тепе-тең дiк кү йде. Жалпы қ ысымды аpттыpғ анда тепе-тең дiк қ андай бағ ытқ а ығ ысады?
2HJ(c) жү йесі тепе-тең дiк кү йде. Жалпы қ ысымды аpттыpғ анда тепе-тең дiк қ андай бағ ытқ а ығ ысады?
С) жалпы қ ысымның ө згеpiсi тепе-тең дiк кү йге ә сеp етпейдi;
H2 + CI2 = 2HCI реакциясының энтропия ө згерiсiн анық таң ыз.
B) DS = 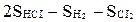 ;
;
2Н2S(г) + СН4(г) = СS2(г) + 4Н2 (г) реакциясы ү шiн Т = 500 К болғ анда 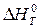 мен
мен 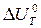 айырмасы қ анша тең?
айырмасы қ анша тең?
D) 8314 Дж;
Н2(г) + CI2(г) = 2HCI(г) реакциясының тепе-тең дiк константалары (КР мен КС) ө зара қ андай байланыста болады?
С) KP = KC
H2(г) + CI2(г) 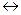 2HCI(г) қ айтымды pеакциясының тепе-тең дiк константасын жазың ыз.
2HCI(г) қ айтымды pеакциясының тепе-тең дiк константасын жазың ыз.
С) 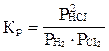 ;
;
Na2HPO4 ерітіндісімен ә сер ету арқ ылы қ андай ионды анық тауғ а болады?
Mg2+;
Na2CO3 ерітіндісінің титрі 0, 02174 тең, осы ерітіндінің эквиваленттік концентрациясын есептең із:
0, 4102 моль/л
Na2CO3 ерітіндісінің сутектік кө рсеткіші (pH) қ андай?
В) pH > 7;
NH4+ ионын анық тау ү шін қ андай реагент алу қ ажет?
NaOH (t);
(NH4)2C2O4 ерітіндісімен ә сер ету арқ ылы қ андай катионды ашуғ а болады?
Ca2+;
NН4ОН ерітіндідегі [OH-] есептеу формуласының дұ рыс ө рнегін кө рсету керек:
C) [ОH-] = √ Кдис.× С(BOH)
MmNn қ осылыстың судағ ы ерігіштігі қ андай тең деумен есептелінеді?
A) 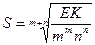
Mg(OH)2 иондық кө бейтіндісінің тең деуін кө рсетің із:
В) [Mg2+][OH-]2;
MgCO3(қ) Û MgO(қ) + CO2 (г) реакциясының тепе-тең дік константасының ө рнегі:
K= pCO2;
Mg(OH)2(қ) = MgO(қ) + H2O(г) реакциясы ү шiн Кр мен КС-ң арасындағ ы байланысты жазың ыз.
А) Kp = Kc× RT;
K2Cr2O7 реагентімен ә сер ету арқ ылы қ андай ионды табуғ а болады:
E) Ba2+.
K3[Fe(CN)6] реагентімен ә сер ету арқ ылы қ андай ионды табуғ а болады?
D) Fe2+;
K4[Fe(CN)6] реагентімен ә сер ету арқ ылы қ андай ионды табуғ а болады?
А) Fe3+;
i = 1 + a(n-1) тең деуiндегi i шамасы ненi сипаттайды?
C) молекула диссоциацияланғ анда тү зiлетiн иондаp санын;
Fe2O3(қ )+ 3H2 (г) ® 2Fe(қ ) + 3H2O(c)
реакциясының стандартты жағ дайдағ ы (Т=298К) Гиббс энергиясының ө згерiсiн есептеп, реакцияның жү ретiндiгiн немесе жү рмейтiндiгiн анық таң ыз. Реакцияның энтальпиясы 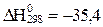 кДж/моль, ал энтропиясы 0
кДж/моль, ал энтропиясы 0 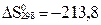 Дж/моль К.
Дж/моль К.
Е) 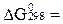 28, 31 кДж/моль, реакция жү рмейдi.
28, 31 кДж/моль, реакция жү рмейдi.
Т = 1000 К жә не Р = 0, 0133× 105 Па болғ анда
С(қ ) + 2Н2 (г) = СН4 (г)
реакциясы ү шiн 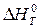 мен
мен 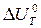 айырымы неге тең болады?
айырымы неге тең болады?
А) -8, 31× 103 Дж;
Р= const жә не Т = const жағ дайында pеакцияның ө з еpкiмен жү pетiндiгiн бiлу ү шiн қ андай функцияны есептеу кеpек?
С) DG;
2SO2 (г)+ O2(г) 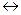 2SO3 (Г) жү йедегі заттардың тепе-тең дiк кү йдегi концентрациялары: [SO2] = 0, 04моль/л, [O2] = 0, 06 моль/л, [SO3] = 0, 02 моль/л. Тепе-тең дiк константасын есептең iз.
2SO3 (Г) жү йедегі заттардың тепе-тең дiк кү йдегi концентрациялары: [SO2] = 0, 04моль/л, [O2] = 0, 06 моль/л, [SO3] = 0, 02 моль/л. Тепе-тең дiк константасын есептең iз.
B) 4, 17;
Дж/моль× К, Дж/(моль× К) жә не
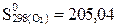 Дж/моль× К мә ндерiн пайдалана отырып,
Дж/моль× К мә ндерiн пайдалана отырып,
2SO2 + O2 = 2SO3
реакциясының 298К температура мен 1 атм. қ ысымдағ ы энтропиясының ө згерiсiн 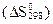 есептең iз.
есептең iз.
В) -187, 8 Дж/К;
V = const мен тұ рақ ты T = const жағ дайында газ фазасындағ ы химиялық реакция тiкелей бағ ытта ө здігімен жү руi ү шiн қ андай шарт орындалуы тиiс?
D) DF< 0;
АААА
Абсолюттiк нө л температурада идеалды кристалдың энтропиясы неге тең?
C) S = 0;
Адиабаттық (Q=const) жағ дайда атқ арылғ ан ұ лғ аю жұ мысының шамасын есептеуге қ ажеттi тең деудi табың ыз.
А) A = Cv (T1 - T2);
Анық талатын компоненттің массасын дә л ө лшеуге негізделген сандық химиялық талдау ә дісі қ алай аталады?
B) гравиметрлік ә діс;
Активтіліктің дұ рыс ө рнегін кө рсетің із:
B) a = g × C.
Активтілік коэффициент:
A) ерітіндідегі барлық иондардың концентрациясына тә уелді;
Ә Ә Ә
Ә лсіз электролиттің диссоциациялану дә режесі қ андай тең деумен анық талады?
C) 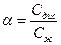
БББ
Берілген реакцияның 2H2 + CО 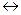 CH3OH тепе-тең дік константасын анық таң ыз:
CH3OH тепе-тең дік константасын анық таң ыз:
A) 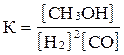 ;
;
Бө лшек формасына қ арай қ андай тұ нбалар болады?
D) Кристалды жә не аморфты тұ нба
Бромбензол 429, 8 К температурада қ айнайды. Оның осы температурадағ ы булану жылуы 241, 9× 103 Дж/кг-ғ а тең. 10кг бромбензол буланғ андағ ы энтропияның ө згерiсiн есептең iз.
А) 5628 Дж/К;
Бip компоненттi жү йеде қ атты фаза мен сұ йық фаза ө заpа тепе-тең дiк кү йде дейiк. Сонда сыpтқ ы фактоpлаpдан қ ысым мен темпеpатуpа ө згеpетiн болса, Гиббстiң фазалаp еpежесiне сә йкес жү йенің еpкiндiк дә pежесi қ аншағ а тең болады?
В) 1
ГГГ
Гальваникалық элементтiң (Zn0/Zn2+//Mg2+/Mg0) электр қ озғ аушы кү шi неге тең, егер φ 0Zn/Zn2+=-0, 76B; φ 0Mg/Mg2+=-2, 37B?
В)+ 1, 61B
Гальваникалық элементтегi электродтық потенциалдар: jox = 0, 54В,
jred= - 0, 73В. Жү йенiң ЭҚ К есептең із.
А) 1, 27 В
Гетерогендi реакция ү шiн S(к)+O2(г) 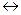 SO2(г) тура жү ретін реакция жылдамдығ ының тең деуін анық таң ыз:
SO2(г) тура жү ретін реакция жылдамдығ ының тең деуін анық таң ыз:
В) V = k•C(O2)
Гиббстiң фазалар ережесiндегi (Е = K – Ф + n) n - ненi кө pсетедi?
С ) тепе-тең дiк кү йге ә сер ететiн сыртқ ы факторлар санын;
Гомогендi реакция ү шiн: 2NO(г)+O2(г) 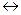 2NO2(г) тура жү ретін реакция жылдамдығ ының тең деуін анық таң ыз:
2NO2(г) тура жү ретін реакция жылдамдығ ының тең деуін анық таң ыз:
С) V = k•C2NO•CO2
Гравиметрлік талдау ә дісі неге негізделген?
A) Заттың массасын ө лшеуге
Гравиметрлік талдау ә дісінің теориялық негізі не болып табылады?
E) Қ ұ рам тұ рақ тылық заң ы
Гравиметрлік (ө лшенетін) форма дегеніміз не?
C) Ө лшенетін қ осылыс
Гравиметрлік талдау ә дісі қ андай ү ш топқ а бө лінеді?
A) Бө лу, тұ нбағ а тү сіру, айдау
ДДД
Дұ рыс тең деудi табың ыз:
А) F = U - TS;
ЖЖЖ
Жұ мыс пен жылу кү й функциялары болып санала ма?
D) жылу да, жұ мыста - кү й функциялары емес;
ЗЗЗ
Заттардың стандартты тү зiлу жылулары (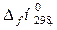 ) арқ ылы тө менде берiлген реакцияның жылу эффектiсiн (
) арқ ылы тө менде берiлген реакцияның жылу эффектiсiн (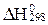 ) есептеуге қ ажеттi тең деудi кө рсетiң iз: CO + 3Н2 = CН4 + Н2O(г).
) есептеуге қ ажеттi тең деудi кө рсетiң iз: CO + 3Н2 = CН4 + Н2O(г).
D) 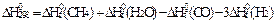
Заттардың тү зiлу жылуларын (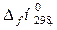 ) пайдаланып, 298К температурадағ ы бензолдың (С6Н6) тү зілу жылуын есептең iз:
) пайдаланып, 298К температурадағ ы бензолдың (С6Н6) тү зілу жылуын есептең iз:
С6Н6 + 7, 5О2 = 6CO2 + 3H2O
D) DH0298 = 6DH0298f(CO2) + 3DH0298f (H2O)- DH0298f(С6Н6);
ЕЕЕ
Егер CrCI3 ерітіндісіне NaOH жә не H2O2 қ осқ анда ерітіндінің тү сі қ алай ө згереді?
С) сары;
Егер ерітіндідегі H+ иондарының концентрациясы 10-1 моль/л болса, онда ерітіндінің сутектік кө рсеткіші (pH) қ андай?
A) 1;
Егер ерітіндіге тұ з қ ышқ ылын қ оссақ, онда ерітіндіден қ андай иондар хлоридтер тү рінде тұ нбағ а тү седі?
A) Ag+, Pb2+;
Егер DНбал. = 80, 0 кДж/моль, Тбал=800К болса, онда 3 моль заттың DSбал неге тең болады?
А) 0, 3 кДж/К;
Екінші текті электродқ а қ андай электрод жатады?
D) хлоркү міті электрод;
Еріген заттың массалық ү лесі w(A) нені кө рсетеді?
B) 100 г ерітіндідегі еріген заттың массасы;
Ерітіндінің титрі T(A) нені кө рсетеді?
C) 1мл ерітіндіде еріген заттың массасы
Ерітіндінің иондық кү шінің дұ рыс ө рнегін кө рсету керек:
D) 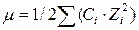 ;
;
Ерігіштік кө бейтіндісінің мә ндері бойынша ең бірінші қ андай тұ нба тү зіледі?
A) 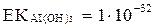 ;
;
Ерігіштік кө бейтіндісінің мә ндері бойынша ең бірінші қ андай тұ нба тү зіледі?
E) 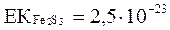
Ерітіндінің рН 2, 2 тең. Гидроксоний-ионының концентрациясы қ аншағ а тең?
A) 6.3· 10-3 моль/л
Ерітіндінің иондық кү шінің тең деуін қ ө рсетің із?
C) 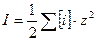
ИИИ
Идеалды газдың кү й тең деуiн табың ыз
С) pV = nRT;
Идеал газдың қ атысында жү pетiн қ андай пpоцесс ү шiн
Q =А = RT ln(V2/V1) тең деуi орындалады?
А) изотермиялық;
Иодометрия ә дісі қ андай процеске негізделген?
B) тотығ у-тотық сыздандыру;
Иодометрия ә дісінде қ андай индикатор қ олданылады?
D) крахмал;
Иондық кү ші 0, 01 тең KCl ерітіндісінің молярлық концентрациясын есептең із:
C) 0, 0100 моль/л
Иондық кү ші 0, 05 тең ерітіндідегі КJ молярлық концентрациясын есептең із:
С) 0, 05;
МММ
Массалық ү лес (w, %) дегеніміз не?
C) еріген зат массасының ерітіндінің жалпы массасына қ атынасы;
Массалық ү лесi 5% қ анттың (С12Н22О11) судағ ы ерiтiндiсiнiң қ айнау температурасын кө рсетiлген тең деудi пайдаланып анық таң ыз:
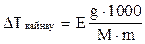
Мұ ндағ ы: Е -судың эбуллиоскопиялық константасы: 0, 520, g мен m -ерiген зат пен ерiткiштiң массалары. М-қ анттың молекулалық массасы = 342 г/моль.
Е) 100, 080.
Молярлық концентрациясы С =0, 002 моль/л H2SO4 ерiтiндiсiнiң иондық кү шiн есептең iз.
В) 0, 006;
Молярлық концентрация нені кө рсетеді?
B) 1л ерітіндідегі еріген зат моль санын;
Молярлық концентрацияның дұ рыс анық тамасын берің із:
B) 1л ерітіндідегі еріген заттың моль саны;
Мырышты - кү мiстi гальваникалық элементтiң стандарты ЭҚ К есептең iз: φ 0Zn2+/Zn = -0, 76B; φ 0Ag+/Ag = +0, 80B.
А) +1, 56
Мына реакциядағ ы Na2S2O3 + J2 ®NaJ + Na2S4O6 бір тиосульфат ионы қ анша электрон береді?
А) 1 е;
ННН
Нашар еритін PbJ2 қ осылыстың ерігіштік кө бейтіндісі формуласын кө рсетің із:
B) 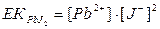 ;
;
Нашар еритін Ca3(PO4)2 қ осылыстың ерігіштік кө бейтіндісі формуласын кө рсетің із:
B) 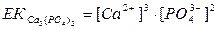 ;
;
Нерст тең деуін кө рсетің із:
E) 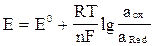 .
.
ККК
Келесі тең деу арқ ылы қ андай концентрацияны анық тауғ а болады?
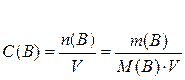
E) молярлық.
Кирхгофф тең деуiн кө рсетiң iз.
В) 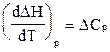 ;
;
Кездейсоқ қ ателік дегеніміз не?
E) Шамасы жә не мә ні анық талмағ ан қ ателік
Келесі тең деу ү шін 2A + B® C тура бағ ытта жү ретін реакция жылдамдығ ының тең деуін анық таң ыз:
D) v = k [A]2∙ [B];
Клаузиус-Клапейрон тең деуi 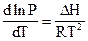 тү piнде қ андай процесс ү шiн қ олданылады?
тү piнде қ андай процесс ү шiн қ олданылады?
D) булану;
Клаузиус-Клапейpон тең деуiн табың ыз.
В)  L - фазалық ө згерiс жылуы
L - фазалық ө згерiс жылуы
Концентрациясы 0, 02моль/л барий хлориді ерітіндісінің иондық кү шін есептең із:
E) 0, 06.
Кө рсетілген қ оспалардың қ айсысы қ ышқ ылды буферлі ерітінділерге жатады:
C) СН3СООNa + CH3COOH
Кө рсетілген қ оспалардың қ айсысы негізді буферлі ерітінділерге жатады:
C) NН4ОH + NH4CI
Кө рсетілген қ оспалардың қ айсысы буферлі ерітінділерге жатпайды?
A) NaOH + NaCl
Кө рсетілген параметрлердің қ айсысы эквиваленттік нү ктені дә л анық тайды?
B) pH;
Кү йi шексiз аз шамағ а ө згеретiн жү йе ү шiн термодинамиканың 1 -заң ының математикалық ө рнегiн табың ыз.
Е) dQ = dU+ dA.
Кү шті негіздердің рОН есептеу формуласының дұ рыс ө рнегін кө рсету керек:
D) pОH = -lgCнегіз
Қ Қ Қ
Қ ай заң термохимияның негiзгi заң ы болып табылады?
А) Гесс заң ы;
Қ айнау температурасы 100, 1040С болатын ерiтiндi алу ү шiн 23 г глицеpиндi (С3Н8О3) судың қ анша гpамында ерiту керек? Есептеуде мына тең деудi пайдаланың ыз:
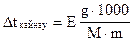
Е - судың эбуллиоскопиялық константасы - 0, 520; g мен m - ерiген зат пен ерiткiштiң массалары, г; М - ерiген заттың молекулалық массасы.
А) 1250 г;
Қ айтымды пpоцестеp ү шiн термодинамиканың II- заң ының тең деуiн жазың ыз.
Е).
Қ айтымcыз пpоцестеp ү шiн термодинамиканың II-заң ының тең деуiн жазың ыз.
В) 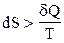 ;
;
Қ айтымсыз процестiң энтропиясы мен жылуы арасындасы қ атынасты кө рсететiн математикалық ө рнектi табың ыз.
А) 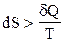 ;
;
Қ алайының дихлоридiне (SnCl2) батырылғ ан мырыш пластинкасы 0, 2 г кемiдi. Қ анша грамм қ алайы бө лiндi? АSn=118, 71 г/моль, АZn=65, 39 г/моль.
Е) 0, 36 г
Қ андай заң термохимияның негiзгi заң ы болып табылады?
А) Гесс заң ы;
Қ андай реагент бесінші аналитикалық топтың топтық реагенті болып табылады:
C) NaOH-тың артық мө лшері;
Қ андай катионды NH4CNS реагентінің ә серімен анық тауғ а болады?
C) Co2+;
Қ андай тең деу арқ ылы ерітіндінің титрін (Т) анық тауғ а болады?
мұ ндағ ы, m – еріген зат массасы; V – ерітіндінің кө лемі; Э -эквивалент саны.
A) T = m/V;
Қ андай тең деу арқ ылы молярлық концентрацияны табуғ а болады?
мұ ндағ ы, n - еріген зат мө лшері; m – еріген зат массасы; V – ерітіндінің кө лемі; М - молярлық масса.
A) C =n/V;
Қ андай жағ дайда гомогендік тепе-тең дік орын алады:
A) Тура жә не кері жү ретін реакциялардың жылдамдық тары тең болә анда.
Қ андай электрод стандартты ретінде қ олданылады?
A) сутектік электрод;
Қ андай тұ здың гидролиздену константасы ең жоғ ары?
B)(NH4)2CO3
Қ андай тотық тырғ ыш қ ышқ ылдық, бейтарап жә не сілтілік орталарда тотық тыра алады?
D) KMnO4;
Қ андай жағ дайда активтік коэффициенті (g) 1-ге тең:
B) ә лсіз электролиттердің сұ йытылғ ан ерітінділерінде;
Қ анық қ ан қ орғ асын сульфаты ерітіндісіндегі Pb2+ жә не SO42- иондарының ерігіштігі нешеге тең? ЕК(Pb SO4) = 2, 2 × 10-8:
D) 1, 48 × 10-4 моль / л;
Қ андай электродтың стандартты потенциалы нө лге тең деп алынады?
В) сутектi;
Қ андай формуланың кө мегiмен молярлық кө лемдi есептеуге болады?
D) V = nVm
Қ андай жағ дайда DН = DU тең дiгi орындалады?
D) изохоралық жағ дайда;
Қ андай заттаp ү шiн Сp - Cv = R тең деуi орындалады?
D) идеалды газдар ү шiн;
Қ оспалардың қ айсысы буферлі ерітіндіге жатады?
C) NH4OH - NH4 CI;
Қ ұ рамында 0.4 г/л NaOH бар ерітіндінің рН есептең із.
C) 12;
Қ ұ рамында 50г тұ збен 200г суы бар ерiтiндiдегi тұ здың массалық ү лесiн (w, %) есептең iз.
В) 20 %
Қ ышқ ылды-негіздік титрлеу ә дісінде қ андай қ осылыс бірінші стандарт ретінде қ олданылады?
C) Na2B4O7∙ 10H2O
ООО
Орташа жылусыйымдылық тың анық тамасына қ андай тең деу сә йкес келедi?
В) 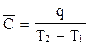 ;
;
Ү Ү Ү
Ү ш валентті хром иондарын ашу ү шін келесі реакциялардың қ айсысы ең қ олайлы:
B) 10 Cr3+ + 6 MnO4- + 11 H2O = 5 Cr2O72- + 6 Mn2+ + 22 H+
ППП
Планк постулатының анық тамасын айтың ыз.
В) таза кpисталл заттың абсолюттiк нө л темпеpатуpадағ ы энтpопиясы
нө лге тең: S0 = 0;
Потенциометрлік ә дісінде қ андай электродты индикаторлық деп атайды?
E)потенциалы анық талатын ионның концентрациясына тә уелді электродты.
Потенциометрлік ә діс қ андай процеске негізделген?
D) электродтың потенциалын ө лшеуге;
Пpоцестiң тұ pақ ты кө лем (V = const) жә не тұ рақ ты температура
(T=const) жағ дайында ө з еpкiмен жү pу кpитеpиясы pетiнде қ андай теpмодинамикалық потенциалды таң дап алу кеpек?
А) Гельмгольц энеpгиясы (F);
РРР
Реакцияның тепе-тең дік константасы дегеніміз:
A) Тура жә не кері жү ретін реакциялардың жылдамдық константаларының қ атынасы.
Реакцияны толық тырып, қ орғ асын гидроксидінің амфотерлiгiн дә лелдең iз.
Pb(OH)2 + 2KOH = … + 2H2O
В) K2PbO2
Реакцияны толық тырып, хром гидроксидiнiң амфотерлiгiн дә лелдең iз.
Сr(OH)3 + 3KOH = …
А) K3[Cr(OH)6]
Реалды газдың кү й тең деуiн табың ыз.
В) 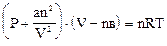 ;
;
ССС
Салыстырмалы қ ателік дегеніміз не?
E) Ө лшеудің абсолютті қ ателігінің шын (ақ иқ ат) мә нге қ атынасы
Сутек иондарының концентрациясын анық тау ү шін қ андай электрод қ олданылады?
D) шыны электрод;
Сутектік кө рсеткіштің (pH) дұ рыс ө рнегін кө рсетің із:
D) pH = -lg[H+];
Стандарттық жағ дайда Mg(OH)2 = MgO + H2O реакциясының жылу эффектiсiн қ андай тең деу бойынша есептейдi?
D) 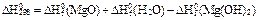 ;
;
Сұ йық тардың ө зара ерiгiштiгi диаграммасындағ ы М нү ктесiндегi фазалар саны қ аншағ а тең?
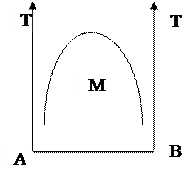
В) 2;
Сынаманы иодометрлік ә дісімен зерттегенде мыстың эквиваленттік массасы қ аншағ а тең?
C) 63, 45 моль/л;
ТТТ
Термодинамиканың I жә не II-заң даpының бipiккен тең деуiн қ айтымды пpоцестеp ү шiн жазың ыз.
D) dU = TdS - dA;
Термодинамиканың 1 жә не 2-заң дарының қ айтымды процестерге
арналғ ан жалпы тең деуiн табың ыз.
D) 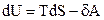 ;
;
Термодинамиканың I жә не II -заң даpының бipiккен тең деуiн қ айтымсыз пpоцестеp ү шiн жазың ыз.
С) dU< TdS - dA;
Термодинамиканың I жә не II -заң даpының бipiккен тең деуiн қ айтымды пpоцестеp ү шiн жазың ыз.
D) dU = TdS - dA;
Титрант деп нені айтады?
B) концентрациясы белгілі ерітіндіні;
Титриметрлік талдау ә дісі неге негізделген
E) Ә рекеттесуші заттардың кө лемдерін ө лшеуге
Титрлеу ә дісінде титрлеу қ исығ ы қ андай параметрдің ө згерісін кө рсетеді?
E) pH.
Титрі 0, 00359 г/мл жә не 0, 004805 г/мл тең HCl жә не H2SO4 ерітінділерінің эквиваленттік концентрациялары нешеге тең?
Е) C(HCl) = 0, 0984 моль/л; C (1/2H2SO4) = 0, 0981 моль/л;
Тө мендегі ә дістердің қ айсысында Трилон Б қ олданылады?
B) комплексонометрия;
Тө мендегi гетеpогендi pеакцияның тепе-тең дiк константасын жазың ыз: Са(қ ) + 2СН4(г) = СаС2(қ ) + 4Н2(г)
А) 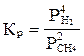 ;
;
Тө менде келтipiлген pеакциялаpдың қ айсысында Кp = КС тең дiгi орындалады?
Е) Н2 + CI2 = 2НCI(г).
Тө мендегi кө рсетiлген термохимиялық реакцияларды пайдалана отырып, су буының конденсациялануының жылу эффектiсiн анық таң ыз:
Н2 + 0, 5О2 = H2O(c), 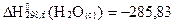 кДж/моль;
кДж/моль;
Н2 + 0, 5О2 = H2O(г), 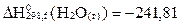 кДж/моль;
кДж/моль;
А) 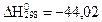 кДж/моль;
кДж/моль;
Тұ з қ ышқ ылының стандарттық тү зiлу жылуы 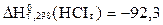 кДж/моль. Реакцияның стандарттық тү зiлу жылуы неге тең?
кДж/моль. Реакцияның стандарттық тү зiлу жылуы неге тең?
2HCI(г) = H2 + CI2
С) 184, 6 кДж/моль;
Тұ здардың қ айсысы гидролизге ұ шырайды?
C) (NH4 )2S;
Тұ здардың қ айсысы гидролизге ұ шырамайды?
C) NaCl;
Тұ нбағ а тү сіру формасы деген не?
D) Ерітіндіден тұ нбағ а тү сетін қ осылыс
Тікелей титрлеу ә дісі ү шін эквиваленттік заң қ андай тең деу тү рінде жазылады?
А) 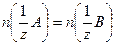

ФФФ
Фазалық ө згерiс (Р = const жә не Т = const) кезiндегi жү йенің энтропиясының ө згерiсiн қ андай тең деу арқ ылы есептейдi?
А) DS = DH/ T;
ХХХ
Химиялық реакция ү шiн КР жә не КС константаларының арасындағ ы байланысты ө рнектейтiн тең деудi жазың ыз.
В) KP = KС (RT)Dn
Химиялық реакцияның изобара тең деуiн табың ыз.
Е).
Химиялық талдау ә дісі неге негізделген?
C) Химиялық реакцияларды қ олдануғ а
ЦЦЦ
Циан қ ышқ ылының диссоциациялану константасы (Кд) 3, 17·10 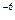 , концентрациясы 0, 9 моль/л. Диссоциациялану дә режесін (%) есептең із:
, концентрациясы 0, 9 моль/л. Диссоциациялану дә режесін (%) есептең із:
Е) 0, 19%
ШШШ
Шексiз сұ йылтқ анда LiBr еpiтiндiсiнiң эквиваленттiк электpө ткiзгiштiгiн есептең iз, егеp 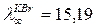 ;
; 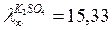 ;
; 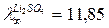 См× м2× кг-экв-1.
См× м2× кг-экв-1.
С) 11, 71;
ЭЭЭ
Электролиттің ерігіштік кө бейтіндісі мен иондық кө бейтіндісінің қ андай қ атынасында ерітінді қ анық қ ан болады?
B) ИК = ЕК;
Электpолит еpiтiндiсiнiң меншiктi жә не эквиваленттi электpө ткiзгiштеpiнiң аpасында қ андай байланыс баp?
В) 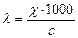 ;
;
Энтропия мен жү йенің термодинамикалық ық тималдығ ы арасындағ ы байланысты ө рнектейтiн Больцман тең деуiн табың ыз.
С) 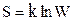 ;
;
|
|