
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Источника тока
|
|
Основой работы ХИТ является взаимодействие окислителя и восстановителя. Из курса химии известно, что в такой реакции восстановитель, окислитель, отдает электроны, а окислитель, восстанавливаясь, присоединяет электроны.
В качестве примера можно привести следующую электрохимическую систему элементов:
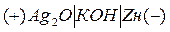
При нарушении электродов в электролит между ними устанавливается определенная разность электрических потенциалов называемая напряжением разомкнутой цепи (НРЦ).
Более отрицательным будет потенциал электрода с восстановителем, т.к. у него сильнее тенденция к отдаче (Zn) электронов.
Если соединить оба электрода между собой с помощью внешней проводящей цепи, то через нее при наличии напряжения разомкнутой цепи начнется переток электронов от отрицательного электрода к положительному, что равносильно прохождению электрического тока (рисунок 2.2).
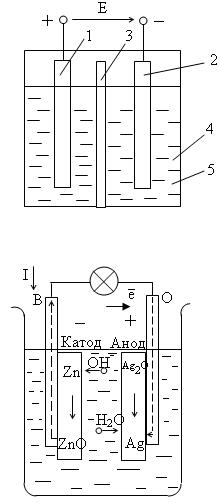
Рисунок 2.2 – Устройство химического источника тока:
1 – положительный электрод; 2 – отрицательный электрод;
3 – сепаратор; 4 – электролит; 5 – корпус
При этом будут протекать следующие процессы:
- на катоде – окисление цинка, цинк является восстановителем, т.е. атом цинка отдает свой электрон во внешнюю цепь, а свободная валентная связь идет на образование окиси цинка
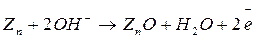 (2.1)
(2.1)
- на аноде - восстановление окиси серебра, который является окислителем, т.е. атом серебра принимает электроны и восстанавливается до валентно нейтрального серебра с образованием гидроокислительной группы ОН ˉ
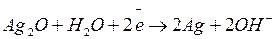 (2.2)
(2.2)
- в растворе электролита – движение гидроксид-ионов. (ОН) в растворе от окислителя к восстановителю (от анода к катоду)
- во внешней цепи – движение электронов от восстановителя к окислителю (от катода к аноду)
Суммируя реакции (2.1) и (2.2), получаем:
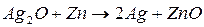 (2.3)
(2.3)
Таким образом, в результате протекания реакции (2.3) во внешней цепи генерируется постоянный электрический ток, т.е. химическая энергия реакции превращается в электрическую энергию.
|
|