
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Принципы ферментативного катализа. Трипсин
|
|
Ферменты – это белки, которые представляют собой высокоэффективные специфические катализаторы химических реакций, протекающих в живой клетке. Между ферментативным и химическим катализом принципиальных различий нет, химические механизмы реакций, лежащих в их основе, сходны. Для упрощения полагают, что с субстратом (веществом, которое превращается) взаимодействует не весь фермент, а только его активный центр – часть белковой молекулы, часто расположенная на поверхности фермента, и иногда имеющая форму щели или впадины. Активный центр состоит из зоны связывания субстрата и собственно зоны катализа. Зона связывания ответственна за выбор субстрата, его закрепление и правильную ориентацию относительно каталитического центра. При этом субстрат взаимодействует с ферментом за счёт разного типа нековалентных взаимодействий, а именно электростатических, Ван-дер-Ваальсовых, водородных и др. Функциональные группы аминокислот каталитического центра непосредственно участвуют в превращении субстрата.
1. а) За счёт изменения каких параметров реакции (температура, энергия активации, давление, путь реакции, объём) катализатор увеличивает скорость реакции? б) Для реакции разложения пероксида водорода рассчитайте, во сколько раз эффективность (увеличение скорости реакции) фермента каталазы больше, чем мелкодисперсной платины, если энергия активации:
без катализатора 18 ккал/моль
катализируемая платиной 12 ккал/моль
катализируемая ферментом 5, 6 ккал/моль
Уравнение Аррениуса для константы скорости реакции k = A ·exp(– E A/ RT). 1 кал = = 4, 184 Дж. Считать, что температура равна 300 К, R = 8, 31 Дж/(моль·К) и что для одной и той же реакции значение параметра А одинаково. Написать уравнение реакции.
Трипсин – это фермент, катализирующий гидролиз пептидных связей в белках. Он гидролизует связи, образованные карбоксильной группой аминокислот лизина (Lys) и аргинина (Arg). Дан небольшой пептид (запись по номенклатурным правилам осуществляется от N-конца пептида к его С-концу):
Arg-Ala-Leu-Gly-Lys-Ala-Arg-Gly-Gly-Lys
2. а) Напишите все пептиды, которые получаются из данного пептида при его частичном гидролизе трипсином. б) Как можно добиться того, чтобы гидролиз прошёл не полностью?
Лизин в боковом радикале содержит аминогруппу:

3. Если боковую аминогруппу лизина модифицировать, например ацилировать, будет ли трипсин гидролизовать связи в пептидах после модифицированного лизина? Почему?
4. Напишите продукты реакции аминокислоты лизина со следующими реагентами:
а) 2, 4-динитрофторбензол, б) R–C(O)H, в) малеиновый ангидрид (в щелочной среде),
г) C2H5–S–CO–CF3, д) KNCO, е) 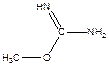
5. Сколько пептидов получится из пептида, указанного в вопросе 2, при модификации всех лизинов 2, 4-динитрофторбензолом и последующем неполном гидролизе трипсином?
6. Перечислите те аминокислоты из указанных ниже, которые могут входить в зону связывания трипсина. Обоснуйте своё предположение.

| 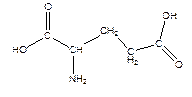
| 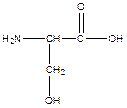
| 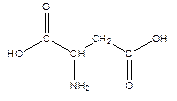
|
| Фенилаланин | Глутаминовая кислота | Серин | Аспарагиновая кислота |
7. Расшифруйте вещества A, B и С в цепочке превращений, если известно, что в составе вещества А w(C) = 71, 64 %, и оно даёт реакцию серебряного зеркала, реакция получения вещества А протекала в мягких условиях, а борную кислоту используют для стабилизации вещества В.
 ; ;
| 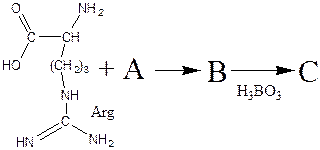
|
|
|