
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
На переднем крае химии
|
|
Что же представляет собой сейчас передний край химии? Главной задачей химии, по-прежнему, является разработка методов синтеза и создание новых веществ, препаратов и материалов. Число химически созданных соединений неуклонно растет. Молекулярная архитектура вновь синтезированных соединений бесконечно разнообразна и фантастически богата. Получены молекулы-ромбоиды (составляющие структуру одномерных металлов), протонные «губки» и «трубки» (молекулярно-организованные протононесущие резервуары и каналы), молекулярные тороиды, крауны (способные разделять катионы и анионы), гипервалентные радикалы, высокоспиновые молекулы (имеющие десятки неспаренных электронов в одной структуре), многопалубные полиароматические молекулы и т. д.
Крупным событием в химии стало освоение принципов звездообразного синтеза, при котором реагенты соединяются по фрактальному типу в гигантскую молекулу — дендример. Природа использовала этот принцип при формировании гликогена, амилопектина и некоторых других полисахаридов и белков. Прогнозируется, что полимерные дендримеры будут служить молекулярно-энергетическими антеннами, собирающими энергию солнечного излучения и преобразующими ее в фототок.
Настоящим сокровищем для химии стали фуллерены, с которыми связывают самые смелые и радужные прогнозы. Фуллерен – это молекула, состоящая из 60, 70 и более атомов углерода, связанных друг с другом так, что вся структура напоминает футбольный мяч (рис. 1). Оказывается, что и «чистые» фуллерены, и эндофуллерены (с внедренными в молекулу различными атомами и ионами) являются очень перспективными для микроэлектроники и для использования в составе сверхпроводников.

|
Рис.1 Фуллерен. Атомы углерода расположены в узлах решетки.
Крупным событием в современной химии стал синтез цилиндрических углеродныхнанотрубок (диаметром около 10 нм), которые построены по тому же принципу, что и фуллерены. Эти трубки характеризуются высокой растворимостью водорода, что позволяет использовать их в химических источниках тока. Такие нанотрубки можно укладывать, изгибать, резать, выпрямлять, организуя молекулярные электронные устройства.
Большой интерес к себе вызывает синтетическая химия на поверхности, которая исследует сверхтонкие объекты, мономолекулярные слои, мембраны, межфазные границы, адсорбционные слои реагентов на твердых телах, а также нанокластеры. Именно благодаря этим исследованиям появилось большое разнообразие источников света всех возможных цветов.
Новое «лицо» химии — это когерентная химия. Когерентность в химии проявляется в синхронизации реакции во времени, которая выражается в периодическом изменении скорости реакции и детектируется как осцилляции в выходе продуктов, эмиссии люминесценции, электрохимического тока и т. д. Когерентность в химии вносит в нее такие понятия, как волновой пакет, фаза, интерференция, бифуркация, фазовая турбулентность. В когерентной химии случайное, статистическое поведение молекул заменяется организованным, упорядоченным и синхронным: хаос становится порядком.
Первые наблюдения осциллирующих режимов химических реакций стали уже достоянием истории. Тогда осцилляции воспринимались скорее как экзотика, а не как химическая закономерность. Сегодня реакция Белоусова—Жаботинского, осцилляции рН и электрохимического потенциала в гетерогенных системах типа вода-масло, волновое горение и прочие — стали уже классикой.
Реакция Белоусова—Жаботинского — класс химических реакций, протекающих в колебательном режиме, при котором некоторые параметры реакции (цвет, концентрация компонентов, температура и др.) изменяются периодически, образуя сложную пространственно-временную структуру реакционной среды.В настоящее время под этим названием объединяется целый класс родственных химических систем, близких по механизму, но различающихся используемыми катализаторами (Ce3+, Mn2+ и комплексы Fe2+, Ru2+), органическими восстановителями (малоновая кислота, броммалоновая кислота, лимонная кислота, яблочная кислота и др.) и окислителями (броматы, иодаты и др.). При определенных условиях эти системы могут демонстрировать очень сложные формы поведения от регулярных периодических до хаотических колебаний и являются важным объектом исследования универсальных закономерностей нелинейных систем.
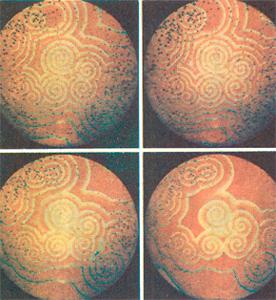
Рис.2 Некоторые конфигурации, возникающие при реакции Белоусова — Жаботинского в тонком слое в чашке Петри
Однако осознание того, что макроскопическая когерентность является фундаментальным свойством, пришло лишь недавно. Это связано с двумя обстоятельствами. Во-первых, в когерентных режимах можно ожидать увеличения выходов реакции, селективности процессов, самоочистки поверхностей от каталитических ядов и т. п. Во-вторых, интерес к химическим осцилляторам проявился вновь благодаря биохимическим осциллирующим процессам в нервных клетках, мышцах, митохондриях. Считается, что система химических осцилляторов является прообразом будущих моделей нейронных сетей.
Современная химия, раздвигая свои горизонты, активно вторгается в области, которые для «классической» химии не представляли интереса или были недостижимы. Особенно впечатляющие результаты достигнуты в области фемтохимии, которая развивается благодаря прогрессу в получении ультракоротких (10-14 - 10-15с) лазерных импульсов. Эти импульсы позволяют эффективно воздействовать на отдельные атомы и молекулы вещества, обеспечивая высочайшее пространственно-временное разрешение в управлении химическими превращениями. Мощные лазерные импульсы — великолепное средство генерации коротких ударных волн, стимулирующих экзотические химические превращения (например, синтез металлического водорода). Другим направлением создания экзотических условий является лазерное охлаждение до сверхнизких температур (10-4 - 10-6К), с помощью которого, например, удалось получить новое состояние вещества — кристаллический газ.
|
|