
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Методы изучения и диагностики наследственных патологий
|
|
В настоящем разделе представлена краткая характеристика генетико-эпидемиологического подхода в изучении наследственных болезней (генетический, близнецовый и популяционно-статистические методы), методы клинической диагностики (клиническое обследование и параклинические исследования), лабораторные методы диагностики (цитогенетические, биохимические, молекулярно-генетические) и методы моделирования наследственных болезней в эксперименте на животных.
Генетико-эпидемиологический подход в изучении роли наследственности в этиологии и патогенезе болезней человека предполагает совместное применение генеалогического, близнецового и популяционно-статистических методов.
Генеалогический метод - метод родословных, т.е. прослеживание болезни (или признака) в семье или роду с указанием типа родословных связей между членами родословной. Технически он складывается из двух этапов: составления родословной и генеалогического анализа. На первом этапе, используя специальные символы и правила, которые достаточно хорошо известны, составляется родословная.
Второй этап (генеалогический анализ) позволяет решать несколько задач. Во-первых, установить наследственный характер болезни или признака. Наследственную природу анализируемых болезней (признаков) предполагают, если они повторяются в родословной несколько раз (рис.32). Во-вторых, в случае доказательства наследственного характера болезни возможно установление типа наследования (аутосомно-до-минантный, аутосомно-рецессивный, Х-сцеплен-ный, Y-сцепленный, митохондриальный). Наконец, анализ родословных является обязательным условием успешного решения задач картирования генов на хромосомах, расшифровки механизмов взаимодействия генов, изучения интенсивности мутационного процесса. В клиничес-
Глава 4 / РОЛЬ НАСЛЕДСТВЕННОСТИ, КОНСТИТУЦИИ
кой практике генеалогический анализ составляет основу осуществления медико-генетического консультирования.
Близнецовый метод. Возможности его использования при изучении наследственной патологии определяются представлениями о происхождении близнецов: партнеры однозиготной (монозиготной) пары близнецов являются генетически тождественными, поскольку образуются из одной зиготы; партнеры двузиготной (ди-зиготной) пары близнецов образуются из двух разных зигот, а потому их фенотипическое сходство не больше, чем у братьев и сестер, родившихся в разное время; пары разнополых близнецов всегда являются двузиготными; внутри-парное различие, обнаруживаемое по какой-либо нормальной или патологической особенности

Рис. 32. Габсбургская губа, прослеженная на протяжении столетий: а - император Максимилиан IV (1459-1519); б - император Карл V - внук (а) (1500-1558); в - эрцгерцог Карл Тешенский (1771-1847); г - эрцгерцог Альбрехт - сын (в) (1817-1895). Strohmayer, Nova Acta Leopoldina, 5, 1937 (из книги К. Штерна «Основы генетики человека». М.: Медгиз, 1965. СМ)
И ВОЗРАСТА В ПАТОЛОГИИ 129
'• fara: i.4«M!
Конкордантность (%) близнецовых пар для разных групп болезней
Таблица 18
| Тип заболевания | Конкордантность близнецов | |
| монозиготные | дизиготные | |
| Болезни с наследственной предрасположенностью | 40-60 | 4-18 |
| Аутосомно-доминантные болезни | ||
| Аутосомно-рецессивные болезни |
однозиготных близнецов, должно быть отнесено за счет различий, обусловленных факторами среды.
Близнецовый метод считается особенно эффективным для доказательства наследственной предрасположенности к конкретным заболеваниям (мультифакториальные болезни и комплексные признаки). В этом случае применяют два варианта сравнения: сравнение конкордантности (совпадения фенотипов) моно- и дизиготных близнецов; сравнение конкордантности вместе и порознь выросших монозиготных близнецов. Обобщенные результаты использования близнецового метода для понимания природы разных заболеваний представлены в табл.18.
Популяционно-статистические методы. В отношении моногенных (менделевских) болезней эти методы в сравнительных исследованиях различных групп населения (популяций, этносов) позволяют выявить и оценить наиболее важные факторы популяционной динамики (отбор, дрейф генов, инбридинг, давление мутаций), определяющие пространственную изменчивость (территориальную гетерогенность в распространенности) наследственных болезней. Например, показано, что накопление некоторых рецессивных болезней среди финноязычного населения Финляндии обусловлено длительной изоляцией субпопуляций и дрейфом генов. Накопление редких патологических мутаций среди евреев-ашкена-зи объясняется эффектом «родоначальника» и дрейфом генов. Для популяций Средней Азии, а также некоторых арабских популяций показано, что главным фактором, детерминирующим груз и структуру наследственных болезней, накопление аутосомно-рецессивной патологии, являются неслучайные родственные браки (ассор-тативность браков).
Для других форм патологии - мультифакто-риальных заболеваний (болезней с наследственным предрасположением) популяционно-статистические методы, наряду с использованием со-
временных молекулярно-генетических методов, позволяют на основе анализа ассоциаций и сцепления генетических маркеров с конкретными признаками и болезнями в сравниваемых группах «больные - здоровые» («случай - контроль») в популяции, «больные - здоровые» в ядерных семьях, принадлежащих данной популяции, осуществлять поиск «генов-кандидатов» исследуемой болезни.
Методы, клинической диагностики. Наследственная патология имеет некоторые специфические характеристики. Для их выявления используется весь арсенал методов клинической диагностики (анамнез, осмотр, физические методы и пр.), параклинические исследования (общеклиническая диагностика с использованием современной аппаратуры исследования отдельных органов и систем - R-логические, ультразвуковые, томографические и т. д.). Главный смысл их применения (и выбор оптимальных клинических приемов) - обнаружить специфические черты болезни, указывающие на наследственный характер поражения. К ним относятся: семейный характер заболевания; хроническое, прогредиентное, рецидивирующее течение; врожденный характер заболевания; «резистентность» к наиболее распространенным методам терапии; наличие патогномоничных признаков (или их сочетаний), свойственных только данной форме наследственной патологии. Именно последнее, обусловленное тем, что большинство мутантных генов, вызывающих наследственные болезни, обладает плейотропным эффектом и вовлечением в процесс многих органов и систем (неспецифичных ассоциаций), определяет необходимость применения параклинических методов исследования. Так, при таких наследственных болезнях соединительной ткани, как синдром Элерса - Данлоса, Марфана, для которых характерно нарушение сосудистой стенки (особенно аорты), подвывих хрусталика, пролапс митрального клапана, патология суставов, по-
Часть I. ОБЩАЯ НОЗОЛОГИЯ
надобятся R-логические, ультразвуковые, офтальмоскопические и некоторые другие параклинические методы исследования. Однако окончательная диагностика и выявление более тонких генетических вариантов исследованной патологии осуществляются с применением специальных лабораторных методов диагностики.
Лабораторные методы диагностики. Лабораторная диагностика наследственных болезней (фено- или генотипирование индивидов) в основе своей может быть направлена на идентификацию одной из трех «ступеней» болезни. Во-первых, это выявление этиологической причины наследственной патологии, или характеристика генотипа, т.е. определение конкретной мутации у индивида (генной, хромосомной, геномной). Эти цели достигаются с помощью цитоге-нетических или молекулярно-генетических методов. Во-вторых, лабораторные методы позволяют регистрировать первичный продукт гена (биохимические, иммунологические методы). В-третьих, возможна регистрация специфических метаболитов измененного обмена, возникших в процессе реализации патологического действия мутации (биохимические, иммунологические, цитологические методы регистрации на уровне жидкостей - кровь, моча, секрет или клеток).
Цитогенетические методы. Они предназначены для изучения структуры хромосомного набора или отдельных хромосом. Объектом цито-генетических наблюдений могут быть делящиеся соматические, мейотические и интерфазные клетки. Чаще исследования выполняются на соматических клетках: наиболее удобный объект - культура лимфоцитов периферической крови, но также и культура клеток из кусочков кожи (фибробласты), костного мозга, эмбриональных тканей, хориона, клеток амниотической жидкости.
Специальным образом полученные препараты из культуры клеток затем окрашиваются. Все методы окраски препаратов можно разделить на три группы: простые, дифференциальные, флюоресцентные.
Простая окраска (метод окраски по Гимзе или в русскоязычной литературе - «рутинная окраска») используется для ориентировочного определения числовых аномалий кариотипа. Струк- гурвые хромосомные аномалии (делеции, транс- юкации, инверсии), выявленные при простой ок-
раске, должны быть идентифицированы с помощью дифференциальной окраски. Под этим методом понимают способность хромосом к избирательному окрашиванию по длине с фиксацией в виде чередования эу- и гетерохроматических районов (темные и светлые полосы).
Благодаря успехам в молекулярной генетике человека разработан принципиально новый метод изучения хромосом - метод флюоресцентной гибридизации in situ (FISH). Он основан на использовании однонитевого специфического участка ДНК («зонда»), специальным образом «помеченного» и способного, после присоединения к участку анализируемой хромосомы, присоединить флюоресцентные красители (красный, зеленый и другие цвета). С помощью люминесцентного микроскопа окрашенные хромосомы визуализируются на фоне неокрашенных. Метод позволяет расшифровать сложные хромосомные перестройки, а также локализовать ген.
Биохимические методы. Эти методы направлены на выявление биохимического фенотипа организма - от первичного продукта гена (полипептидной цепи) до конечных метаболитов в моче или поте. Поэтому существует огромное разнообразие методов. Но для целей диагностики наследственных болезней оправданными являются две биохимические стратегии, которые позволяют определить дальнейший ход обследования и выбор соответствующих биохимических методов и тестов: массовые и селективные программы первичной биохимической диагностики наследственных болезней.
Массовые просеивающие программы применяются в диагностике фенилкетонурии, врожденного гипотиреоза, адреногенитального синдрома, врожденных аномалий нервной трубки и болезни Дауна. Селективные диагностические программы предусматривают проверку, уточнение биохимических аномалий обмена для пациентов, у которых подозреваются генные болезни, используя простые качественные реакции или более точные методы (тонкослойная хроматография мочи и крови, газовая хроматография, флюорометрические методики и др.).
Молекулярно-генетические методы. Это большая и разнообразная группа методов, предназначенных для выявления вариаций в структуре исследуемого участка ДНК (аллеля, гена, региона хромосомы) вплоть до расшифровки первичной последовательности нуклеотидных осно-
" лава 4 / РОЛЬ НАСЛЕДСТВЕННОСТИ, КОНСТИТУЦИИ И ВОЗРАСТА В ПАТОЛОГИИ
Таблица 19 Подходы к ДНК-диагностике наследственных болезней
| Прямая диагностика мутаций | - Детекция крупных перестроек (мутаций) генов методами блот-гибридизации с исполь зованием ДНК-зондов; - выявление крупных и мелких делеций генов ПЦР-амплификацией отдельных фрагмен тов, в том числе мультиплексной ПЦР; - детекция внутригенных мутаций, изменяющих сайты узнавания определенных рестрик- таз (и вследствие этого - размер фрагментов, выявляемых блот-гибридизацией или ПЦР-амплификацией); - аллель-специфическая гибридизация (амплификация) с использованием олигонуклео- тидов, комплементарных нормальной или мутантной последовательности ДНК; - детекция конформационного полиморфизма одноцепочечной ДНК (single strand conformation polymorphism); - метод детекции ошибок спаривания (cleavage mismatch detection); - гетеродуплексный анализ фрагментов гена; - секвенирование гена или его фрагмента |
| Косвенная (непрямая) молекулярная диагностика | Анализ косегрегации генетических маркеров (микро- и минисателлиты, ПДРФ), сцепленных с патологическим геном, и болезни в семьях |
ваний. Все разнообразие подходов для идентификации генов или определенных фрагментов ДНК и их вариаций основывается на двух основных методических разработках - технологии блот-гибридизации и амплификации отдельных участков ДНК.
Общая схема блот-гибридизации по Саузерну представлена на рис. 33 (метод назван по имени
| Авторадиография |
Детекция флуоресцентной метки Рис. 33. Блот-гибридизация по Саузерну
доктора из Эдинбурга Эдмунда Саузерна, а английское blot означает промокать).
В основу методики амплификации положена полимеразная цепная реакция (ПЦР), которая позволяет в течение нескольких часов выделить и размножить определенный фрагмент ДНК в количестве, превышающем исходное в 10е раз. Такая высокая степень направленного обогащения значительно упрощает работу с минимальными количествами ДНК-образцов. Реакция высоко специфична и чувствительна, позволяет исследовать единичную копию гена в исходном материале.
В табл.19 приводятся другие методы геноти-пирования, основанные главным образом на этих же двух технологиях, а также обозначены подходы к ДНК-диагностике болезней (прямая и косвенная диагностика).
Методы моделирования. Как и в других разделах биологии и медицины, в генетике человека и медицинской генетике широко применяются методы моделирования. Они разделяются на две группы: биологические и математические.
Для изучения многих моногенных болезней человека используются животные, несущие мутации в гомологичных генах. Они являются удобными моделями для исследования молекулярных основ патогенеза и отработки оптимальных вариантов лечения. С этой целью во многих питомниках мира созданы и поддерживаются коллекции генетических линий животных (мышей, крыс, кроликов, собак и др.). Мировая коллекция мышей насчитывает несколько сотен линий с моногенно наследуемыми дефектами.
Часть I. ОБЩАЯ НОЗОЛОГИЯ
Для анализа экспрессии мутантных генов in: в оценки биологических свойств первично-• «иного продукта удобными оказались транс-юшые животные. Трансгенных животных получают искусственным введением (трансгеноз).гческого материала (фрагмент гена или иная последовательность ДНК) в оплодотворен-г- у. яйцеклетку или в ранние зародыши млеко-глтающих. Дальнейшее развитие технологий —. -нсгеноза позволило подойти к конструированию модельных генетических линий животных - направленному получению генетических в-лелей наследственных болезней путем введена сайт-специфических модификаций в геном ржиекопитающих, или «выбиванию» (вырезанию) переделенного гена, идентичного гену человека. Такие мыши, у которых экспериментально «вырезан» определенный ген из генома, называются нокаутяыми (от англ. knock out). На таких животных можно приближенно понять патогенез наследственной болезни и апробировать ме-тоды лечения.
Математическое моделирование применяют в тех случаях, когда сформулированные задачи не могут быть решены только путем анализа экспериментального материала или их решение математически оказывается более быстрым и точным, чем экспериментально. В области генетики популяций математическое моделирование позволяет, например, оценить удельный вес многочисленных факторов популяционной динамики |©гбор, мутации, дрейф генов, инбридинг, миграции) в формировании «груза» наследственной патологии. Изучение таких сложных процессов, как взаимодействие наследственных факторов и факторов среды в развитии признака, закономерностей функционирования генома человека как интегративной системы, взаимодействие генов («генные сети») при формировании физиологических свойств организма, становится предметом исследования биоинформатики (компьютерной геномики).
4.2. РОЛЬ КОНСТИТУЦИИ В ПАТОЛОГИИ
Среди факторов, играющих роль в этиологии болезней, определенное значение имеет конституция человека (лат. constitutio - строение), под которой подразумевается совокупность относи-
тельно устойчивых структурных и функциональных особенностей, оказывающих влияние на реактивность организма и его сопротивляемость к действию болезнетворных факторов.
Учение о конституции имеет многовековую историю. Поводом для его возникновения явилось стремление врачей выделить среди огромного количества людей, наделенных чрезвычайно разнообразными индивидуальными свойствами, какие-либо типовые структурные и функциональные особенности организма и установить их связь с развитием тех или иных заболеваний.
Основоположником учения о конституции и ее связи с развитием болезней явился Гиппократ, который различал людей с сухим и влажным; сильным и слабым; вялым и упругим типами конституции. Кроме того, он подразделял людей по темпераменту на сангвиников, холериков, флегматиков и меланхоликов. В 1-Й столетиях нашей эры учение о конституции организма получило дальнейшее развитие в трудах Галена, который ввел понятие о habitus, подразумевая под этим особенности телосложения, влияющие тем или иным образом на развитие болезней.
Основное развитие учение о конституции получило в XX столетии.
4.2.1. Классификация типов конституции
Сложным явилось создание классификации типов конституции. Единой классификации не существует. Предложено более 40 ее разновидностей, причем за основу классификации в большинстве случаев принимались особенности телосложения, такие как соотношение между ростом и весом, длиной туловища и конечностей, а также размеры и форма грудной клетки, степень развития мускулатуры и др. Значительно реже классификация типов конституции основывалась на функциональных особенностях нервной системы.
К. Сиго [Sigaud С, 1914] предложил выделять 4 типа конституции - дыхательный, пищеварительный, церебральный и мышечный, в зависимости от преимущественного развития той или иной системы организма (рис. 34). Дыхательный (респираторный) тип характеризуется длинной грудной клеткой с острым эпигаст-
Глава 4 / РОЛЬ НАСЛЕДСТВЕННОСТИ, КОНСТИТУЦИИ И ВОЗРАСТА В ПАТОЛОГИИ 133
ральным углом и умеренным развитием брюшных внутренностей; у пищеварительного (ди-гестивного) типа грудная клетка короткая, эпи-гастральный угол тупой, вместе с тем увеличены размеры живота, усиленно развит жевательный аппарат, имеется склонность к ожирению; для людей церебрального типа характерен большой череп с хорошо развитой лобной частью в сочетании с нежным тонким телосложением и короткими конечностями; мышечному (мускульному) типу конституции присуще усиленное развитие мускулатуры, пропорциональное телосложение, широкая грудная клетка. Согласно представлениям Сиго, формирование типа конституции происходит главным образом в детском возрасте и зависит от тренировки органов и систем организма.
Немецкий психиатр Э. Кречмер [Kretchmer Е., 1921] выделил три типа конституции - пикнический (пикник), лептосомный (астеник) и атлетический (атлет). Пикник характеризуется большой массой тела за счет избыточного отложения жира, короткой грудной клеткой, большим выступающим животом, длинным туловищем и сравнительно короткими конечностями. Астеник - высокий и тонкий, с длинными конечностями и относительно коротким туловищем, узкой грудной клеткой. Атлет - человек с хорошо развитой мускулатурой, с широкими грудной клеткой и плечами, узким тазом.
В. Шелдон [Sheldon W., 1940] взял за основу классификации степень развития дериватов зародышевых листков - эктодермы, эндодермы и мезодермы, и выделил соответственно 3 конституциональных типа: эндоморфный, эктоморфный
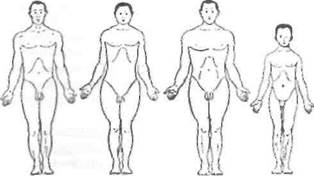
а б в г
Рис. 34. Типы конституции по Сиго: а ■ дыхательный, б - пищеварительный, в - мышечный, г - церебральный
и мезоморфный. Характеристика этих типов имеет сходство с конституциональными типами, выделенными Э. Кречмером: эндоморфный тип сходен с пикником, эктоморфный - с астеником, а мезоморфный - с атлетом. Эта классификация пользуется признанием на Западе.
В нашей стране наиболее популярна классификация М.В. Черноруцкого (1928), который выделил на основании особенностей телосложения два крайних типа - астеник и гиперстеник, и один промежуточный - нормостеник.
Астенический тип конституции характеризуется относительно коротким туловищем и длинными конечностями, узкой, плоской и сравнительно длинной грудной клеткой с острым эпигастральным углом, узкими плечами, тонкой длинной шеей, небольшим объемом живота; в целом продольные размеры значительно превалируют над поперечными. У людей с гиперсте-ническим типом конституции имеется обратное соотношение размеров тела по сравнению с астениками: относительно длинное туловище и короткие конечности, короткая шея, широкая короткая грудная клетка с увеличенным передне-задним размером, большой, часто выступающий вперед живот; в целом имеется нарастание поперечных размеров тела. Нормостеники характеризуются пропорциональным телосложением, широким плечевым поясом и выпуклой грудной клеткой, хорошим развитием мускулатуры. Заслугой М.В. Черноруцкого является то, что совместно со своими сотрудниками он изучил особенности обмена веществ и состояние некоторых внутренних органов у выделенных им конституциональных типов.
При сопоставлении различных классификаций можно отметить присутствие в большинстве их двух крайних вариантов: с одной стороны, тип с увеличенными продольными размерами тела, а с другой - люди с увеличенными поперечными размерами. Недостатком большинства классификаций является то, что в них не включены промежуточные (смешанные) типы конституции, к которым относится большинство людей.
Все перечисленные классификации типов конституции строились с учетом особенностей телосложения. Значительно реже в качестве основополагающих признаков использовались функциональные особенности организма. Н. Eppinger, L. Hess (1910) предложили классифицировать
Часть I. ОБЩАЯ НОЗОЛОГИЯ
— МЛ Чет-
| тип ко»: | ||
| Астеники | : в диссимиляциинад ассимилп цией. склонность к повышению основного обмена и алкалозу; ускоренная утилизация глюкозыпри сахарной нагрузке; содержание холестерина илипидов в крови в пределах нормы или снижено | брюшной полости, язвенной болезни, тяжелому течению туберкулеза легких, гипотонии, патологической аменорее |
| Гиперстеники | Преобладание процессов ассимиляции, склонность к понижению основного обмена и ацидозу; нарушение толерантности к глюкозе при сахарной нагрузке; повышенное содержание в крови липидов и холестерина | Предрасположенность к заболеваниям сердечно-сосудистой системы (атеросклерозу, инфаркту миокарда, гипертонии), сахарному диабету пожилых, ожирению, желчекаменной болезни |
| Нормостеники | Равновесие процессов ассимиляции и диссимиляции; показатели обмена веществ и физиологических процессов близки к средней норме | Предрасположенность к заболеваниям верхних дыхательных путей и опорно-двигательного аппарата |

|
конституциональные типы в зависимости от особенностей функционирования вегетативной нервной системы. Исходя из этого, они предложили подразделять всех людей на симпатикотони-ков и ваготоников. Эта классификация подверглась критике на том основании, что антагонизм между симпатической и парасимпатической системами проявляется не во всех отношениях.
И.П. Павлов (1925) выделил людей с различными типами высшей нервной деятельности на основе учета силы, подвижности и уравновешенности основных нервных процессов - возбуждения и торможения. Для их обозначения И.П. Павловым была использована предложенная Гиппократом классификация видов темперамента -сангвиник, холерик, флегматик и меланхолик. Сангвиник характеризуется сильным уравновешенным подвижным типом высшей нервной деятельности; холерик - сильным неуравновешенным подвижным; флегматик - сильным уравновешенным инертным и меланхолик - слабым типом высшей нервной деятельности (рис. 35).
4.2.2. Типы конституции и болезни
| Рис. 35. Типы высшей нервной деятельности. Неизвестный художник XIX в., из архива кафедры патофизиологии СГМУ Глава 4 / РОЛЬ НАСЛЕДСТВЕННОСТИ, КОНСТИТУЦИИ И ВОЗРАСТА В ПАТОЛОГИИ |
В настоящее время не вызывает сомнений, что люди определенного телосложения более склонны к некоторым заболеваниям [Харрисон Дж., 1968]. Это заключение основывается на многочисленных наблюдениях, сделанных М.В. Чер-норуцким и рядом других авторов. Связь между типами конституции и соматическими заболеваниями отражена в табл. 20.
Имеются данные о связи между типом конституции и психическими заболеваниями. Впервые на существование такой связи указал психиатр Э. Кречмер. Согласно его наблюдениям, среди больных шизофренией превалируют астеники, а среди больных маниакально-депрессивным психозом-пикники; кроме того, он и его соавторы утверждают, что развитие эпилепсии чаще имеет место у атлетов, чем у людей с другим типом конституции. В дальнейшем эти наблюдения получили некоторое подтверждение в исследованиях других авторов. В. Шелдон отметил, что истерия и депрессия чаще возникают у людей с мезоморфным или эндоморфным типом конституции, а тревожные состояния более характерны для лиц с эктоморфным типом телосложения.
Имеются также указания на более частое развитие неврозов у людей с сильным неуравновешенным и слабым типами высшей нервной деятельности.
Приведенные наблюдения указывают на то важность учета типа конституции для профилактики многих заболеваний. Своевременное проведение профилактических мероприятий может предупредить развитие болезни.
4.2.3. Факторы, влияющие на формирование типа конституции
В прошлом по этому вопросу высказывались противоположные суждения. Сторонники одного из них (Ю. Тандлер, Р. Миллер, О. Негели, П. Матес и др.) считали, что тип конституции всецело зависит от генотипических особенностей данного человека, т.е. является наследственно обусловленным и в течение всей жизни остается неизменным. Согласно мнению К. Сиго, тип конституции формируется в процессе жизни и зависит от вида деятельности, тренировки той или иной системы организма. А.А. Богомолец также рассматривал конституцию как совокупность фенотипических особенностей организма и считал, что в формировании типа конституции основную роль играют факторы внешней среды, условия жизни.
В настоящее время большинство ученых (П.Д. Горизонтов, А.Д. Адо, Н.Н. Зайко и др.) считают, что в формировании типа конституции главную роль играют наследственные особенности, но могут оказать влияние и факторы внешней
среды (инфекции и интоксикации, избыточное питание или голодание, гиповитаминозы, физическая нагрузка, занятие спортом и др.).
4.3. ЗНАЧЕНИЕ ВОЗРАСТА В ВОЗНИКНОВЕНИИ И РАЗВИТИИ БОЛЕЗНИ
В разные возрастные периоды люди по-разному реагируют на одни и те же воздействия. Каждому возрасту свойственны свои особенности и склонность к развитию определенных заболеваний. В онтогенезе человека (как, впрочем, и других млекопитающих) выделяют два периода: пренатальный и постнатальный. Последний, в свою очередь, делится на три периода: 1) период роста, когда формируются характерные для представителей данного вида морфологические и функциональные системы; 2) период зрелости, характеризуется завершившимся формированием морфологических и функциональных систем; 3) период старости, при котором происходит постепенное ослабление всех физиологических функций и затухание жизненного процесса.
4.3.1. Возраст и болезни
Ранний детский возраст характеризуется пониженной реактивностью и резистентностью (см. разд. 5.1), что обусловлено незаконченным развитием нервной, эндокринной и иммунной систем, незрелостью ферментных систем, несовершенством внешних и внутренних барьеров.
У новорожденного ребенка развитие корковых центров еще не закончено, возбудимость клеток коры низкая; регуляция метаболизма и функций организма осуществляется в основном подкорковыми центрами. Имеется слабость процессов внутреннего торможения и недостаточная способность к дифференцировке поступающих в ЦНС сигналов. Поэтому на воздействие различных безусловных раздражителей ребенок отвечает генерализованной реакцией. Болевая чувствительность у детей первого года жизни выражена слабо, что может затруднить своевременную постановку правильного диагноза при заболеваниях внутренних органов.
Дети первого года жизни, особенно новорожденные, характеризуются недостаточным проявлением защитно-приспособительных и компен-
Часть I. ОБЩАЯ НОЗОЛОГИЯ
саторных реакций. Из-за незаконченного формирования механизмов теплорегуляции у детей раннего возраста легко возникают состояния перегревания и переохлаждения. Недостаточность аппарата регуляции водно-солевого обмена является причиной частого развития состояний гипергидратации или обезвоживания (экси-коза) при нарушениях пищеварения, при гипервентиляционном синдроме и других заболеваниях.
Новорожденные тяжелее, чем взрослые, переносят кровопотерю. Вместе с тем дети первого года жизни проявляют большую устойчивость к гипоксии и не реагируют на нее учащением дыхания и пульса. Полностью эти реакции формируются к 6-7-му годам жизни.
Особенностью течения инфекционных заболеваний у детей является их недостаточная способность реагировать специфическими изменениями на действие возбудителя и, как следствие этого, имеют место стертость и искажение некоторых характерных симптомов, что может создать трудности для диагностики. Характерна также склонность к генерализованным реакциям и развитию осложнений, что связано с недостаточным проявлением защитных механизмов (незавершенность фагоцитоза, пониженное обезвреживание микробных токсинов, слабое развитие тканевых барьеров). Регионарные лимфатические узлы у ребенка начинают функционировать как барьер только после третьего месяца жизни. До этого срока микробы свободно проникают во внутреннюю среду организма. Вместе с тем в этом периоде жизни понижена чувствительность к возбудителям ряда инфекций (скарлатина, дифтерия, корь, краснуха, брюшной тиф) в связи с наличием пассивного иммунитета, обусловленного поступлением антител из организма матери через плаценту и с молоком при грудном вскармливании. Большую опасность для детей раннего возраста представляет гнойная инфекция, в особенности стафилококковая, а также вирусные инфекции, которые являются одной из частых причин заболевания пневмонией у детей [Носов С.Д., 1966].
Уровень иммуноглобулинов в крови новорожденного ребенка соответствует таковому у матери. Спустя '/а - 1 год после рождения восприимчивость к инфекционным заболеваниям повышается вследствие исчезновения из крови ребенка материнских антител. В то же время появляется способность к образованию собственных
антител и к развитию аллергических реакций, которые в период новорожденности не выражены. Но в целом объем антителообразования в течение первого года жизни недостаточный.
Одним из частых заболеваний у детей раннего возраста является пневмония. Ее развитию способствует недостаточное расправление легких при вдохе вследствие слабой экскурсии грудной клетки, ригидности стромы легких, частого образования ателектазов (т.е. спадения альвеол). Пневмония в большинстве случаев является ин-терстициальной и имеет генерализованный характер. Развитие пневмонии у новорожденных не сопровождается появлением выраженной одышки, что объясняется слабой возбудимостью дыхательного центра. Слабо выражен кашлевой рефлекс. К концу первого года жизни основные функции ребенка еще не устойчивы. Отсутствуют способность к ограничению патологического процесса, например воспаления, в пределах первично пораженного участка ткани, сохраняется склонность к диффузным реакциям и развитию сепсиса. Центральная нервная система ребенка легко истощаема.
В возрасте от 1 до 6-7 лет у детей постепенно совершенствуются все функции организма, ослабляется склонность к генерализованным реакциям при действии патогенных факторов, учащается заболеваемость детскими инфекциями, усиливаются проявления аллергии.
В период полового созревания (пубертантный период) может наблюдаться чрезмерная неустойчивость вегетативной нервной системы, психики и поведения. Возможны нарушения функции сердечно-сосудистой (ювенильная гипертония, акроцианоз) системы. В этом возрасте отмечается также повышенная частота развития туберкулеза и сахарного диабета. Может отклоняться от нормы процесс полового развития - он может быть ускорен или, напротив, замедлен.
По мере роста организма происходит развитие и совершенствование тканевых барьеров и иммунной системы, совершенствуется нервно-эндокринная регуляция. Поэтому у людей зрелого возраста реактивность и резистентность наиболее выражены. Отчетливо проявляются характерные особенности того или другого заболевания и различных патологических процессов. То же можно сказать в отношении развития защитно-приспособительных и компенсаторных реакций, что способствует благоприятному исходу болезни.
Глава 4 / РОЛЬ НАСЛЕДСТВЕННОСТИ, КОНСТИТУЦИИ И ВОЗРАСТА В ПАТОЛОГИИ
При продвижении от зрелого к пожилому и старческому возрасту снова происходит снижение реактивности и резистентности организма. У стариков уменьшается способность адаптироваться к воздействию изменяющихся физиологических и патогенных факторов внешней среды вследствие снижения метаболизма и функциональных резервов различных органов. Происходит угнетение физиологической, иммунологической и аллергической видов реактивности. Снижается противоинфекционный иммунитет. Особенно часто наблюдается развитие заболеваний, вызываемых вирусами, гноеродными микроорганизмами, что связано не только с недостаточным образованием антител, но и с ослаблением активности фагоцитов и повышением проницаемости тканевых барьеров. Снижается противоопухолевая резистентность. Частому развитию злокачественных опухолей в пожилом и старческом возрасте способствуют не только ослабление иммунного надзора, но и накопление с возрастом соматических мутаций, с которыми связывают опухолевую трансформацию клеток. Возрастает частота сердечно-сосудистой патологии вследствие развития атеросклероза и разба-лансированности в системе регуляции сосудистого тонуса. Повышается заболеваемость сахарным диабетом (диабет пожилых), деменцией; учащаются переломы костей в связи с развитием остеопороза.
Многие заболевания в этом возрасте имеют хроническое течение и нередко характеризуются недостаточно четкими проявлениями вследствие пониженной реактивности.
Таким образом, возрастная реактивность имеет существенное значение и должна обязательно учитываться при проведении профилактики, постановке диагноза и лечении пациентов любого возраста.
4.3.2. Старение
Старение является неотвратимой стадией развития всех живых существ, которым удалось прожить достаточно долго.
Процесс старения характеризуется развитием структурных и функциональных изменений, которые ограничивают способность организма поддерживать состояние гомеостаза при действии разнообразных стрессоров, вызывают снижение резистентности и обусловливают повышенную
заболеваемость людей пожилого и старческого возраста, что приводит в конце концов к полной утрате жизнеспособности.
Изменения в органах и тканях имеют генерализованный характер (табл.21), хотя и могут развиваться неодновременно.
Внешними проявлениями старения являются дистрофические изменения кожи и ее придатков: она истончается, становится морщинистой, уменьшается количество потовых и сальных желез, седеют и выпадают волосы. Разрушаются зубы. Происходит уменьшение массы тела за счет снижения объема мышечной и костной ткани и уменьшения количества внутриклеточной жидкости. Снижается плотность костной ткани, она разрыхляется (остеопороз). В связи с этим возрастает частота переломов. Нередко возникает кифоз вследствие сплющивания тел позвонков. Снижается мышечная сила. Проблемы, с которыми сталкиваются старые люди, - это ходьба и подъем по лестнице, самообслуживание, понижение ясности зрения и остроты слуха, недержание мочи, нарушение интеллектуальных функций. В основе указанных изменений лежат атрофические процессы в различных тканях, замещение клеток, выполняющих специфические функции, соединительной и жировой тканями, в мозге - глией. Этому способствуют генетические изменения в клетках и ухудшение кровоснабжения из-за прогрессирующего склероза сосудов и снижения функции сердца.
Проявления старения на уровне клеток. Как в стареющих фибробластах в культуре (in vitro), так и в клетках многих тканей при старении снижается скорость процессов транскрипции и трансляции на уровне генома, нарастает количество хромосомных мутаций; происходит увеличение количества лизосом, тогда как число митохондрий уменьшается. Понижается чувствительность клеток к различным ростовым факторам и гормонам, что связано с уменьшением числа рецепторов и нарушениями в пострецеп-торной передаче сигналов. Замедляется деградация белков, что связано со снижением активности внутриклеточных протеаз. Увеличивается количество структурно измененных белков. В клетках накапливается липофусцин.
В связи с пониженной доставкой кислорода, уменьшением в клетках количества митохондрий и нарушением синтеза дыхательных фер-
Часть I. ОБЩАЯ НОЗОЛОГИЯ
Изменения в различных системах организма в процессе старения
Таблица 21
| Вид системы | Характеристика возрастных изменений |
| Нервная система | Снижается в той или иной степени масса мозга, уменьшается количество нейронов в коре головного мозга, мозжечка и ядрах подкорки; увеличивается количество клеток глии. В нейронах изменяется активность ряда ферментов, что ведет к нарушению синтеза и обмена нейромедиа-торов, например дофамина. Снижаются память, скорость образования условных рефлексов, познавательные способности |
| Органы чувств | Снижается острота зрения и слуха, нарушаются обоняние и вкусовая чувствительность |
| Эндокринная система | Уменьшается секреция гормонов щитовидной, поджелудочной и половыми железами, корой надпочечников, аденогипофизом и эпифизом. Снижается реакция (1-клеток поджелудочной железы на гипергликемию и чувствительность тканей к действию инсулина |
| Сердечнососудистая система | Уменьшаются минутный обьем и сердечный индекс, максимальная частота сердечных сокращений, скорость кровотока. Повышаются периферическое сопротивление сосудов и системное артериальное давление. Нарастает риск развития ИБС в связи с повышенным содержанием в крови холестерина, ЛПНП и ЛПОНП |
| Органы дыхания | Снижаются максимальная вентиляция легких и ЖЕЛ, увеличивается остаточный объем воздуха в легких |
| Система органов пищеварения | Снижаются секреция пищеварительных ферментов и НО, объем пищеварительных соков, двигательная функция желудка и кишечника; иногда возникают нарушения глотания |
| Мочевыде- лительная система | Уменьшаются количество функционирующих нефронов, клубочковая фильтрация, концентрационная способность почек; замедляется выведение с мочой лекарственных препаратов; ночной диурез превалирует над дневным (никтурия). У женщин нередко возникает недержание мочи, у мужчин - затруднение мочеиспускания в связи с аденомой предстательной железы |
| Система гемостаза | Повышаются как прокоагулянтная, так и антикоагулянтная активность крови, од-нако последняя возрастает в меньшей степени, чем первая; снижается антиагрегационная способность стенок сосудов, что способствует образованию тромбов |
| Иммунная система | Ослабевает клеточный и гуморальный иммунитет. Возможно развитие иммунодефицита. Усиливаются аутоиммунные реакции |
ментов угнетаются процессы тканевого дыхания и окислительного фосфорилирования. В результате снижается синтез макроэргических соединений, что ограничивает функциональные резервы клеток и возможность синтеза различных веществ. Ослабляется работа энергозависимых мембранных насосов. В связи с этим в клетках повышается содержание Na+, Са2+ и СТ, а содержание калия, магния и фосфора снижается.
Обнаруживается рассогласованность в активности ферментов - у одних она понижена, у других повышена; к числу последних относятся моноаминооксидаза, сукцинатдегидрогеназа, альдолаза и др.
Следует иметь в виду, что при старении изменяются некоторые показатели, характеризующие метаболические процессы. В частности, возрастает средняя концентрация глюкозы в крови (до 6, 7 ммоль/л) и мочевины (до 8, 9 ммоль/ л), существенно снижается содержание альбуминов в плазме крови.
Биологическая наука, занимающаяся изучением изменений в организме при старении,
называется геронтологией. Одной из задач, которую она пытается разрешить, является выяснение причин и механизмов старения.
4.3.3. Механизмы старения
По поводу механизмов старения существовали многочисленные гипотезы, но большинство из них имеет в настоящее время только исторический интерес. Так, И.И. Мечников высказал предположение, что старение является следствием эндогенной интоксикации организма веществами, образующимися в кишечнике при гнилостном брожении. Чтобы затормозить процесс старения, он предложил употреблять в пищу как можно больше молочнокислых продуктов и вести правильный образ жизни. Некоторым подтверждением этой гипотезы является высокое содержание молочнокислых продуктов в диете кавказских долгожителей.
Существующие в настоящее время теории и гипотезы относительно механизмов старения можно подразделить на две группы. Теории, относящиеся к одной из этих групп, рассматрива-
Глава 4 / РОЛЬ НАСЛЕДСТВЕННОСТИ, КОНСТИТУЦИИ И ВОЗРАСТА В ПАТОЛОГИИ
ют старение как генетически запрограммированный процесс, который развивается в «плановом» порядке, подобно другим стадиям онтогенеза. Другие считают, что старение является результатом накапливающихся в течение жизни повреждений в геноме и других клеточных структурах.
Теории о связи старения с генетически запрограммированными процессами возникли на основе данных о запрограммированной смерти клеток на ранних стадиях онтогенеза. С нею связаны, например, рассасывание хвоста головастиков, исчезновение клеток между пальцами у развивающихся млекопитающих и птиц.
В пользу теории запрограммированного старения свидетельствует ряд наблюдений. Л. Хай-флик около 40 лет тому назад обнаружил, что фибробласты человеческого эмбриона, находясь в условиях клеточной культуры, могут совершить около 60 клеточных циклов, после чего прекращают деление. В дальнейшем они еще сохраняют жизнеспособность в течение ряда месяцев, но затем погибают. Пролиферативный потенциал клеток мог быть изменен только в слабой степени путем добавления в питательную среду глю-кокортикоидов и факторов роста. Фибробласты пациентов с ускоренным старением имели существенно укороченный срок жизни в культуре. Ограниченный срок жизни клеток в культуре был установлен не только для фибробластов, но и для других клеток от многих видов животных.
Одна из теорий программированного старения объясняет ограниченную способность клеток к делению существованием специфического гена, который экспрессируется после того, как клетка совершит соответствующее количество делений. Предполагается, что этот ген кодирует белок, который тормозит вступление клетки в фазу S митотического цикла, вследствие чего не происходит репликации ДНК. Так, установлено, что ингибитором пролиферации эндотелиальных клеток является интерлейкин-la (ИЛ-1а), при его инактивации способность этих клеток к делению резко возрастает. Но не доказано, что ИЛ-1а может тормозить пролиферацию фиброблас-тов или каких-либо других клеток.
Установлено, что при искусственном слиянии молодых и стареющих клеток образованные таким образом гибриды не размножаются, т.е. фенотип стареющих клеток является доминирую-
щим. Это объясняют присутствием в старых клетках ингибитора, блокирующего митотический цикл. Природа этого ингибитора не установлена. Предполагается, что это продукт антионкогена, т.е. не исключено, что механизмы, участвующие в ограничении опухолевого роста, могут быть ответственными и за старение.
Высказывается также предположение, что старение является результатом уменьшения передачи информации некоторых необходимых для жизни генов.
Среди теорий, рассматривающих старение как результат накопления в клетках различных повреждений в процессе их жизни, заслуживают особого внимания теория ошибок [Orgel L., 1963] и свободнорадикальная теория старения, предложенная Д. Харманом (1956) и Н.М. Эмануэлем (1958).
Согласно теории ошибок в результате аномалий в структуре генов или погрешностей в процессе транскрипции и трансляции генной информации может произойти синтез аномальных белков, которые утрачивают способность выполнять соответствующие функции. Это может иметь катастрофические последствия, если такие белки играют роль ферментов, участвующих в белковом синтезе, например РНК-полимераза, ами-ноацил-1-РНК-синтетаза, рибосомальные белки. В результате погрешности в синтезе белков будут продолжать накапливаться. В пользу этой теории свидетельствует нарастание количества аномальных белков в стареющих клетках, но полного подтверждения она не получила, так как попытки вызвать преждевременное старение клеток посредством искусственного усиления продукции аномальных белков пока не увенчались успехом.
Согласно свободнорадикальной теории, повреждение генома и других клеточных структур в процессе старения происходит в основном под действием свободных радикалов кислорода, которые образуются при тканевом дыхании в качестве его побочного продукта. Большая их часть подвергается в клетках обезвреживанию с помощью системы антиоксидантов, но некоторые сохраняют активность и взаимодействуют с различными внутриклеточными структурами, вызывают мутации, стимулируют перекисное окисление липидов, нарушают структуру и функцию клеточных мембран. Полагают, что под действием кислородных радикалов в первую очередь
Часть I. ОБЩАЯ НОЗОЛОГИЯ
повреждается ДНК митохондрий, так как она является менее защищенной, чем ядерная, из-за отсутствия в митохондриях гистонов и ферментов, осуществляющих репарацию поврежденных участков ДНК. Кроме того, именно в митохондриях образуется наибольшее количество радикалов кислорода в связи с утечкой электронов из дыхательной цепи. Во многих тканях старых индивидуумов были обнаружены различные виды мутаций митохондриальной ДНК (точко-вые мутации, делеции, дупликации).
Повреждения митохондриальной ДНК сопровождаются нарушением синтеза дыхательных ферментов. В результате снижается образование макроэргов, необходимых для работы мембранных насосов, выполнения специфических функций и поддержания внутриклеточного гомеоста-за, что завершается гибелью клетки. Справедливость этой гипотезы подтверждается наблюдениями, свидетельствующими о снижении функции митохондрий в процессе старения. Установлено, что с возрастом в клетках снижается мощность системы антиоксидантов и нарушается равновесие между про- и антиоксидантами. На основе всего этого сложилось мнение, что оксидантный стресс играет важную роль в процессах старения.
Предполагается также, что возрастные нарушения функции клеток в какой-то степени связаны с прогрессирующим накоплением в их цитоплазме и ядре пигмента липофусцина, который образуется путем неферментного гликози-лирования долгоживущих белков и нуклеиновых кислот. Присоединившиеся к макромолекулам сахара могут окисляться и образовывать массивные перекрестные связи между белками, ли-пидами и нуклеиновыми кислотами, что сопровождается нарушением их функции.
Можно предположить, что максимальный срок жизни, присущий тому или другому виду
живых существ, запрограммирован в геноме клеток, но под действием оксидативного стресса и других повреждений он может в той или другой степени укорачиваться.
На уровне целого организма возрастные изменения в различных тканях и органах не являются равнозначными в смысле их влияния на продолжительность жизни. Главную роль играют возрастные изменения функции регулятор-ных систем (в особенности гипоталамуса), сердечно-сосудистой системы и других жизненно важных органов. Наиболее частыми причинами, укорачивающими срок жизни, являются развитие злокачественных опухолей и заболевания сердца и сосудов.
На продолжительность жизни оказывают влияние генетические факторы, степень сохранения интеллектуальной деятельности, выраженность инстинкта самосохранения, способность организма перестраиваться в зависимости от условий жизни, склонность к развитию атеросклероза в жизненно важных органах [Franke H., 1973].
Наблюдения, проведенные на животных (главным образом, на грызунах), свидетельствуют о том, что положительное влияние на продолжительность жизни оказывает качественно полноценное, но количественно ограниченное питание, в особенности в первую половину жизни.
На продолжительность жизни, по-видимому, оказывает влияние функция эпифиза. Удаление его у крыс приводит к уменьшению продолжительности жизни, а введение животным пептидного экстракта эпифиза сопровождается противоположным эффектом.
Существует особый раздел медицины - гериатрия, которая ставит своей целью оказание медицинской помощи пожилым и старым людям, основываясь на знании особенностей физиологических и патологических процессов в позднем периоде жизни.
Глава 4 / РОЛЬ НАСЛЕДСТВЕННОСТИ, КОНСТИТУЦИ
И ВОЗРАСТА В ПАТОЛОГИИ 1
|
|