
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Кинетика массопередачи
|
|
ЛЕКЦИЯ 12
ОСНОВЫ МАССОПЕРЕДАЧИ
ОБЩИЕ СВЕДЕНИЯ
Массопередача имеет место в процессах абсорбции, перегонки и ректификации, экстракции и выщелачивания, сушки, адсорбции, кристаллизации и др.
При абсорбции происходит селективное поглощение газов или паров жидкими поглотителями — абсорбентами, т. е. имеет место переход вещества из газовой или паровой фазы в жидкую.
При перегонке и ректификации жидкая смесь разделяется на составляющие компоненты. Происходит переход веществ из жидкой фазы в паровую и из паровой в жидкую.
При экстракции происходит извлечение одного или нескольких веществ из растворов или твердых веществ с помощью растворителей. При экстракции в системе жидкость - жидкость имеет место переход вещества из одной жидкой фазы в другую жидкую фазу.
Процесс извлечения веществ из твердого тела с помощью растворителя называют выщелачиванием. При выщелачивании вещество переходит из твердой фазы в жидкую.
При адсорбции происходит избирательное поглощение газов, паров или растворенных в жидкостях веществ твердым поглотителем — адсорбентом, способным поглощать один или несколько компонентов из их смеси. Процесс используется во многих производствах, где из смеси газов, паров или растворенных веществ необходимо извлечь тот или иной компонент. При адсорбции вещества переходят из газовой или жидкой фазы в твердую.
Сушка - это удаление влаги из твердых или жидких влажных материалов путем ее испарения. В этом процессе имеет место переход влаги из твердого влажного материала в паровую или газовую фазу.
При кристаллизации из жидкой фазы выделяется вещество в виде кристаллов. При этом происходит переход вещества из жидкой фазы в твердую в результате возникновения и роста кристаллов в растворе.
КИНЕТИКА МАССОПЕРЕДАЧИ
Массопередача — процесс перехода вещества (или нескольких веществ) из одной фазы в другую в направлении достижения равновесия.
В массообмене участвуют, как минимум, три вещества: распределяющее вещество (или вещества), составляющее первую фазу; распределяющее вещество (или вещества), составляющее вторую фазу; распределяемое вещество (или вещества), которое переходит из одной фазы в другую.
Обозначим первую фазу 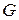 , вторую -
, вторую - 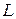 , а распределяемое вещество — М. Все массообменные процессы обратимы, поэтому распределяемое вещество может переходить из фазы
, а распределяемое вещество — М. Все массообменные процессы обратимы, поэтому распределяемое вещество может переходить из фазы 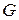 в фазу
в фазу 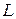 и наоборот в зависимости от концентрации вещества в фазах.
и наоборот в зависимости от концентрации вещества в фазах.
Пусть распределяемое вещество находится первоначально только в фазе 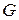 и имеет концентрацию
и имеет концентрацию 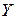 . В фазе
. В фазе 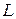 в начальный момент распределяемое вещество отсутствует, т. е. концентрация его в этой фазе
в начальный момент распределяемое вещество отсутствует, т. е. концентрация его в этой фазе 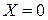 .
.
Если распределяющие фазы привести в соприкосновение друг с другом, начинается переход распределяемого вещества из фазы 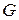 в фазу
в фазу 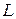 и с появлением вещества М в фазе
и с появлением вещества М в фазе 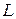 начинается обратный переход его из фазы
начинается обратный переход его из фазы 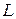 в фазу
в фазу 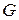 . До некоторого момента времени число частиц распределяемого вещества М, переходящих в единицу времени из фазы
. До некоторого момента времени число частиц распределяемого вещества М, переходящих в единицу времени из фазы 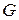 в фазу
в фазу 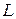 , больше, чем число частиц, переходящих из фазы
, больше, чем число частиц, переходящих из фазы 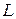 в фазу
в фазу 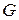 . Однако конечным результатом является переход вещества М из фазы
. Однако конечным результатом является переход вещества М из фазы 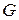 в фазу
в фазу 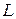 . По истечении определенного времени скорости прямого и обратного перехода вещества М в фазах
. По истечении определенного времени скорости прямого и обратного перехода вещества М в фазах 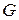 и
и 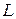 становятся одинаковыми. Такое состояние системы называется равновесным. При равновесии устанавливается строго определенная зависимость между концентрациями распределяемого вещества в фазах. Такие концентрации называют равновесными.
становятся одинаковыми. Такое состояние системы называется равновесным. При равновесии устанавливается строго определенная зависимость между концентрациями распределяемого вещества в фазах. Такие концентрации называют равновесными.
При равновесии каждой концентрации 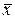 соответствует равновесная концентрация
соответствует равновесная концентрация  , и наоборот, каждой концентрации
, и наоборот, каждой концентрации 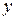 соответствует определенная равновесная концентрация
соответствует определенная равновесная концентрация 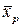 .
.
В условиях равновесия существуют определенные в каждом конкретном случае зависимости между концентрациями:
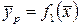 ;
; 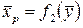 . (12.1)
. (12.1)
Эти зависимости определяются экспериментально и называются равновесными зависимостями.
Равновесные зависимости изображаются графически кривой или в частном случае прямой линией. На рис. 12.1 показана зависимость равновесной концентрации у компонента в газовой фазе 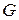 от его концентрации
от его концентрации  в жидкой фазе
в жидкой фазе 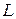 при постоянных давлении и температуре.
при постоянных давлении и температуре.
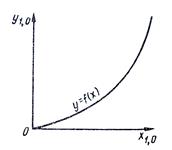
Рис. 12.1 Диаграмма равновесия при p=const и t=const
Отношение концентраций компонента в фазах в условиях равновесия 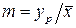 называется коэффициентом распределения.
называется коэффициентом распределения.
Коэффициент распределения геометрически выражает тангенс угла наклона линии равновесия. В случае кривой линии равновесия коэффициент распределения является переменной величиной.
Конкретный вид законов равновесия применительно к различным процессам массопередачи будет рассматриваться в соответствующих главах.
Равновесные зависимости позволяют определить не только направление процесса, но и скорость перехода распределяемого вещества из одной фазы в другую.
Разность между фактической и равновесной концентрациями, характеризующая степень недостижения равновесия, является движущей силой массообменных процессов.
Расчет движущих сил и коэффициентов скорости массообменных процессов составляет кинетику массопередачи.
Основные уравнения массопередачи могут быть получены из общего уравнения кинетики. Согласно этому уравнению скорость массообменных процессов прямо пропорциональна движущей силе процесса и обратно пропорциональна диффузионному (массообменному) сопротивлению.
Обозначив величину, обратную диффузионному сопротивлению, через 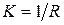 (где
(где 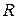 - диффузионное, или массообменное, сопротивление), запишем
- диффузионное, или массообменное, сопротивление), запишем
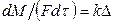 , (12.2)
, (12.2)
где: М – количество вещества, перешедшего из одной фазы в другую; F – площадь поверхности массопередачи; τ – продолжительность процесса; k – коэффициент скорости процесса, называемый в теории массопередачи; Δ – движущая сила.
Нетрудно видеть, что 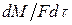 является скоростью массопередачи, отнесенной к единице контакта фаз.
является скоростью массопередачи, отнесенной к единице контакта фаз.
Если 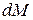 отнесено к единице времени, имеем
отнесено к единице времени, имеем
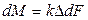 . (12.3)
. (12.3)
При 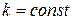 для всей поверхности массообмена
для всей поверхности массообмена
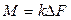 . (12.4)
. (12.4)
Уравнения (12.3) и (12.4) называют основными уравнениями массопередачи. Согласно этим уравнениям количество вещества, перенесенного из ядра одной фазы в ядро другой фазы, пропорционально разности его концентраций в ядрах фаз, площади поверхности фазового контакта и продолжительности процесса.
Коэффициент массопередачи показывает, какое количество вещества переходит из одной фазы в другую в единицу времени через единицу поверхности фазового контакта при движущей силе, равной единице.
Коэффициенты массопередачи в зависимости от единиц, в которых выражены движущая сила и количество распределяемого вещества, могут выражаться в м/с, кг/(ед. дв. силы 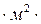 с), кмоль/ (ед. дв. силы
с), кмоль/ (ед. дв. силы 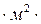 с).
с).
|
|