
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Теоретическое введение. Экспериментально определить значения средней теплоемкости воздуха в диапазоне изменения температур от t1 до t2
|
|
Цель работы
Экспериментально определить значения средней теплоемкости воздуха в диапазоне изменения температур от t 1 до t 2, установить зависимость теплоемкости воздуха от температуры.
Содержание работы
1. Определить мощность, затрачиваемую на нагрев газа от t 1
до t 2.
2. Зафиксировать значения расхода воздуха в заданном интервале времени.
3. Рассчитать количество теплоты, которую воспринимает газ от нагревательной спирали.
4. Рассчитать величину средней массовой с объемной с´ и мольной μ с теплоемкости, установить влияние температуры на теплоемкость.
Указания по подготовке к лабораторной работе
1. Проработать раздел курса “Теплоемкость” по рекомендуемой литературе.
2. Ознакомиться с настоящим методическим пособием.
3. Подготовить протоколы лабораторной работы, включив необходимый теоретический материал, относящийся к данной работе (расчетные формулы, схемы, графики).
Теоретическое введение
Теплоемкость - важнейшая теплофизическая величина, которая прямо или косвенно входит во все теплотехнические расчеты.
Теплоемкость характеризует теплофизические свойства вещества и зависит от молекулярной массы газа μ, температуры t, давления р, числа степеней свободы молекулы i, от процесса, в котором подводится или отводится теплота р = сопst, v = сопst. Наиболее существенно теплоемкость зависит от молекулярной массы газа μ. Так, например, теплоемкость для некоторых газов и твердых веществ составляет
| Вещество | Молекулярная масса, кг/кмоль | Теплоёмкость, кДж/(кг К) |
| Дерево | 2, 4 | |
| Сталь | 0, 5 | |
| Воздух | 28, 97 | |
| Вода (р =0, 1Мпа, t = 4оС) | 1, 19 | |
| Вода (р =18Мпа, t =300оС) | ||
| Водород, Н2 |
Таким образом, чем меньше μ, тем меньше вещества содержится в одном киломоле и тем больше нужно подвести теплоты, чтобы изменить температуру газа на 1 К. Вот почему водород является более эффективным охладителем, чем, например, воздух.
Численно теплоемкость определяется как количество теплоты, которое необходимо подвести к 1 кг (или 1 м 3), вещества чтобы изменить его температуру на 1 К.
Так как количество подведенной теплоты dq зависит от характера процесса, то и теплоемкость так же зависит от характера процесса. Одна и та же система в разных термодинамических процессах обладает различными теплоемкостями - cp, cv, cn. Наибольшее практическое значение имеют cp и cv.
По молекулярно-кинематической теории газов (МКТ) для заданного процесса теплоемкость зависит только от молекулярной массы. Например, теплоемкость cp и cv можно определить как
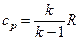 ;
; 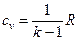 .
.
Для воздуха (k = 1, 4; R = 0, 287 кДж /(кг · К))
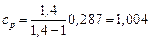 кДж/кг
кДж/кг
Для заданного идеального газа теплоемкость зависит только от температуры, т.е.
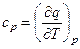 ;
; 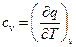 ;
; 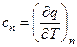 .
.
Теплоемкостью тела в данном процессе называется отношение теплоты dq, полученного телом при бесконечно малом изменении его состояния к изменению температуры тела на dt
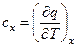 .
.
|
|