
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
ЯМР и ЭПР исследования.
|
|
Наиболее полные сведения об агрегатном состоянии липидных бислоев дают методы радиоспектроскопии ЭПР и ЯМР.
Электронный парамагнитный резонанс – это явление резкого возрастания поглощения энергии электромагнитной волны системой парамагнитных частиц (электронов с некомпенсированными спинами), помещенных во внешнее магнитное поле при резонансной частоте волны. Использование ЭПР заключается в исследовании спектров ЭПР. Спектром ЭПР называется зависимость мощности поглощения электромагнитной волны от величины магнитной индукции внешнего поля. Чем сильнее взаимодействие между атомами и молекулами образца, тем спектры ЭПР шире. Чем слабее взаимодействие между частицами (подвижность молекул больше), тем уже спектр ЭПР. По ширине спектров ЭПР можно судить о подвижности молекул веществ.
Так как молекулы фосфолипидов диамагнитные, для ЭПР-исследований биомембран используются спин-зонды и спин-метки – молекулы или молекулярные группы с неспаренными электронами.
Парамагнитные спин-зонды вводятся в липидную мембрану, спектры поглощения спин-зондами электромагнитной волны дают информацию о свойствах липидного окружения, в частности о подвижности липидных молекул в мембране. Этот метод обладает существенным недостатком – внесение в биологический объект чужеродных молекул-зондов может изменять структуру объекта. От этого недостатка свободен метод ЯМР.
Ядерный магнитный резонанс – это явление резкого возрастания поглощения энергии электромагнитной волны системой атомных ядер, обладающих магнитным моментом, помещенных во внешнее магнитное поле при резонансной частоте волны.
Как и в случае ЭПР, спектры ЯМР тем шире, чем больше вязкость и меньше молекулярная подвижность исследуемого объекта.
2 Люминесценция и ее виды. Излучение света происходит не только в результате нагревания тел, но и при других явлениях. Например, при электрическом разряде в газах, некоторых химических процессах (гниение органических веществ, окисление фосфора) и т.д. Наблюдаются свечение светлячков и морских микроорганизмов. Можно вызвать вторичное видимое свечение некоторых веществ под действием ультрафиолетового излучения и т.п. Все виды самосвечения, кроме свечения нагретых тел, называют холодным свечением или люминесценцией. Тепловое излучение является универсальным свойством тел и при соответствующих условиях становятся равновесным. Люминесценция является избирательным свойством тел, хотя весьма распространенным, причем излучение не может принять равновесный характер. Люминесценция прекращается, как только будет израсходована энергия того процесса, который ее вызывает. Поэтому говорят, что при люминесценции тело высвечивает фотоны. Люминесценция происходит одновременно с тепловым излучением и независимо от него, хотя температура тела может влиять на интенсивность люминесценции Люминесценция, как и тепловое излучение, происходит в результате сообщения атому дополнительной энергии, в связи, с чем он переходит в возбужденное состояние, при возвращении в основное состояние происходит излучение фотона. Однако распределение при этом возбужденных атомов по энергетическим уровням различается. При тепловом возбуждении атомы занимают последовательно все энергетические уровни, соответствующие температуре тела, при этом на более низких уровнях находится наибольшее число атомов, которые на более высоких уровнях убывают по экспоненциальной зависимости. При люминесценции это правило не соблюдается, и на определенных более высоких энергетических уровнях может находиться значительно большее число атомов, чем на нижележащих (“ инверсная заселенность уровней ”)Люминесценцию классифицируют: А) по природе, вызывающих возбуждения атомов и молекул, Б) по длительности послесвечения, В) по происходящим при возбуждении внутриатомным процессам.Например, биолюминесценцией называют свечение, наблюдаемое в живых организмах (грибы, бактерии, насекомые); электролюминесценцией называют свечение газов при электрическом разряде; катодолюминесценцией - свечение, возбуждаемое ударами электронов (например, на экранах электроннолучевых трубок); фотолюминесценцией – свечение, возникающее под действием ультрафиолетового излучения; рентгенолюминесценцией – свечение под действием рентгеновских лучей.
В зависимости от длительности послесвечения различают флуоресценцию и фосфоресценцию. Свечение, которое прекращается одновременно с прекращением возбуждения, называют флуоресценцией. Если послесвечение продолжается не менее 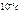 (во многих случаях минуты и даже часы), то такое свечение называется фосфоресценцией. Вещества с особенно длительным послесвечением называются фосфорами.
(во многих случаях минуты и даже часы), то такое свечение называется фосфоресценцией. Вещества с особенно длительным послесвечением называются фосфорами.
3 Течение. жидкости по горизонтальной трубе, Закон Пуазейля.
Если по горизонтальной трубе постоянного сечения будет протекать жидкость реальная жидкость, для которой нельзя пренебречь силами вязкого трения, то давление в трубе не будет постоянным, произойдет перераспределение давления, которое будет существенно зависеть от свойств жидкости. В реальной жидкости различные слои жидкости, имеющие разные скорости будут взаимодействовать между собой, то есть между слоями жидкости благодаря межмолекулярным взаимодействиям будут возникать силы вязкого трения − более медленный слой будет тормозить более быстрый. Важно отметить, что эти силы направлены параллельно слоям жидкости, то есть тангенциально к границе раздела.
Закон Пуазейля — это физический закон так называемого течения Пуазейля, то есть установившегося течения вязкой несжимаемой жидкости в тонкой цилиндрической трубке. Закон установлен эмпирически в 1839 году Г. Хагеном, а в 1840—1841 годы — независимо Ж. Л. Пуазейлем. Теоретически объяснён Дж. Г. Стоксом в 1845 году.При установившемся ламинарном движении вязкой несжимаемой жидкости сквозь цилиндрическую трубу круглого сечения секундный объёмный расход прямо пропорционален перепаду давления на единицу длины трубы и четвертой степени радиуса и обратно пропорционален коэффициенту вязкости жидкости.
— перепад давления на концах капилляра, Па; Q— секундный объёмный расход жидкости, м³ /с;
R— радиус капилляра, м; d— диаметр капилляра, м; 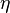 — коэффициент динамической вязкости, Па·с; l— длина трубы, Формула используется для определения вязкости жидкостей. Другим способом определения вязкости жидкости является метод, использующий закон Стокса.
— коэффициент динамической вязкости, Па·с; l— длина трубы, Формула используется для определения вязкости жидкостей. Другим способом определения вязкости жидкости является метод, использующий закон Стокса.
Билет5
1.Потенциал покоя
Экспериментально установлено, что между поверхностями биомембраны невозбужденной клетки существует разность потенциалов, часто называемая для краткости потенциалом покоя:
÷ (XII.1)
Однако до начала XX века этот вопрос (как и вообще природа электричества в живом организме) был предметом спора, суть которого можно коротко выразить тезисом: непонятно, возникает ли электричество, например, в мышце только в момент ее повреждения или существует и до него. Не имея возможности рассказать об истории этого спора до начала XX века, укажем, что только к этому времени Э. Бернштейну удалось понять, что электрические свойства мышц и нервов обусловлены не особенностями их устройства как целого, а свойствами и особенностями мембран составляющих их клеток. Этот ученый по праву считается основателем мембранной теории биопотенциалов (первая его статья была опубликована в 1902 г.).
Разберем, что такое потенциал покоя и как он возникает. Представим себе, что внутри клетки имеется много свободных ионов какого-нибудь элемента (рис. 1.) и клеточная мембрана пропускает только эти ионы. Естественно, они начнут двигаться наружу и вместе с ними наружу будет выноситься положительный заряд. В результате между внутренней и наружной поверхностями мембраны возникает разность потенциалов (рис. I.2.). Потенциал наружной поверхности будет больше, чем потенциал внутренней (при этом разность концентраций ионов внутри и снаружи будет к этому моменту еще довольно значительной). Эта разность потенциалов будет тормозить движение наружу новых положительных ионов и увеличивать их поток внутри клетки. В конце концов эти потоки станут равными по величине (установится динамическое равновесие), а суммарный поток будет равным нулю. Установившаяся при этом между поверхностями биомембраны разность электрических потенциалов и есть потенциал покоя.
Его величину можно вычислить из условия равенства электрохимических потенциалов внутри и снаружи летки  . Используя для нахождения электрохимического потенциала формулу, получим:
. Используя для нахождения электрохимического потенциала формулу, получим:
После несложных преобразований получим:
Разность 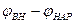 и есть обсуждаемый нами потенциал покоя:
и есть обсуждаемый нами потенциал покоя:
Очень слабым местом мембранной гипотезы в то время было отсутствие данных о том, концентрацию каких ионов следует подставлять в полученную формулу, чтобы получить значение 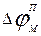 , близкое к наблюдаемому в эксперименте.
, близкое к наблюдаемому в эксперименте.
В 1905 г. в Берлине Гебер, один из молодых сотрудников Нернста, обнаруживает, что почти все соли, содержащие калий, оказывают на мышцу одинаковое действие: участок мышцы, на который действовал раствор такой соли, приобретал отрицательный потенциал по отношению к другим участкам. Бернштейн сразу же оценил значение работы Гебера: стоило только предположить, что потенциал покоя создается именно ионом калия и подставить в формулу соответствующие концентрации, как получался результат, близкий к эксперементальному.
Однако даже после выхода в 1912 г. в свет фундаментальной книги Э. Бернштейна «Электробиология» мембранная теория не вызывала особого доверия ученых, так как не было ее прямых подтверждений. Наиболее интенсивным нападкам подвергалось само существование мембраны (ее увидели при использовании электронной микроскопии лишь во второй половине XX века).
Еще одной экспериментальной проблемой было определение ионного состава внутренней среды. Ученые пытались использовать для определения этого состава самые разные методы, но все полученные данные были лишь приблизительными: клетки слишком малы, а между ними всегда имеются межклеточное вещество и жидкость. Кроме того, сторонникам мембранной теории надо было показать не просто присутствие калия внутри клеток, а присутствие именно свободных, несвязанных ионов калия. Эта проблема была решена с разработкой новых методов измерения и подбором подходящего объекта
В 1936 г. английский специалист по головоногим моллюскам Дж. Юнг обнаружил у кальмаров нервное волокно, диаметр которого доходил до 1 мм, т.е. гигантское по клеточным масштабам, хотя сам моллюск вовсе не был гигантом. Такое волокно, выделенное из организма и помещенное в морскую воду, не погибало. Появилась живая клетка, в которую можно было проникнуть, и с которой можно было работать.
2 Механизмы действия лазерного излучения на биологические ткани.
Лазерное излучение, так же как и обычный свет, может отражаться, поглощаться, рассеиваться, переизлучаться биологической средой, и каждый из этих процессов несет информацию о микро- и макроструктуре этой среды, движении и форме отдельных ее составляющих. Видимый и УФ свет могут оказывать фотобиохимическое действие. Яркими примерами этого являются фотосинтез растений и бактерий, а также механизм зрения [П. 1 — П. 3, 1]. Высокоинтенсивное световое излучение УФ, видимого и ИК диапазонов длин волн оказывает разрушающее (деструктивное) действие на биологические объекты. Необходимые интенсивности можно создать и не только с помощью лазеров. Существуют, например, фотокоагуляторы тканей глаза на основе мощных ксеноновых ламп [П. 22, П. 32].
Таким образом, процессы, характеризующие виды взаимодействий лазерного излучения с биообъектами, можно разделить на три группы. К первой относятся все невозмущающие взаимодействия (по крайней мере, в пределах погрешностей измерений не оказывающие заметного действия на биообъект), ко второй — процессы, в которых проявляется фотохимическое действие, и к третьей — процессы
3 Определение скорости кровотока.
Измерение времени кровотока в участках магистральных сосудов позволяет составить общее представление о сердечном выбросе: чем больше линейная скорость кровотока, тем больше и объемная скорость, т. е. величина сердечного выброса, и наоборот.До недавнего времени в клинике использовались методы определения скорости кровотока, основанные на внутривенном введении веществ, вызывающих через короткое время различные субъективные ощущения у пациента (хлорид кальция, магния сульфат, гистамин, дехолин, никотиновая кислота, эфир, лобелин и др.). Результаты этих исследований весьма сомнительны и зависят от многих факторов, не связанных с изменением времени кровотока (например с индивидуальными различиями в пороге субъективного ощущения индикатора и др.).Более информативными оказались неинвазивные метод разведения красителя и оксигемометрический метод.Оксигемометрия. Датчик оксигемометра помещают на мочку уха. Обследуемому предлагают сделать выдох и задержать дыхание. Возникающая при этом временная гипоксемия сопровождается постепенным снижением оксигемометрической кривой (рис. 3.306). После этого делают глубокий вдох, и через несколько секунд кривая начинает возвращаться к исходному уровню. Время от начала глубокого вдоха до начала подъема кривой соответствует времени кровотока на участке «легкое-ухо», которое в норме колеблется от 3, 0 до 5, 0 с.При определении скорости кровотока прямыми методами пользуются сравнительно сложными и трудоемкими методами и приборами. Применение их не всегда безразлично для организма исследуемого. Непрямые методы определения скорости кровотока делятся на объективные и субъективные. Непрямые объективные методы определения скорости кровотока основаны на том, что в ответ на введение в кровь исследуемого некоторых веществ возникают различные явления: кашель — после инъекции лабелина, глубокое дыхание — после эуфиллина, покраснение лица — после гистамина, папаверина и т. д. Эти методы широко распространены, но мы ими не пользовались. Непрямые субъективные методы определения скорости кровотока основаны на сигналах, подаваемых больными с возникновением ощущения на вводимые в вену вещества, о чем больные предупреждаются заранее. Например, при введении хлористого кальция, глюконата кальция и сернокислого магния больной сигнализирует о появлении чувства тепла, после инъекции сахарина и дехолина — о вкусовом ощущении, при введении эфира — о запахе и т. д. Все эти методы широко распространены. Мы пользовались магнезиальным методом, ибо в условиях наших исследований он оказался самым доступным и безопасным.
Билет6
1 ПОТЕНЦИАЛ ДЕЙСТВИЯ
Еще Э. Бернштейн изучал процесс возбуждения клеточной мембраны и предсказал измерение ее проницаемости для различных ионов. Однако завершить изучение этого вопроса он не успел. Примерно в 1939 г. Коул и Кертис (США) и Ходжкин и Хаксли (Великобритания) измеряли потенциалы невозбужденной и возбужденной клеток на гигантском аксоне кальмара: оказалось, что в состоянии покоя разность потенциалов была примерно равна -80 мВ (отрицательная), а максимальная разность потенциалов при возбуждении +40мВ (положительная). Далее Ходжкин и Хаксли сформулировали гипотезу о том, что при возбуждении меняется характер проницаемости мембраны для разного типа ионов: из проницаемой главным образом для калия она превращается в проницаемую для натрия и, следовательно, поток ионов натрия внутрь клетки увеличивается.
Разность потенциалов между поверхностями мембраны поднимается до нуля, а затем становится положительной – наступает деполяризация мембраны. Далее процесс развивается в обратном направлении: поток ионов натрия внутрь клетки постепенно уменьшается и возвращается к «невозбужденному» значению; разность потенциалов также возвращается к значению 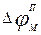 . Такой импульс (рис..3) называют потенциалом действия.
. Такой импульс (рис..3) называют потенциалом действия.
Ходжкин и Хаксли построили также электрическую модель процесса возбуждения, согласно этой модели мембрана представляется следующей схемой (рис. 4).
На рис.4. изображены конденсатор емкости С, два переменных резистора, которым соответствуют проводимости 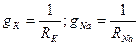 , 3 источника ЭДС, имитирующих равновесные, рассчитанные по формуле Нернста разности потенциалов для ионов калия, натрия и хлора, а также еще одно сопротивление (суммарное сопротивление мембраны для ионов хлора и ряда других) – соответствующая проводимость обозначена на схеме.
, 3 источника ЭДС, имитирующих равновесные, рассчитанные по формуле Нернста разности потенциалов для ионов калия, натрия и хлора, а также еще одно сопротивление (суммарное сопротивление мембраны для ионов хлора и ряда других) – соответствующая проводимость обозначена на схеме.
Согласно этой модели полный ток, протекающий через мембрану, равен сумме 4 слагаемых: где Iк – ток ионов калия; INa –ток ионов натрия; I’ – ток ионов хлора и остальных ионов, иногда называемый током утечки; 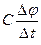 - емкостный ток (ток перезарядки мембраны), протекающий по той ветви цепи, куда включен конденсатор.
- емкостный ток (ток перезарядки мембраны), протекающий по той ветви цепи, куда включен конденсатор.
Рассмотрим сначала ток калия. Ионы калия идут через мембрану всегда, причем в обе стороны. Когда потенциал на мембране (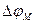 ) равен нернстовскому потенциалу, который иначе называют потенциалом равновесия для калия
) равен нернстовскому потенциалу, который иначе называют потенциалом равновесия для калия 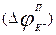 , то сохраняется динамическое равновесие, т.е. алиевый ток
, то сохраняется динамическое равновесие, т.е. алиевый ток 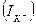 равен нулю. Если мембранный потенциал отклоняется от равновесного, то возникает калиевый ток, величину которого можно определить по закону Ома:
равен нулю. Если мембранный потенциал отклоняется от равновесного, то возникает калиевый ток, величину которого можно определить по закону Ома: 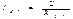 . Заменив
. Заменив 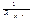 на калиевую проводимость
на калиевую проводимость 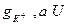 - на величину отклонения мембранного потенциала от равновесного, т.е., получаем:
- на величину отклонения мембранного потенциала от равновесного, т.е., получаем:
Аналогичной формулой определяется и сила натриевого тока:
,
Где  - равновесный натриевый потенциал, т.е. нернстовский потенциал для натрия, который равен примерно +40 мВ (он примерно равен овершуту – превышению нуля значением
- равновесный натриевый потенциал, т.е. нернстовский потенциал для натрия, который равен примерно +40 мВ (он примерно равен овершуту – превышению нуля значением 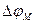 в точке максимума; Как видно, силы токов зависят от мембранного потенциала довольно сложным образом:
в точке максимума; Как видно, силы токов зависят от мембранного потенциала довольно сложным образом: 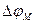 стоит в скобках и, кроме того, входит как аргумент в коэффициенты gк и gNa.
стоит в скобках и, кроме того, входит как аргумент в коэффициенты gк и gNa.
Зависимости проводимостей gк и gNa от времени при некотором неизменном мембранном потенциале изучали в опытах Ходжкина – Хаксли (опыты с фиксацией напряжения). За очень короткое время на мембране устанавливали фиксированную разность потенциалов и долго поддерживали ее. Это позволяло, в частности, избавиться от емкостных токов: если 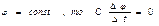 . Чтобы отдельно зарегистрировать токи ионов калия и натрия, использовали блокаторы. При введении тетраэтиламмония (блокатор калия) фиксировали зависимость тока ионов натрия от времени, при введении тетродотоксина – зависимость тока ионов калия от времени. Зависимость
. Чтобы отдельно зарегистрировать токи ионов калия и натрия, использовали блокаторы. При введении тетраэтиламмония (блокатор калия) фиксировали зависимость тока ионов натрия от времени, при введении тетродотоксина – зависимость тока ионов калия от времени. Зависимость 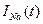 графически выражалась так, как показано на рис. 5. Графики1, 2 и 3 соответствовали различным значениям фиксированного потенциала. Для конкретности положим
графически выражалась так, как показано на рис. 5. Графики1, 2 и 3 соответствовали различным значениям фиксированного потенциала. Для конкретности положим 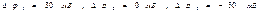 .
.
Рис. 5. позволяет, во-первых, сделать важный вывод о том, что проводимость gNa зависит от времени – ведь при постоянной разности потенциалов ток 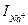 менялся во времени, а это возможно лишь при условии, что проводимость
менялся во времени, а это возможно лишь при условии, что проводимость 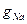 являлась функцией времени:
являлась функцией времени: 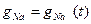 .
.
2 Применение лазерного излучения (НИЛИ, ВИЛИ)
. Благодаря своим уникальным свойством лазерное излучение стало использоваться в самых различных областях науки и техники. Лазерный луч можно использовать при прокладке туннелей, при укладке трубопроводов. С его помощью можно испарять самые тугоплавкие материалы, получить тончайшие отверстия в кости, керамике, сверхтвердых сплавах, полупроводниках. Высокая направленность излучения лазеров используется в радиолокации, лазерные дальномеры обеспечивают высокую точность измерения расстояний.Лазерный луч используется для передачи информации в космической среде. Лазерный луч позволяет производить хирургические операции на паренхиматозных органах. Операции при помощи лазерного луча кратковременны, безболезненны и дают возможность получить тонкие швы. Офтальмологи используют лазер для “приваривания” отслоившейся сетчатки к лежащей под ней сосудистой оболочке. С помощью лазерного луча возможно разрушение дентины при лечении зубов, приваривание зубных протезов непосредственно в полость рта, устранение повреждений голосовых связок, удаления шейных позвонков.В лазеротерапии применяют световые потоки низкой интенсивности, не более 100 мВТ/см2, что сопоставимо с интенсивностью излучения Солнца на поверхности Земли в ясный день. Поэтому его называют низкоинтенсивным лазерным излучением (НИЛИ). НИЛИ стимулирует метаболическую активность клетки, оказывает действие на процессы жизнедеятельности и регенерации (восстановления), приводит к увеличению содержания в ядрах клеток человека ДНК и РНК, оказывает антимутагенный эффект, активизирует синтез ДНК и ускоряет восстановительные процессы в клетках, подвергнутых радиации. Это позволяет использовать НИЛИ в онкологии, на вредных производствах, в военной медицине. НИЛИ стимулирует выработку универсального источника энергии АТФ в митохондриях, повышает эффективность работы дыхательной цепи митохондрий. Происходят перестройки в мембранах митохондрий, оказывается антиоксидантный эффект. При лазерной терапии изменяется соотношение насыщенных и ненасыщенных липидов, вязкость липидной компоненты мембран, что отражается на структурных перестройках в мембране, ее функциональном состоянии, активности мембрано-связанных ферментов. НИЛИ вызывает активацию энергосвязывающих процессов в патологически измененных тканях с нарушением метаболизма, повышение активности важнейших ферментов, снижения потребления кислорода тканями с повышением активности митохондрий, обогащением их энергией, усиление интенсивности гликолиза в тканях.
3 Физические основы реографии.
Реография - метод, который позволяет измерять кровенаполнение конечностей, мозга, сердца и многих других органов.Когда некоторый объем крови протекает через сосуды любого органа в течение систолы, объем этого органа увеличивается. Такие изменения объема изучались в прошлом с помощью, так называемой, плетизмографии, которая была основана на механических измерениях. Но возможности этого метода были ограничены. Он мог применяться только для изучения кровенаполнения верхних конечностей.Позже было обнаружено, что при изменении количества крови в сосудах органов, изменяется их электрическое сопротивление. Это изменение определяется формулой Кедрова:
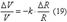 Здесь V - объем органа и Δ V - изменение объема в течение систолы, R – активное сопротивление и - Δ R изменение активного сопротивления органа в течение систолы, k - коэффициент прямой пропорциональности. Δ R имеет отрицательное значение, поскольку электрическое сопротивление крови меньше, чем сопротивление мышц, соединительной ткани, кожа и т.п. Поэтому активное сопротивление органов уменьшается в течение систолы и растет в течение диастолы.Изменение активного электрического сопротивления вызывает изменение полного сопротивления. По техническим причинам более удобно измерять именно изменения импеданса, чем изменения активного сопротивления постоянному току. В реографии кинетика полного сопротивления тела человека отражает частоту и объем локального кровенаполнения органов.Для измерения изменения полного сопротивления биологического объекта, через него пропускают переменный ток высокой частоты. Оптимальная частота, применяемая в реографии - 100 – 500кГц. При частотах выше 500 кГц сглаживаются различия в удельной электропроводности между кровью и окружающими тканями. Изменения полного сопротивления являются очень небольшими, их величина составляет: 0, 08Ом для голени и предплечья, 0, 1Ом для плеча и ступни.Основная (интегральная) реограмма отражает изменение импеданса исследуемого органа при кровенаполнении. Возрастающая часть кривой возникает вследствие систолы, а нисходящая - вследствие диастолы. Обычно одновременно записывается дифференциальная реограмма. Она является производной первого порядка по времени интегральной реограммы и описывает скорость изменения кровенаполнения исследуемого органа.Реография применяется для изучения кинетики полного электрического сопротивления различных органов: сердца (реокардиография), мозга (реоэнцефалография), печени (реогепатография), глаза (реоофтальмография) и т.п.
Здесь V - объем органа и Δ V - изменение объема в течение систолы, R – активное сопротивление и - Δ R изменение активного сопротивления органа в течение систолы, k - коэффициент прямой пропорциональности. Δ R имеет отрицательное значение, поскольку электрическое сопротивление крови меньше, чем сопротивление мышц, соединительной ткани, кожа и т.п. Поэтому активное сопротивление органов уменьшается в течение систолы и растет в течение диастолы.Изменение активного электрического сопротивления вызывает изменение полного сопротивления. По техническим причинам более удобно измерять именно изменения импеданса, чем изменения активного сопротивления постоянному току. В реографии кинетика полного сопротивления тела человека отражает частоту и объем локального кровенаполнения органов.Для измерения изменения полного сопротивления биологического объекта, через него пропускают переменный ток высокой частоты. Оптимальная частота, применяемая в реографии - 100 – 500кГц. При частотах выше 500 кГц сглаживаются различия в удельной электропроводности между кровью и окружающими тканями. Изменения полного сопротивления являются очень небольшими, их величина составляет: 0, 08Ом для голени и предплечья, 0, 1Ом для плеча и ступни.Основная (интегральная) реограмма отражает изменение импеданса исследуемого органа при кровенаполнении. Возрастающая часть кривой возникает вследствие систолы, а нисходящая - вследствие диастолы. Обычно одновременно записывается дифференциальная реограмма. Она является производной первого порядка по времени интегральной реограммы и описывает скорость изменения кровенаполнения исследуемого органа.Реография применяется для изучения кинетики полного электрического сопротивления различных органов: сердца (реокардиография), мозга (реоэнцефалография), печени (реогепатография), глаза (реоофтальмография) и т.п.
Билет7
1. Свойства жидкостей
Вещество в жидком состоянии сохраняет свой объем, но принимает форму сосуда. Если сила тяжести капли уравновешивается силой Архимеда, на каплю действуют только молекулярные силы, то она принимает форму шара. В состоянии невесомости жидкость принимает шарообразную форму и вне сосуда, что было проверено космонавтами. Сохранение объема у жидкости доказывает, что между ее молекулами действуют силы притяжения. Следовательно, расстояния между молекулами жидкости должны быть меньше радиуса молекулярного действия. Если вокруг какой-либо молекулы жидкости описать сферу молекулярного действия, то внутри этой сферы окажутся центры многих других молекул, которые будут взаимодействовать с этой молекулой. Эти силы взаимодействия удерживают молекулу жидкости около ее временного положения равновесия примерно в течение 10-12 – 10-10 сек., после чего она перескакивает в новое временное положение равновесия приблизительно на расстояние своего диаметра. Молекулы жидкости между переходами совершают колебательное движение около временного положения равновесия. Время между переходами молекулы из одного положения в другое называется временем оседлой жизни. Это время зависит от вида жидкости и от температуры. При нагревании жидкости среднее время оседлой жизни молекул уменьшается.
Жидкость обладает текучестью, вызванной тем, что время действия внешней силы обычно во много раз больше времени релаксации, поэтому жидкость течет и принимает форму сосуда, в котором она находится. В небольшом объеме жидкости наблюдается упорядоченное расположение ее молекул, а в большом объеме оно оказывается хаотическим. В этом смысле говорят, что в жидкости существует ближний порядок в расположении молекул и отсутствует дальний порядок. Такое строение жидкости называют квазикристаллическим (кристаллоподобным). В некоторых жидкостях с удлиненной формой молекул возможна единообразная ориентация их по всему объему. Такие жидкости называются жидкими кристаллами, а свойства их отличаются от обычных жидкостей.
При достаточно сильном нагревании время оседлой жизни становится очень маленьким и ближний порядок в жидкости практически исчезает.
Жидкость может обнаруживать механические свойства, присущие твердому телу. Если время действия силы на жидкость мало, то жидкость проявляет упругие свойства. Например, при резком ударе палкой о поверхность воды палка может вылететь из руки или сломаться; камень можно бросить так, что он при ударе о поверхность воды отскакивает от нее, и лишь совершив несколько скачков, тонет в воде. Если же время воздействия на жидкость велико, то вместо упругости проявляется текучесть жидкости. Например, рука легко проникает внутрь воды.
При кратковременном действии силы на струю жидкости последняя обнаруживает хрупкость.
Сжимаемость жидкости больше, чем у этих же веществ в твердом состоянии. Например, при увеличении давления на 1 атм объем воды уменьшается на 50 миллионных долей.
Разрывы внутри жидкости, в которой нет посторонних веществ, например воздуха, могут получаться только при интенсивном воздействии на жидкость, например при распространении в жидкости ультразвуковых волн. Такого рода пустоты внутри жидкости долго существовать не могут и резко захлопываются, т.е. исчезают. Это явление называют кавитацией (от греческого «кавитас» -полость).
2 Спектрофотометрия.Спектрофотометрия - область измерительной техники, разрабатывающая методы и приборы для определения спектральных характеристик объектов. В медико-биологических исследованиях очень большоезначение имеет анализ молекулярных и атомных спектров поглощении. С помощью спектрофотометров в различных биологических пробах определяют содержание ферментов, гормонов, белков, витаминов, многих неорганических веществ, анализируют качественный и количественный состав мазков крови и т. Д.В основе спектрофотометрии лежит регистрация степени ослабления монохроматического пучка света при его прохождении через вещество (закон Бугера—Ламберта— Бера.Закон Бугера-Ламберта-Бера справедлив лишь для плоскопараллельного пучка монохроматического света и при выполнении ряда условий. На практике часто приходится сталкиваться с отклонениями от этого закона. К числу причин отклонения могут быть отнесены физико-химические свойства анализируемого вещества или раствора (диссоциация, флюоресценция и др.), инструментальные факторы (например: отсутствие должной степени монохроматичности пучка света), факторы обусловленные неоднородностью изучаемого объекта в пучке света (особенно отчетливо проявляется при микроспектрофотометрии объектов)Важным принципом спектрофотометрии является принцип оптических плотностей, в соответствии с которым величина оптической плотности смеси соединений, подчиняющихся закону Бугера-Ламберта-Бера и не вступающих в хим. взаимодействие друг с другом, равна сумме оптических плотностей этих соединений.Количественный анализ пробы, содержащей одно вещество, включает следующие операции: 1) регистрацию полного спектра поглощения вещества (D измеряют как функцию длины волны 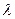 ), выбор аналитической длины волны (
), выбор аналитической длины волны (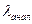 ), приготовление 6-7 эталонных (стандартных) растворов, охватывающих весь ожидаемый диапазон концентраций определяемого вещества и измерение оптической плотности
), приготовление 6-7 эталонных (стандартных) растворов, охватывающих весь ожидаемый диапазон концентраций определяемого вещества и измерение оптической плотности 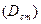 этих растворов при
этих растворов при 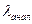 . Затем строят график зависимости величины оптической плотности
. Затем строят график зависимости величины оптической плотности 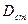 от концентрации. Наиболее точные результаты дают измерения оптической плотности в диапазоне 0, 05-1, 50. Оптическая плотность анализируемого раствора во всех случаях измеряется относительно раствора сравнения (прямой спектрофотометрический метод). В качестве раствора сравнения может быть использован чистый растворитель или раствор, содержащий все компоненты анализируемого раствора, за исключением определяемого вещества. В ряде случаев в качестве раствора сравнения целесообразно использовать раствор определяемого вещества известной концентрации (обычно более низкой, чем в анализируемых пробах). При проведении такого рода измерений говорят о дифференциальной спектрофотометрии.Нередко проводят регистрацию производных спектров поглощения. Производную спектрофотометрию применяют в основном в качественном анализе при идентификации мало поглощающих примесей, установлении структуры органических соединений и.т.д.Спектрофотометрия проводится в инфракрасной (ИК), УФ и видимой областях спектра.К приборам, работающим в видимой области, относятся также спектрофотометры комбинационного рассеяния, которые изучают колебательные энергетические уровни молекул. Они могут быть использованы для определения связей в белках, числа спаренных и неспаренных оснований в нуклеиновых кислотах.Спектрофотометрия микрообъектов или микроспектрофометрия - относительно самостоятельная область исследования. Микроспектрофотометры, как и микроспектрофлуориметры, обычно предназначены для работы в видимой области спектра, реже в УФ-области выполняются по однолучевой схеме. Для регистрации распределения поглощающего вещества по площади микрообъекта используют различного рода сканирующие устройства: систему оптических зондов, перемещающиеся по заданной программе предметные столики, телевизионную (электронную) развертку изображения. Приборы сканирующей конструкции снабжаются микрокомпьютерами, которые автоматически обрабатывают получаемую информацию и позволяют анализировать форму микрообъектов. Например, при автоматическом анализе мазков крови. Скоростной анализ флуоресцентных характеристик индивидуальных клеток крови, окрашенных соответствующими красителями проводится в проточных микрофлуориметрах. Наметилась тенденция к разработке узкоспециализированных микроспектрофотометров и микроспектрофлуориметров, предназначенных для работы в условиях клинических лабораторий.Атомарные спектры поглощения изучают с помощью пламенных спектрофотометров. Атомно-абсорбционные методы дают возможность определения практически всех элементов периодической системы и отличаются высокой избирательностью и чувствительностью (до
от концентрации. Наиболее точные результаты дают измерения оптической плотности в диапазоне 0, 05-1, 50. Оптическая плотность анализируемого раствора во всех случаях измеряется относительно раствора сравнения (прямой спектрофотометрический метод). В качестве раствора сравнения может быть использован чистый растворитель или раствор, содержащий все компоненты анализируемого раствора, за исключением определяемого вещества. В ряде случаев в качестве раствора сравнения целесообразно использовать раствор определяемого вещества известной концентрации (обычно более низкой, чем в анализируемых пробах). При проведении такого рода измерений говорят о дифференциальной спектрофотометрии.Нередко проводят регистрацию производных спектров поглощения. Производную спектрофотометрию применяют в основном в качественном анализе при идентификации мало поглощающих примесей, установлении структуры органических соединений и.т.д.Спектрофотометрия проводится в инфракрасной (ИК), УФ и видимой областях спектра.К приборам, работающим в видимой области, относятся также спектрофотометры комбинационного рассеяния, которые изучают колебательные энергетические уровни молекул. Они могут быть использованы для определения связей в белках, числа спаренных и неспаренных оснований в нуклеиновых кислотах.Спектрофотометрия микрообъектов или микроспектрофометрия - относительно самостоятельная область исследования. Микроспектрофотометры, как и микроспектрофлуориметры, обычно предназначены для работы в видимой области спектра, реже в УФ-области выполняются по однолучевой схеме. Для регистрации распределения поглощающего вещества по площади микрообъекта используют различного рода сканирующие устройства: систему оптических зондов, перемещающиеся по заданной программе предметные столики, телевизионную (электронную) развертку изображения. Приборы сканирующей конструкции снабжаются микрокомпьютерами, которые автоматически обрабатывают получаемую информацию и позволяют анализировать форму микрообъектов. Например, при автоматическом анализе мазков крови. Скоростной анализ флуоресцентных характеристик индивидуальных клеток крови, окрашенных соответствующими красителями проводится в проточных микрофлуориметрах. Наметилась тенденция к разработке узкоспециализированных микроспектрофотометров и микроспектрофлуориметров, предназначенных для работы в условиях клинических лабораторий.Атомарные спектры поглощения изучают с помощью пламенных спектрофотометров. Атомно-абсорбционные методы дают возможность определения практически всех элементов периодической системы и отличаются высокой избирательностью и чувствительностью (до 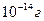 ).
).
Приборы для спектрального анализа комплектуются электронными устройствами обработки и управления, блоками автоматической подачи проб, самописцами, блоками цифровой печати, устройствами автоматической развертки спектра, позволяют определять по одной пробе несколько элементов
Спектрофотометрия широко применяется в биологических исследованиях. Она используется для количественного определения самых разнообразных биологических соединений: ферментов, витаминов, гормонов, белков и других азотистых веществ, нуклеииовых кислот, углеводов, спиртов, альдегидов, фенолов, кетонов, органических кислот, липидов, пигментов, ряда неорганических веществ (например, натрия, калия, кальцин, железа. цинка, хлора, серы) и др.
Приборы. Основными узлами спектрофотометров обычно являются: источник излучения; монохроматор, предназначенный для выделения из спектра излучения источника узких спектральных интервалов; приемник излучения; отсчетное устройство. Спектрофотометры подразделяются на однолучевые и двухлучевые, нерегистрирующие и регистрирующие. Распространенные в медицинских лабораториях однолучевые нерегистрирующие спектрофотометры представляют собой достаточно простые и дешевые приборы с оптикой из оптического стекла или кварца. Использование кварцевой оптики дает возможность проводить измерения в области 200 - 1100 нм, охватывающей ультрафиолетовый, видимый и ближний инфракрасный участки спектра. Исследуемый образец и эталон последовательно вводят в световой пучок. Результаты сравнения пучков в величинах пропускания (в %) или оптической плотности (D) указываются на стрелочном или цифровом приборе.
Источником света спектрофотометров обычно служит водородная лампа (для работы в области спектра 220—320 нм ) или лампа накаливания (для работы в области спектра 320 - 1100 нм ). Луч света через систему зеркал попадает на диспергирующую призму, которая разлагает его, образуя спектр.
3 Гемодинамика.Линейная и объемная скорость кровотока.
Гемодинамика — движение крови по сосудам, возникающее вследствие разности гидростатического давления в различных участках кровеносной системы (кровь движется из области высокого давления в область низкого). Зависит от сопротивления току крови стенок сосудов и вязкости самой крови. О гемодинамике судят по минутному объёму крови. Существует множество нарушений гемодинамики, связанных с травмами, переохлаждениями, ожогами и т. д. Кровь в кровеносной системе непрерывно циркулирует, совершая полный оборот за 27 систол, т.е. за 20-23 секунды. Роль насоса выполняет сердце.Фактически сердце выполняет функции двух насосов, работающих в последовательной гидравлической сети, которая замкнута сама на себя. Последовательность прохождения полного круга любой порцией крови такова: правое предсердие – правый желудочек – малый круг кровообращения – левое предсердие – левый желудочек – большой круг кровообращения- правое предсердие -... и т.д.Поскольку эта система последовательная, количество крови, выталкиваемое при каждом сокращении левым и правым желудочками одинаковое, и составляет, в условиях покоя, 60 – 80 мл. Этот показатель – основной показатель сократительной деятельности сердца – называется систолическим (ударным) объемом. При больших физических и эмоциональных нагрузках он может увеличиваться в 2-3 раза.При стандартной процедуре измерения артериального давления (метод Короткова) измеряется наибольшее (систолическое) и наименьшее (диастолическое) давление крови в большом круге кровообращения. Результатам измерений 120/80 мм рт. столба соответствует среднее значение примерно 100 мм рт. столба. Следовательно, левый желудочек выталкивает ударный объем крови V в условиях, когда противодействует этому давление порядка 100 мм рт. столба. В малом круге кровообращения аналогичные значения давлений и их средний уровень примерно в шесть раз ниже. Среднее давление «на выходе» правого желудочка – порядка 15 мм рт. столба, и этому желудочку протолкнуть такой же по величине ударный объем V значительно легче. Так что затраты энергии в левом и правом желудочках отличаются тоже примерно в шесть раз.
Линейная скорость потока крови (кровотока) - это физическая величина, являющаяся мерой движения частиц крови, составляющих поток. Теоретически она равна расстоянию, проходимому частицей вещества, составляющего поток, в единицу времени: v = L / t. Здесь L - путь (м), t - время (c). Кроме линейной скорости кровотока различают объёмную скорость потока крови, или объёмную скорость кровотока. Средняя линейная скорость ламинарного кровотока (v) оценивается интегрированием линейных скоростей всех цилиндрических слоев потока: v = (dP · r4) / (8η · l), где: dP - разница давления крови в начале и в конце участка кровеносного сосуда, r - радиус сосуда, η - вязкость крови, l - длина участка сосуда, коэффициент 8 - это результат интегрирования скоростей, движущихся в сосуде слоев крови. Объемная скорости кровотока (Q) и линейная скорости кровотока связаны отношением: Q = v · π · r2.Подставив в это отношение выражение для v получим уравнение («закон») Хагена-Пуазейля для объёмной скорости кровтотка: Q = dP · (π · r4 / 8η · l) (1). Исходя из простой логики, можно утверждать, что объёмная скорость любого потока прямо пропорциональна движущей силе и обратно пропорциональна сопротивлению потоку. Аналогично, объёмная скорость кровотока (Q) прямо пропорциональна движущей силе (градиент давления, dP), обеспечивающей кровоток, и обратно пропорциональна сопротивлению кровотоку (R): Q = dP / R. Отсюда R = dP / Q. Подставляя в это отношение выражение (1) для Q, получим формулу для оценки сопротивления кровотоку: R = (8η · l) / (π · r4). Из всех этих формул видно, что самой значимой переменной, определяющей линейную и объёмную скорости кровотока, является просвет (радиус) сосуда. Эта переменная является главной переменной
Билет8
1 Молекулы, находящиеся в глубине жидкости, окружены молекулами жидкости со всех сторон и их действия на эти молекулы взаимно уравновешиваются. У молекул, находящихся в поверхностном слое жидкости, на границе с газообразной средой, слабое взаимодействие с молекулами пара или воздуха над жидкостью. Им можно пренебречь. Это придает поверхностному слою жидкости (толщиной, равной радиусу сферы молекулярного взаимодействия) специфические особенности. На каждую молекулу в поверхностном слое со стороны окружающих ее молекул жидкости действуют силы по двум направлениям: вдоль (по касательной) и перпендикулярно (нормально) к поверхности жидкости. Нормальные составляющие, складываясь между собой, приводят к возникновению силы, направленной перпендикулярно поверхностному слою, в глубь жидкости. Давление молекул поверхностного слоя на соседний, расположенный ниже, слой молекул жидкости получил название молекулярного давления. Силы молекулярного давления действуют только на молекулы самой жидкости и не действуют на тело, погруженное в жидкость.  Касательные составляющие молекулярных сил направлены вдоль поверхностного слоя, они сближают молекулы поверхностного слоя, и поверхностный слой оказывается в состоянии напряжения. Они получили название сил поверхностного натяжения.
Касательные составляющие молекулярных сил направлены вдоль поверхностного слоя, они сближают молекулы поверхностного слоя, и поверхностный слой оказывается в состоянии напряжения. Они получили название сил поверхностного натяжения.
|
|